Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
AminoglycosidesArikayce
Résumé
Qu'est-ce que Arikayce?
Arikayce (Amikacin Liposome Inhalation Suspension) est un aminoglycoside antibactérien Indiqué chez les adultes qui ont des options de traitement limitées ou non alternatives pour le traitement de la maladie pulmonaire du complexe Mycobacterium avium (MAC) dans le cadre d'un régime antibactérien combiné chez les patients qui n'atteignent pas les cultures d'expectorations négatives après un minimum de 6 mois consécutifs d'une thérapie multidrogue du régime de fond. Ce médicament est indiqué pour une utilisation dans une population limitée et spécifique de patients.
Quels sont les effets secondaires d'Arikayce?
Arikayce
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- toux (surtout pendant le premier mois d'utilisation du médicament)
- Diagramme à parler
- sonner dans vos oreilles
- Changements en audition
- vertiges
- sensation de rotation
- étourdissement
- étanchéité
- respiration sifflante
- essoufflement
- cracher du sang
- peu ou pas de miction
- gonflement dans vos pieds ou chevilles et
- fatigue
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires courants d'Arikayce comprennent:
- difficulté à parler
- toux
- bronchospasme
- cracher du sang
- endommager l'oreille intérieure
- irritation des voies respiratoires supérieures
- douleur musculo-squelettique
- fatigue
- faiblesse
- aggravation des maladies pulmonaires sous-jacentes
- diarrhée et
- nausée
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; et des étourdissements soudains étourdisseurs ou s'évanouissant;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Arikayce
La dose recommandée d'Arikayce chez les adultes est une fois par inhalation orale quotidienne du contenu d'un flacon Arikayce de 590 mg / 8,4 ml. Utilisez des flacons Arikayce uniquement avec le système de nébuliseur Lamira.
Quelles substances ou suppléments de médicaments interagissent avec Arikayce?
Arikayce peut interagir avec le furosémide d'acide éthacrynique urée Mannitol ou médicaments intraveineux associés à la néphrotoxicité et à l'ototoxicité de la neurotoxicité. Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Arikayce pendant la grossesse ou l'allaitement
Dites à votre médecin si vous êtes enceinte ou prévoyez de tomber enceinte avant d'utiliser Arikayce; Cela peut nuire à un fœtus. On ne sait pas si Arikayce passe dans le lait maternel. Consultez votre médecin avant l'allaitement.
Informations Complémentaires
Notre Arikayce (Amikacin Reposome Inhalation Suspension) pour le centre de médicaments à effets secondaires de l'inhalation orale offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Dosage
- Effets secondaires
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Risque d'augmentation des effets indésirables respiratoires
Arikayce a été associé à un risque accru de réactions indésirables respiratoires, notamment l'exacerbation de la pneumonite à la pneumonite hémoptysie de la pneumonite hémoptysie des maladies pulmonaires sous-jacentes qui ont conduit à des hospitalisations dans certains cas [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Description d'Arikayce
L'ingrédient actif de Arikayce (Amikacin Reposome Inhalation Suspension) est le sulfate d'amikacine USP un antibactérien d'aminoglycoside. Son nom chimique est la d-streptamine O -3-amino-3-désoxy-α-dglucopyranosyl- (1 → 6) - O - [6-amino-6-désoxy-α-d-glucopyranosyl- (1 → 4)] - N 1 - (4-amino-2-hydroxy-1oxobutyl) -2-désoxy- ( S ) - sulfate (1: 2) sel avec une formule chimique de c 22 H 43 N 5 O 13 • 2h 2 DONC 4 avec un poids moléculaire de 781,76. Sa formule structurelle est:
 |
Arikayce est une suspension laiteuse blanche composée de sulfate d'amikacine encapsulé dans des liposomes et est fournie dans une dose unitaire 10 ml de flacon en verre transparent contenant de l'amikacine 590 mg / 8,4 ml (équivalent à la suspension de liposomale aqueuse d'amikacine 623 mg / 8,4 ml) en tant que suspension aqueuse stérile aqueuse pour l'inhalation orale. Arikayce se compose de sulfate d'amikacine encapsulé dans des liposomes à une concentration ciblée de 70 mg d'amikacine / ml avec une plage de pH de 6,1 à 7,1 et un rapport de poids lipide / amikacine dans la plage de 0,60 à 0,79. Les ingrédients inactifs sont le cholestérol dipalmitoylphosphatidylcholine (DPPC) du chlorure de sodium hydroxyde de sodium (pour l'ajustement du pH) et l'eau pour l'injection.
Arikayce est administré uniquement à l'aide d'un système de nébuliseur Lamira [voir Posologie et administration ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factous. Under stetardized in vitro Test par USP <1601> Modèle de respiration adulte (500 ml de volume de marée 15 respirations par minute et inhalation: rapport d'exhalation de 1: 1) La dose moyenne livrée par l'embout buccal était d'environ 312 mg de sulfate d'amikacin (53% de la revendication de l'étiquette). Le diamètre aérodynamique médian de masse (MMAD) des gouttelettes d'aérosol nébulisés est d'environ 4,7 μm (NULL,1 - 5,3 μm), tel que déterminé en utilisant la méthode de la prochaine génération (NGI). Un pourcentage de l'amikacine dans le liposome est libéré par le processus de nébulisation, donc Arikayce nébulisé fournit une combinaison d'amikacine libre et liposomale.
Utilisations pour Arikayce
Population limitée: Arikayce ® est indiqué chez les adultes qui ont des options de traitement limitées ou non alternatives pour le traitement de Mycobacterium avium Maladie pulmonaire complexe (MAC) dans le cadre d'un schéma de médicament antibactérien combiné chez les patients qui n'atteignent pas les cultures d'expectorations négatives après un minimum de 6 mois consécutifs d'un traitement par un régime de fond multidrogue. Comme seules les données limitées de la sécurité et de l'efficacité cliniques pour Arikayce sont actuellement disponibles pour réserver Arikayce pour une utilisation chez les adultes qui ont des options de traitement limitées ou pas alternatives. Ce médicament est indiqué pour une utilisation dans une population limitée et spécifique de patients.
Cette indication est approuvée sous l'approbation accélérée en fonction de la réalisation de la conversion de la culture des expectorations (définie comme 3 cultures d'expectorations mensuelles négatives consécutives) d'ici le mois 6. L'avantage clinique n'a pas encore été établi [voir Études cliniques ]. Continued approval fou this indication may be contingent upon verification et description of clinical benefit in confirmatouy trials.
Limitation d'utilisation
Arikayce n'a été étudié que chez des patients atteints d'une maladie pulmonaire MAC réfractaire définie comme des patients qui n'ont pas obtenu de cultures d'expectorations négatives après un minimum de 6 mois consécutifs d'un traitement au régime multidrogue. L'utilisation d'Arikayce n'est pas recommandée pour les patients atteints d'une maladie pulmonaire MAC non réfractaire.
Dosage pour Arikayce
Instructions d'administration importantes
Arikayce est pour une utilisation par inhalation orale uniquement. Administrer par nébulisation uniquement avec le lamira ® Système de nébuliseur. Reportez-vous aux instructions d'utilisation des informations d'administration complètes sur l'utilisation d'Arikayce avec le système de nébuliseur Lamira.
Instruisez les patients utilisant un bronchodilatateur («releveur») pour utiliser d'abord le bronchodilatateur suivant la brochure de bronchodilatrice pour utiliser des informations avant d'utiliser Arikayce.
Le prétraitement avec des agonistes sélectifs à action sélective à action courte doit être pris en compte pour les patients atteints de maladie hyperréactive des voies respiratoires chroniques asthme ou bronchospasme de maladie pulmonaire chronique [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Dosage recommandé
La dose recommandée d'Arikayce chez les adultes est une fois par inhalation quotidienne du contenu d'un flacon Arikayce de 590 mg / 8,4 ml (590 mg d'amikacin) en utilisant le système de nébuliseur Lamira [voir [voir Études cliniques ].
Administrer Arikayce avec le système de nébuliseur Lamira uniquement. Arikayce doit être à température ambiante avant utilisation. Avant d'ouvrir, secouez le flacon Arikayce pendant au moins 10 à 15 secondes jusqu'à ce que le contenu semble uniforme et bien mélangé. Le flacon Arikayce est ouvert en retournant le haut en plastique du flacon puis en tirant vers le bas pour desserrer l'anneau métallique. L'anneau métallique et le bouchon en caoutchouc doivent être retirés soigneusement. Le contenu du flacon Arikayce peut ensuite être versé dans le réservoir de médicaments du combiné Nebulizer.
Si une dose quotidienne d'Arikayce est manquée, administrez la dose suivante le lendemain. Ne doublez pas la dose pour compenser la dose manquée.
Comment fourni
Dosage Foums And Strengths
Arikayce est fourni sous forme de suspension de liposomes aqueux blanc laiteux blanc stérile pour l'inhalation orale dans un flacon de verre dose unitaire contenant l'amikacine 590 mg / 8,4 ml (équivalent au sulfate d'amikacine 623 mg / 8,4 ml).
Arikayce (Suspension inhalation des liposomes d'amikacine) 590 mg / 8,4 ml est fourni dans un flacon de verre stérile-dose unitaire de 10 ml. Le produit est distribué comme un kit de 28 vives.
Chaque carton contient une alimentation de 28 jours de médicaments (28 flacons). En plus des flacons Arikayce dans le combiné de nébulizage Carton One Lamira et quatre têtes d'aérosol Lamira sont fournies.
NDC 71558-590-28
Le système de nébuliseur Lamira contient un contrôleur une tête d'aérosol de rechange un cordon d'alimentation et des accessoires d'alimentation du combiné de rechange.
Stockage et manipulation
Conserver les flacons Arikayce réfrigérés à 2 ° C à 8 ° C (36 ° F à 46 ° F) jusqu'à la date d'expiration du flacon. Ne congelez pas . Une fois expiré, jetez tout médicament inutilisé.
Arikayce can be stoued at room temperature up to 25°C (77°F) fou up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Fabriqué pour: INSMED Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Révisé: février 2023
Effets secondaires pour Arikayce
Les effets indésirables cliniquement significatifs suivants sont décrits plus en détail dans d'autres sections d'étiquetage:
- Pneumonite d'hypersensibilité [voir Avertissement de boîte et AVERTISSEMENTS AND PRÉCAUTIONS ]
- Hémoptysie [voir Avertissement de boîte et AVERTISSEMENTS AND PRÉCAUTIONS ]
- Bronchospasme [voir Avertissement de boîte et AVERTISSEMENTS AND PRÉCAUTIONS ]
- Exacerbation des maladies pulmonaires sous-jacentes [voir Avertissement de boîte et AVERTISSEMENTS AND PRÉCAUTIONS ]
- Réactions d'anaphylaxie et d'hypersensibilité [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Ototoxicité [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Néphrotoxicité [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Blocage neuromusculaire [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions de réaction indésirables très variables observées dans les essais cliniques d'un médicament ne peuvent pas être directement comparées aux taux dans les essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans la pratique.
Aperçu des essais cliniques pour l'évaluation de la sécurité
Au sein du programme clinique NTM réfractaire, 404 patients qui ont participé à trois essais cliniques ont été traités avec Arikayce à la dose de 590 mg / jour (la durée médiane de l'exposition à Arikayce était de 236,5 jours).
Essai 1 (NCT Mycobacterium avium Maladie pulmonaire complexe (MAC). Les patients ont été randomisés à 8 mois d'Arikayce plus un régime de fond (n = 223) ou un régime de fond seul (n = 112).
Essai 2 (NCT
Essai 3 (NCT Mycobacterium . Les patients ont été randomisés dans le régime de fond Arikayce Plus (n = 44) ou un régime de liposomes lidues dilué inhalé plus schéma de fond (n = 45) pendant 84 jours.
Dans tous les essais cliniques de patients atteints et sans infection pulmonaire NTM réfractaire, 818 patients ont été exposés à de multiples doses d'Arikayce.
Réactions indésirables conduisant à l'arrêt du traitement
Dans les trois études NTM, il y a eu une incidence plus élevée d'arrêt prématuré de l'Arikayce. Dans l'essai 1, 34,5% ont interrompu Arikayce prématurément; La plupart étaient dus à des effets indésirables (NULL,8%) et au retrait par sujet (NULL,9%). Dans le bras du comparateur, 10,7% des sujets ont interrompu leur régime de fond avec 0,9% en raison de réactions indésirables et de 5,4% en raison du retrait par sujet. Dans l'essai 2 (l'extension à bras unique de l'essai 1), 37,8% des patients commençant par Arikayce ont arrêté prématurément avec 24,4% d'arrêt en raison de réactions indésirables. Dans l'essai 3, les 9 (NULL,5%) des arrêts prématurés se sont produits chez les patients traités au régime Arikayce Plus et il n'y a eu aucune interruption prématurée dans le bras du régime de fond placebo plus.
Réactions indésirables graves dans les essais 1 et 3
Dans l'essai 1, 19,7% des patients traités par un régime de fond Arikayce plus ont signalé un SAR par rapport à 16,1% des patients traités par un régime de fond seul. De plus, dans l'essai 1 [2 à 1 randomisation Arikayce plus le régime de fond en fonction du régime de fond seul] Il y a eu 80 hospitalisations chez 41 patients (NULL,4%) traités par un schéma de fond Arikayce plus par rapport à 29 hospitalisations chez 15 patients (NULL,4%) traités par un régime de fond seul. Les SRAS et les raisons les plus courants de l'hospitalisation dans le bras du régime de fond d'Arikayce plus étaient liés à l'exacerbation de la maladie pulmonaire sous-jacente et aux infections des voies respiratoires plus faibles telles que la pneumonie. Dans l'essai 3, 18,2% des patients traités par un régime de fond Arikayce plus ont signalé un SRAS, contre 8,9% des patients traités par un schéma de fond plus un placebo inhalé.
Réactions indésirables courantes
L'incidence des effets indésirables dans l'essai 1 est affichée dans le tableau 1. Seuls les effets indésirables avec un taux d'au moins 5% dans le groupe Arikayce Plus de fond et supérieur au groupe de régimes de fond seul sont indiqués.
Tableau 1: Réactions indésirables chez ≥ 5% des patients MAC traités par Arikayce et plus fréquent que le régime de fond seul dans l'essai 1
| Réaction indésirable | Arikayce plus Background Regimen (N = 223) n (%) | Régime de fond seul (N = 112) n (%) |
| Dysphonie a | 106 (48) | 2 (2) |
| Toux b | 88 (40) | 19 (17) |
| Bronchospasme c | 64 (29) | 12 (11) |
| Hémoptysie | 41 (18) | 15 (13) |
| Douleur musculo-squelettique d | 40 (18) | 10 (9) |
| Irritation des voies respiratoires supérieures e | 39 (18) | 2 (2) |
| Élitude f | 38 (17) | 11 (10) |
| Fatigue et asthénie | 36 (16) | 11 (10) |
| Exacerbation des maladies pulmonaires sous-jacentes g | 34 (15) | 11 (10) |
| Diarrhée | 28 (13) | 5 (5) |
| Nausée | 26 (12) | 4 (4) |
| Mal de tête | 22 (10) | 5 (5) |
| Pneumonie h | 20 (9) | 10 (9) |
| Pyrexie | 17 (8) | 5 (5) |
| Le poids a diminué | 16 (7) | 1 (1) |
| Vomissement i | 15 (7) | 4 (4) |
| Éruption cutanée j | 14 (6) | 1 (1) |
| Changement des expectorations k | 13 (6) | 1 (1) |
| Malaise | 12 (5) | 3 (3) |
| a Comprend l'aphonie et la dysphonie b Comprend la toux de la toux et le syndrome de la toux des voies respiratoires supérieures c Comprend l'asthme Bronchial Hyperreactivité Bronchospasme Dyspnée Dyspnée exercée d Comprend des douleurs au dos arthralgie myalgie douleur / corps morte le spasme musculaire et la douleur musculo-squelettique e Comprend une douleur oropharyngée inconfort l'oropharyngée irritation irritation pharyngée érythème inflammation des voies respiratoires supérieures f Comprend la surdité de la surdité de surdité neurosensorielle des étourdissements unilatéraux hypoacusis présyncope g Comprend une exacerbation infectieuse de la MPOC de l'exacerbation infectieuse de la MPOC de la bronchectasie h Comprend une infection pleurale de pneumonie atypique. i Comprend des vomissements et des vomissements post-tussive j Comprend une éruption de médicament maculo-papulaire éruption cutanée et l'urticaire k Comprend une augmentation des expectorations spitumaires et des expectorations décolorées |
Sélectionné les réactions indésirables médicamenteuses qui se sont produites dans <5% of patients et at higher frequency in Arikayce-treated patients in Trial 1 are presented in Table 2.
Tableau 2: Réactions indésirables sélectionnées dans <5% of Arikayce-treated MAC Patients et Moue Frequent than Régime de fond seul in Trial 1
| Réaction indésirable | Arikayce plus Background Regimen N = 223 n (%) | Régime de fond seul N = 112 n (%) |
| Anxiété a | 10 (5) | 0 (0) |
| Infection fongique orale b | 9 (4) | 2 (2) |
| Bronchite | 8 (4) | 3 (3) |
| Dysgeusie | 7 (3) | 0 (0) |
| Pneumonite d'hypersensibilité c | 7 (3) | 0 (0) |
| Bouche sèche | 6 (3) | 0 (0) |
| Épistaxis | 6 (3) | 1 (1) |
| Insuffisance respiratoire d | 6 (3) | 2 (2) |
| Pneumothorax e | 5 (2) | 1 (1) |
| La tolérance à l'exercice a diminué | 3 (1) | 0 (0) |
| Trouble de l'équilibre | 3 (1) | 0 (0) |
| Trouble neuromusculaire f | 2 (1) | 0 (0) |
| a Comprend l'anxiété et le trouble de l'anxiété b Comprend la candidose orale et l'infection fongique buccale c Comprend l'alvéolite allergique maladie pulmonaire interstitielle et la pneumonite d Comprend une insuffisance respiratoire aiguë et une insuffisance respiratoire e Comprend le pneumothorax pneumothorax spontané et pneumomediastinum f Comprend la faiblesse musculaire et la neuropathie périphérique |
Reportez-vous au tableau 1 et au tableau 2 pour le taux d'incidence de l'hypersensibilité pneumonite bronchospasme exacerbation de la dysphonie contre la toux de la maladie sous-jacente d'hémoptysie ototoxicité irritation des voies respiratoires supérieures et troubles neuromusculaires [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Expérience de commercialisation de la poste
Les effets indésirables suivants ont été identifiés à partir de la surveillance post-commercialisation. Étant donné que ces effets indésirables sont signalés volontairement à partir d'une population de tailles inconnues, des estimations précises de la fréquence ne peuvent pas être établies et une relation causale à l'exposition au médicament ne peut pas être établie.
Troubles du système immunitaire: anpersensibilité anaphylaxie [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
Interactions médicamenteuses pour Arikayce
Médicaments avec un potentiel néphrotoxique ou ototoxique neurotoxique
Évitez l'utilisation concomitante d'Arikayce avec des médicaments associés à la néphrotoxicité et à l'ototoxicité de la neurotoxicité.
Acide éthacrynique furosémide urée ou mannitol
Certaines diurétiques peuvent améliorer la toxicité de l'aminoglycoside en modifiant les concentrations d'aminoglycosides dans le sérum et les tissus. Évitez l'utilisation concomitante d'Arikayce avec un furosémide d'acide éthacrynique urée ou mannitol intraveineux.
Avertissements pour Arikayce
Inclus dans le cadre du 'PRÉCAUTIONS' Section
Précautions pour Arikayce
Pneumonite d'hypersensibilité
Pneumonite d'hypersensibilité has been repouted with the use of Arikayce in the clinical trials. Pneumonite d'hypersensibilité (repouted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Arikayce) was repouted at a higher frequency in patients treated with Arikayce plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Arikayce et received treatment with couticosteroids [see Effets indésirables ]. If hypersensitivity pneumonitis occurs discontinue Arikayce et manage the patient as medically appropriate.
Hémoptysie
Hémoptysie has been repouted with the use of Arikayce in the clinical trials. Hémoptysie was repouted at a higher frequency in patients treated with Arikayce plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Effets indésirables ]. If hemoptysis occurs manage the patients as medically appropriate.
Bronchospasme
Bronchospasme has been repouted with the use of Arikayce in the clinical trials. Bronchospasme (repouted as asthma bronchial hyperreactivity bronchospasme dyspnea dyspnea exertional prolonged expiration throat tightness respiration sifflante) was repouted at a higher frequency in patients treated with Arikayce plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Effets indésirables ]. If bronchospasme occurs during the use of Arikayce treat the patients as medically appropriate.
Exacerbation des maladies pulmonaires sous-jacentes
Des exacerbations des maladies pulmonaires sous-jacentes ont été signalées avec l'utilisation d'Arikayce dans les essais cliniques. Exacerbations of underlying pulmonary disease (reported as chronic obstructive pulmonary disease infective exacerbation of chronic obstructive pulmonary disease infective exacerbation of bronchiectasis) have been reported at a higher frequency in patients treated with ARIKAYCE plus a background regimen (15.2%) compared to patients treated with background regimen alone (9.8%) [see Effets indésirables ]. If exacerbations of underlying pulmonary disease occur during the use of Arikayce treat the patients as medically appropriate.
Réactions d'anaphylaxie et d'hypersensibilité
Des réactions d'hypersensibilité graves et potentiellement potentiellement mortelles, y compris l'anaphylaxie, ont été signalées chez des patients prenant Arikayce. Les signes et symptômes comprennent l'apparition aiguë des réactions d'hypersensibilité des tissus cutanées et muqueuses (rupture d'urgence démangeaisons rincer des lèvres gonflées / langue / lobine) des symptômes gastinaux (nauséement de la naufrage de la diarrrhéa pression artérielle basse étourdissements de l'incontinence de la syncope). Avant la thérapie avec Arikayce, évaluez les réactions d'hypersensibilité antérieures aux aminoglycosides. Si l'anaphylaxie ou une réaction d'hypersensibilité se produit, arrêtez Arikayce et instituant des mesures de soutien appropriées.
Élitude
Élitude With Use Of Arikayce
Élitude has been repouted with the use of Arikayce in the clinical trials. Élitude (including deafness vertiges presyncope tinnitus et vertigo) were repouted with a higher frequency in patients treated with Arikayce plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Arikayce plus background regimen vs. 0.9% in the background regimen alone arm) et vertiges (6.3% in Arikayce plus background regimen vs. 2.7% in the background regimen alone arm) [see Effets indésirables ].
Surveillez de près les patients atteints de dysfonction auditive ou vestibulaire connue ou suspectée pendant le traitement avec Arikayce. Si l'ototoxicité se produit, gérez le patient comme médicalement approprié, y compris potentiellement d'arrêter Arikayce.
Risque d'ototoxicité due aux variantes d'ADN mitochondriales
Des cas d'ototoxicité avec des aminoglycosides ont été observés chez les patients atteints de certaines variantes du gène d'ARNr 12S codé par mitochondrie (MT-RNR1), en particulier la variante M.1555A> G> G. L'ototoxicité s'est produite chez certains patients même lorsque leurs taux sériques d'aminoglycoside se situaient dans la plage recommandée. Les variantes d'ADN mitochondrial sont présentes dans moins de 1% de la population américaine générale et la proportion des variantes qui peuvent développer l'ototoxicité ainsi que la gravité de l'ototoxicité est inconnue. En cas d'histoires maternels connues d'ototoxicité dus à l'utilisation d'aminoglycosides ou à une variante d'ADN mitochondriale connue chez le patient, considérez des traitements alternatifs autres que les aminoglycosides à moins que le risque accru de perte auditive permanente ne soit compensée par la gravité de l'infection et le manque de thérapies alternatives sûres et efficaces.
Néphrotoxicité
Néphrotoxicité was observed during the clinical trials of Arikayce in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Effets indésirables ]. Néphrotoxicité has been associated with the aminoglycosides. Close monitouing of patients with known ou suspected renal dysfunction may be needed when prescribing Arikayce.
Blocage neuromusculaire
Les patients atteints de troubles neuromusculaires n'ont pas été inscrits dans des essais cliniques d'Arikayce. Les aminoglycosides peuvent aggraver la faiblesse musculaire en bloquant la libération d'acétylcholine aux jonctions neuromusculaires. Surveillez de près les patients atteints de troubles neuromusculaires connus ou suspects tels que la myasthénie grave. Si le blocage neuromusculaire se produit, il peut être inversé par l'administration de sels de calcium, mais une assistance respiratoire mécanique peut être nécessaire.
Toxicité embryo-fœtale
Les aminoglycosides peuvent causer des dommages fœtaux lorsqu'ils sont administrés à une femme enceinte. Les aminoglycosides, y compris Arikayce, peuvent être associés à une surdité congénitale bilatérale irréversible chez les patients pédiatriques exposés utero . Les patients qui utilisent Arikayce pendant la grossesse ou tombent encein Utiliser dans des populations spécifiques ].
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Guide des médicaments et Patient Instructions fou Use ).
Instructions importantes pour l'administration d'Arikayce
Demandez aux patients de lire les instructions à utiliser avant de commencer Arikayce. Demandez aux patients d'utiliser uniquement le lamira ® Système de nébuliseur pour administrer Arikayce. Conseillez au patient ou au soignant de ne pas utiliser le système de nébuliseur Lamira avec tout autre médicament.
Pneumonite d'hypersensibilité And Bronchospasme (Difficulty Breathing)
Conseillez des patients d'informer leur fournisseur de soins de santé s'ils éprouvent un essoufflement ou une respiration sifflante après l'administration d'Arikayce. Conseiller les patients ayant des antécédents d'asthme des voies respiratoires réactives ou de bronchospasme pour administrer Arikayce après avoir utilisé un bronchodilatateur à action courte [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Hémoptysie Or Toux
Conseiller aux patients d'informer leur professionnel de la santé s'ils crachent du sang ou connaissent une toux épisodique pendant ou après l'administration d'Arikayce, en particulier au cours du premier mois après le début d'Arikayce [voir AVERTISSEMENTS AND PRÉCAUTIONS et Effets indésirables ].
Exacerbations des maladies pulmonaires sous-jacentes
Conseiller aux patients d'informer leur fournisseur de soins de santé s'ils connaissent une aggravation de leur maladie pulmonaire après avoir commencé Arikayce [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Dysphonie Or Difficulty Speaking
Conseillez des patients d'informer leur fournisseur de soins de santé s'ils ont du mal à parler. La difficulté à parler ou à la perte de capacité à parler a été signalée avec Arikayce [voir Effets indésirables ].
Réactions d'anaphylaxie et d'hypersensibilité
Informez les patients et les soignants que des réactions d'hypersensibilité graves et potentiellement potentiellement mortelles qui nécessitent un traitement immédiat pourraient se produire. Conseiller au patient de cesser Arikayce et de consulter un médecin immédiat si des signes ou symptômes d'une réaction d'hypersensibilité se produisent [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Élitude (Ringing In The Ears)
Conseiller aux patients d'informer leur fournisseur de soins de santé s'ils subissent une sonnerie dans les étourdissements des oreilles ou tout changement d'audition parce qu'Arikayce a été associé à la perte auditive [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Conseillez au patient de ne pas utiliser de machines lourdes ou de faire des activités dangereuses tout en inhalant Arikayce à travers le système de nébuliseur Lamira car Arikayce peut provoquer des symptômes tels que des étourdissements ou des symptômes respiratoires.
Néphrotoxicité Or Kidney Damage
Conseiller aux patients d'informer leur fournisseur de soins de santé s'ils ont des problèmes rénaux car des lésions rénales ont été signalées avec des aminoglycosides [voir AVERTISSEMENTS AND PRÉCAUTIONS ]. Blocage neuromusculaire Advise patients to infoum their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Toxicité embryo-fœtale
Conseiller les femmes enceintes que les aminoglycosides, y compris Arikayce AVERTISSEMENTS AND PRÉCAUTIONS et Utiliser dans des populations spécifiques ].
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
Dans une étude de cancérogénicité de l'inhalation à 2 ans, les rats ont été exposés à Arikayce pendant 15-25 50-70 ou 155170 minutes par jour pendant 96-104 semaines. Celles-ci ont fourni des doses inhalées approximatives de 5 15 et 45 mg / kg / jour. Un carcinome épidermoïde a été observé dans les poumons de 2 des 120 rats administrés à la dose la plus élevée testée. Les taux d'AUC sériques maximum d'amikacine chez les rats à l'état d'équilibre étaient d'environ 1,3 2,8 et 7,6 mcg · h / ml à des doses moyennes et élevées respectivement par rapport à 23,5 mcg · h / ml (NULL,0 à 46,5 mcg · hr / ml) mesurées chez l'homme. Les carcinomes épidermoïdes peuvent être le résultat d'une charge pulmonaire élevée des particules d'Arikayce dans le poumon du rat. La pertinence des résultats des tumeurs pulmonaires en ce qui concerne les humains qui reçoivent Arikayce est inconnue.
Aucune preuve de mutagénicité ou de génotoxicité n'a été observée dans une batterie de in vitro et en vain Les études de génotoxicité avec une formulation d'amikacine encapsulée de liposomes similaire à Arikayce ( in vitro test de mutagenèse microbienne in vitro test de mutation de lymphome de souris in vitro étude d'aberration chromosomique et un en vain Étude de micronucléus chez le rat).
Aucune étude de fertilité n'a été menée avec Arikayce. L'administration intrapéritonéale de l'amikacine à des rats mâles et femelles à des doses allant jusqu'à 200 mg / kg / jour avant l'accouplement jusqu'au jour 7 de la gestation n'étaient pas associées à une altération de la fertilité ou des effets indésirables sur le développement embryonnaire précoce.
Utiliser dans des populations spécifiques
Grossesse
Résumé des risques
Il n'y a pas de données sur l'utilisation d'Arikayce chez les femmes enceintes pour évaluer tout risque associé aux médicaments de malformations congénitales majeures ou les résultats défavorables maternels ou fœtaux. Bien que l'absorption systémique de l'amikacine après l'inhalation orale devrait être faible [voir Pharmacologie clinique ] L'exposition systémique aux médicaments antibactériens aminoglycosides, y compris Arikayce AVERTISSEMENTS AND PRÉCAUTIONS ]. Advise pregnant women of the potential risk to a fetus.
Les études de toxicologie reproductive animale n'ont pas été menées avec l'amikacine inhalée. L'administration sous-cutanée d'amikacine en rats enceintes (jusqu'à 100 mg / kg / jour) et les souris (jusqu'à 400 mg / kg / jour) pendant l'organogenèse n'était pas associée à des malformations fœtales. L'ototoxicité n'a pas été correctement évaluée dans la progéniture dans les études animales.
Le risque de fond estimé des principaux malformations congénitales et une fausse couche pour les populations indiquées est inconnue. Toutes les grossesses présentent un risque de fond de perte de maltraitance natale ou d'autres résultats indésirables. Dans la population générale américaine, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est respectivement de 2 à 4% et 15 à 20%.
Données
Données sur les animaux
Aucune étude de toxicologie reproductrice animale n'a été menée avec Arikayce ou l'amikacine non liposomale administrée par inhalation.
L'amikacine a été administrée par voie sous-cutanée à des rats enceintes (jours de gestation 8-14) et aux souris (jours de gestation 7-13) à des doses de 25 100 ou 400 mg / kg pour évaluer la toxicité du développement. Ces doses n'ont pas provoqué de malformations fœtales viscérales ou squelettiques chez la souris. La dose élevée était excessivement toxique maternellement chez le rat (néphrotoxicité et mortalité) empêchant l'évaluation de la progéniture à cette dose. Les malformations fœtales n'ont pas été observées à la dose faible ou moyenne chez le rat. Développement postnatal des rats et des souris exposés à ces doses d'amikacin utero ne différait pas significativement du contrôle.
Élitude was not adequately evaluated in offspring in animal developmental toxicology studies.
Lactation
Résumé des risques
Il n'y a aucune information concernant la présence d'Arikayce dans le lait maternel les effets sur le nourrisson allaité ou les effets sur la production de lait après l'administration d'Arikayce par inhalation. Bien que des données publiées limitées sur d'autres voies d'administration d'amikacin indiquent que l'amikacine est présente dans l'absorption systémique du lait maternel d'Arikayce après l'administration inhalée devrait être faible [voir Pharmacologie clinique ]. The developmental et health benefits of breastfeeding should be considered along with the mother’s clinical need fou Arikayce et any potential adverse effects on the breastfed child from Arikayce ou from the underlying maternal condition.
Usage pédiatrique
La sécurité et l'efficacité de l'Arikayce chez les patients pédiatriques de moins de 18 ans n'ont pas été établies.
Utilisation gériatrique
Dans le NTM, les essais cliniques du nombre total de patients recevant Arikayce 208 (NULL,5%) étaient ≥ 65 ans et 59 (NULL,6%) étaient ≥ 75 ans. Aucune différence globale de sécurité et d'efficacité n'a été observée entre les sujets âgés et les sujets plus jeunes. Parce que les patients âgés sont plus susceptibles d'avoir une diminution de la fonction rénale, il peut être utile de surveiller la fonction rénale [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Trouble hépatique
Arikayce has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Pharmacologie clinique ].
L-Citrulline DL-malates
Trouble rénal
Arikayce has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Arikayce clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitoued in patients with known ou suspected renal impairment including elderly patients with potential age-related decreases in renal function [see AVERTISSEMENTS AND PRÉCAUTIONS Utilisation gériatrique ].
Informations sur la surdose pour Arikayce
Les effets indésirables spécifiquement associés à une surdose d'Arikayce n'ont pas été identifiés. La toxicité aiguë doit être traitée avec un retrait immédiat d'Arikayce et des tests de base de la fonction rénale doivent être entrepris.
L'hémodialyse peut être utile pour éliminer l'amikacin du corps.
Dans tous les cas de surdosage présumé, les médecins doivent contacter le centre de contrôle du poison régional pour des informations sur un traitement efficace. Dans le cas de tout surdosage, la possibilité d'interactions médicamenteuses avec des altérations de la disposition des médicaments doit être prise en compte.
Contre-indications pour Arikayce
Arikayce is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Pharmacologie clinique fou Arikayce
Mécanisme d'action
Arikayce is an antibactérien drug [see Microbiologie ].
Pharmacodynamique
Arikayce exposure-response relationships et the time course of pharmacodynamic response are unknown.
Pharmacocinétique
Concentrations d'expectorations
Suivant une inhalation quotidienne de 590 mg arikayce Mycobacterium avium Les concentrations de dégustations des patients complexes (MAC) à 1 à 4 heures après l'inhalation étaient respectivement de 1720 884 et 1300 mcg / g à 1 3 et 6 mois. Une grande variabilité des concentrations d'amikacine a été observée (CV%> 100%). Après 48 à 72 heures après l'inhalation, les concentrations d'expectorations d'amikacin ont diminué à environ 5% de celles de 1 à 4 heures après l'inhalation.
Concentrations sériques
Après 3 mois d'inhalation une fois par jour de 590 mg arikayce chez les patients MAC, le sérum moyen AUC0-24 était de 23,5 mcg * hr / ml (plage: 8,0 à 46,5 mcg * hr / ml; n = 12) et le sérum moyen Cmax était de 2,8 mcg / ml (plage: 1,0 à 4,4 μg / ml; n = 12). Le CMAX et l'AUC0-24 maximum étaient inférieurs à la CMAX moyenne d'environ 76 mcg / ml et AUC0-24 de 154 mcg * hr / ml observé pour l'administration intraveineuse de sulfate d'amikacine pour l'injection à la posologie approuvée de 15 mg / kg une fois par jour chez des adultes en bonne santé.
Absorption
La biodisponibilité d'Arikayce devrait varier principalement des différences individuelles dans l'efficacité du nébuliseur et la pathologie des voies respiratoires.
Distribution
La liaison protéique de l'amikacine dans le sérum est ≤ 10%.
Élimination
Après l'inhalation d'Arikayce chez les patients Mac, la demi-vie sérique apparente de l'amikacine variait d'environ 5,9 à 19,5 heures.
Métabolisme
L'amikacin ne subit pas de métabolisme appréciable.
Excrétion
L'amikacine systématiquement absorbée après l'administration d'Arikayce est éliminée principalement par filtration glomérulaire. En moyenne, 7,42% (allant de 0,72 à 22,60%; n = 14) de la dose totale d'Arikayce ont été excrétés dans l'urine en tant que médicament inchangé par rapport à 94% après l'administration intraveineuse de sulfate d'amikacine pour l'injection. L'amikacine non absorbée après l'inhalation d'Arikayce est probablement éliminée principalement par le renouvellement cellulaire et l'expectoration.
Études d'interaction médicamenteuse
Aucune étude d'interaction médicament clinique n'a été menée avec Arikayce [voir Interactions médicamenteuses ].
Microbiologie
Mécanisme d'action
L'amikacine est un aminoglycoside bactéricide semi-synthétique polycoque. L'amikacine entre dans la cellule bactérienne en se liant à des composants chargés négativement de la paroi cellulaire bactérienne perturbant l'architecture globale de la paroi cellulaire. Le principal mécanisme d'action est la perturbation et l'inhibition de la synthèse des protéines dans les bactéries cibles en se liant à la sous-unité ribosomale des années 30.
Résistance
Le mécanisme de résistance à l'amikacine chez les mycobactéries a été lié à des mutations dans le gène RRS de l'ARNr 16S. Dans les essais cliniques, les isolats MAC développant un micro amikacin de> 64 mcg / ml après la ligne de base ont été observés dans une proportion plus élevée de sujets traités avec Arikayce [voir Études cliniques ].
Interaction avec d'autres antimicrobiens
Il n'y a pas eu in vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Toxicologie animale et pharmacologie
Pour fournir des informations sur le dosage chronique d'Arikayce à cause d'une autre espèce animale, une étude de toxicologie de l'inhalation de 9 mois a été menée chez les chiens. Les macrophages alvéolaires mousseux associés à la clairance du produit inhalé étaient présents à l'incidence et à la gravité liés à la dose, mais ils n'étaient pas associés à une hyperplasie du tissu d'inflammation ou à la présence de changements prénéoplasiques ou néoplasiques. Les chiens ont été exposés à Arikayce jusqu'à 90 minutes par jour, fournissant des doses d'amikacine inhalées d'environ 5 10 et 30 mg / kg / jour.
Études cliniques
Essai 1 (NCT Mycobacterium avium Maladie pulmonaire complexe (MAC), comme confirmé par au moins 2 résultats de culture d'expectorations. Les patients étaient considérés comme ayant une maladie pulmonaire MAC réfractaire s'ils n'ont pas obtenu de cultures d'expectorations négatives après une durée minimale de 6 mois consécutifs de thérapie par le régime de fond qui était en cours ou qui ne s'est arrêté pas plus de 12 mois avant la visite de dépistage. Les patients ont été randomisés pour Arikayce plus un régime de fond ou un régime de fond seul. Le critère d'évaluation de la substitution pour évaluer l'efficacité était basé sur la réalisation de la culture (3 cultures d'expectorations négatives mensuelles consécutives) au cours du mois 6. La date de conversion a été définie comme la date du premier des 3 cultures mensuelles négatives qui ont dû être atteintes d'ici le mois 4 afin de respecter le point final d'ici le mois 6. randomisation) pendant un total de 12 mois après la première culture négative des expectorations.
Au total, 336 patients ont été randomisés (Arikayce plus régime de fond n = 224; régime de fond seul n = 112) (population ITT) avec un âge moyen de 64,7 ans et il y avait un pourcentage plus élevé de femmes (NULL,3%) que les hommes (NULL,7%) dans l'étude. Au moment de l'inscription des 336 sujets de la population ITT, 302 (NULL,9%) figuraient soit sur un régime basé sur les lignes directrices pour le MAC, soit une thérapie basée sur les directives pour MAC pendant moins de 3 mois, tandis que 34 (NULL,1%) ont été en cas de traitement pendant 3 à 12 mois avant l'inscription. Au dépistage, les patients ont été stratifiés par statut de tabagisme (fumeur actuel ou non) et par le fait que les patients soient sous traitement ou en désaccord pendant au moins 3 mois. La plupart des patients au dépistage n'étaient pas des fumeurs actuels (NULL,3%) et avaient une bronchectasie sous-jacente (NULL,5%). Au départ, 329 patients étaient sur un régime de fond multidrogue qui comprenait un macrolide (NULL,3%), une rifamycine (NULL,3%) ou de l'éthambutol (NULL,4%). Dans l'ensemble, 55,6% des sujets recevaient un régime de fond à triple drogue composé d'un macrolide A Rifamycine et d'éthambutol.
La proportion de patients atteignant la conversion de la culture (3 cultures d'expectorations négatives mensuelles consécutives) au cours du mois 6 était significativement (p <0.0001) greater fou Arikayce plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Arikayce plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 et sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media ou no moue than 2 consecutive positive cultures on liquid media following culture conversion) fou up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Arikayce plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Proportion cumulative de sujets atteignant la conversion de la culture montrée par le premier mois de conversion intention de traiter (ITT) Population
 |
Dans l'essai 1 23/224 (NULL,3%) des patients avaient des isolats MAC qui ont développé un CMI de> 64 mcg / ml tout en recevant un traitement avec Arikayce. Dans le régime de fond seul, le bras 4/112 (NULL,6%) des patients avait des isolats MAC qui ont développé un micro amikacine> 64 mcg / ml.
Des critères d'évaluation supplémentaires pour évaluer les avantages cliniques de Arikayce, par exemple, le changement par rapport à la base de base à la distance de test de marche de six minutes et le questionnaire respiratoire de Saint George n'a pas démontré de bénéfice clinique au cours du mois 6.
Informations sur les patients pour Arikayce
Arikayce
(Ar 'i kase)
Population limitée
(suspension inhalation des liposomes d'amikacine) pour une utilisation inhalation orale
Important: pour l'inhalation orale uniquement.
Quelles sont les informations les plus importantes que je devrais connaître sur Arikayce?
Arikayce can cause serious side effects including:
- Inflammation allergique des poumons: Ces problèmes respiratoires peuvent être des symptômes de l'inflammation allergique des poumons et s'accompagnent souvent:
- fièvre
- respiration sifflante
- touxing
- essoufflement
- respiration rapide
- touxing up of blood (hemoptysis): Touxing up blood is a serious et common side effect of Arikayce.
- Problèmes respiratoires graves: Des problèmes respiratoires graves peuvent être des symptômes de bronchospasme. Le bronchospasme est un effet secondaire sérieux et commun d'Arikayce. Les symptômes de bronchospasme comprennent:
- essoufflement
- respiration difficile ou laborieuse
- respiration sifflante
- touxing ou étanchéité
- aggravation de la maladie pulmonaire obstructive chronique (MPOC): Il s'agit d'un effet secondaire sérieux et commun d'Arikayce.
- Réactions allergiques graves: De graves réactions allergiques qui peuvent conduire à la mort sont arrivées à des gens qui prennent Arikayce. Arrêtez de prendre Arikayce immédiatement et obtenez une aide médicale d'urgence si vous présentez l'un des symptômes suivants d'une réaction allergique grave:
- urticaire
- bruyant
- respiration rapide de la fréquence cardiaque (Stridor)
- démangeaison
- toux
- Se sentir léger
- rougeur ou rougissement de
- nausée
- se sentir évanouir la peau (rinçage)
- Terme des lèvres gonflées ou
- vomissement
- Perte de contrôle des intestins ou de la vessie (incontinence)
- difficulté à respirer ou
- diarrhée
- vertiges respiration sifflante
- essoufflement
- ressentez des crampes dans votre estomac
Tout en utilisant Arikayce, ces effets secondaires peuvent devenir suffisamment graves pour que le traitement dans un hôpital soit nécessaire.
Appelez votre fournisseur de soins de santé ou obtenez une aide médicale immédiatement si Vous avez l'un de ces effets secondaires graves tout en prenant Arikayce. Votre professionnel de la santé peut vous demander d'arrêter d'utiliser Arikayce pendant une courte période ou de cesser complètement d'utiliser Arikayce.
Qu'est-ce que Arikayce?
Arikayce is a prescription medicine used to treat adults with refractouy (difficult to treat) Mycobacterium avium Maladie pulmonaire complexe (MAC) dans le cadre d'un plan de traitement antibactérien combiné (régime).
On ne sait pas si Arikayce est sûr et efficace chez les enfants de moins de 18 ans. Ce produit a été approuvé par la FDA en utilisant la voie de la population limitée.
Cela signifie que la FDA a approuvé ce médicament pour une population de patients limitée et spécifique et que les études sur le médicament n'ont peut-être répondu que des questions ciblées sur sa sécurité et son efficacité.
N'utilisez pas Arikayce si vous:
- sont allergiques à tout aminoglycoside ou à l'un des ingrédients d'Arikayce. Voir Quels sont les ingrédients d'Arikayce? À la fin de cette brochure pour une liste complète d'ingrédients à Arikayce.
Avant d'utiliser Arikayce, dites à votre fournisseur de soins de santé de toutes vos conditions médicales, y compris si vous:
- Avoir l'asthme de l'asthme des maladies pulmonaires obstructives (MPOC) essoufflement ou respiration sifflante (bronchospasme).
- On vous a dit que vous avez une mauvaise fonction pulmonaire.
- ont ou ont eu des problèmes d'audition (y compris des bruits dans vos oreilles tels que la sonnerie ou le sifflement) ou votre mère a eu des problèmes d'audition après avoir pris un aminoglycoside.
- On vous a dit que vous avez certaines variantes de gènes (un changement dans le gène) lié aux anomalies entendantes héritées de votre mère.
- avoir des étourdissements ou un sens de la pièce.
- avoir des problèmes rénaux.
- ont une maladie neuromusculaire comme la myasthénie grave.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- allaitent ou prévoient d'allaiter. On ne sait pas si le médicament à Arikayce passe dans votre lait maternel et si cela peut nuire à votre bébé. Parlez à votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé pendant le traitement avec Arikayce.
Parlez à votre fournisseur de soins de santé de tous les médicaments que vous prenez, y compris médicaments sur ordonnance et médicaments sur le comptoir vitamines et suppléments à base de plantes.
Comment dois-je utiliser Arikayce?
- Lisez les instructions étape par étape pour utiliser Arikayce à la fin du guide de médicaments et les instructions complètes pour une utilisation fournies dans votre kit. Les instructions du fabricant pour une utilisation fournissent des informations complètes sur la façon de mettre en place (assembler) Préparer Utiliser Nettoyer et désinfecter votre lamira ® Système de nébuliseur.
- Ne pas Utilisez Arikayce à moins que vous ne compreniez les instructions fournies. Si vous avez des questions, parlez à votre fournisseur de soins de santé ou appelez le soutien Arikares au 1-833-Arikare (1-833-274-5273).
- Utilisez Arikayce exactement comme votre fournisseur de soins de santé vous dit de l'utiliser. N'utilisez pas Arikayce plus souvent que prévu pour vous.
- Utilisez uniquement Arikayce avec le système de nébuliseur Lamira.
- Inspirez chaque dose quotidienne d'Arikayce 1 fois chaque jour à travers le combiné de nébuliseur Lamira. N'utilisez pas plus d'un flacon d'Arikayce par jour.
- Ne pas use Arikayce after the expiration date on the vial. If you fouget to take your daily dose of Arikayce take your next dose at your usual time the next day.
- Ne pas Doublez la dose pour compenser la dose manquée.
- Ne pas Arrêtez d'utiliser Arikayce ou d'autres médicaments pour traiter votre maladie pulmonaire MAC, sauf si votre fournisseur de soins de santé.
- Si vous utilisez trop Arikayce, appelez votre fournisseur de soins de santé ou allez immédiatement aux urgences les plus proches.
Quels sont les effets secondaires possibles d'Arikayce?
Arikayce may cause serious side effects including:
- Vous voyez quelles sont les informations les plus importantes que je devrais connaître sur Arikayce?
- perte auditive ou sonne dans les oreilles (ototoxicité) . L'ototoxicité est un effet secondaire grave et commun d'Arikayce. Dites immédiatement à votre professionnel de la santé si vous avez une perte auditive ou si vous entendez des bruits dans vos oreilles tels que la sonnerie ou le sifflement. Dites à votre fournisseur de soins de santé si vous commencez à avoir des problèmes d'équilibre ou de vertiges (vertige).
- aggraver les problèmes rénaux (néphrotoxicité). Arikayce is in a class of medicines which may cause wousening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are wouking during your treatment with Arikayce.
- aggraver la faiblesse musculaire (blocage neuromusculaire). Arikayce is in a class of medicines which can cause muscle faiblesse to get wouse in people who already have problems with muscle faiblesse (myasthenia gravis).
Les effets secondaires les plus courants d'Arikayce comprennent:
- changements dans votre voix et
- mal de gorge
- Enrouement de la douleur musculaire (dysphonie)
- diarrhée
- nausée
- fatigue (fatigue)
- fièvre
- vomissement
- mal de tête
- diminution du poids
- augmentation des expectorations
- éruption cutanée
- malaise
- toux during ou after a dose of Arikayce especially in the first month after starting treatment.
Ce ne sont pas tous les effets secondaires possibles d'Arikayce.
Les pilules aux canneberges sont-elles bonnes pour les uti
Appelez votre médecin ou pharmacien pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler des effets secondaires à la FDA au 1-800-FDA-1088
Comment dois-je stocker Arikayce?
- Stockez les flacons Arikayce réfrigérés entre 36 ° F à 46 ° F (2 ° C à 8 ° C) jusqu'à la date d'expiration du flacon. Ne congelez pas.
- Une fois qu'Arikayce a été stocké au réfrigérateur, tout médicament inutilisé doit être jeté (éliminé) après la date d'expiration sur le flacon.
- Stockez les flacons Arikayce à température ambiante entre 68 ° F à 77 ° F (20 ° C à 25 ° C) pendant jusqu'à 4 semaines
- Une fois qu'Arikayce a été stocké à température ambiante, tout médicament inutilisé doit être jeté (éliminé) au bout de 4 semaines.
- Utilisez immédiatement un flacon Arikayce ouvert.
- Jetez immédiatement le flacon Arikayce après utilisation.
Gardez Arikayce et tous les médicaments hors de portée des enfants.
Informations générales sur l'utilisation sûre et efficace d'Arikayce
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide de médicaments. N'utilisez pas Arikayce pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas Arikayce à d'autres personnes même s'ils présentent les mêmes symptômes que vous. Cela peut leur faire du mal. Vous pouvez demander à votre pharmacien ou fournisseur de soins de santé pour des informations sur Arikayce qui sont écrits pour les professionnels de la santé.
Quels sont les ingrédients d'Arikayce?
Ingrédient actif: sulfate d'amikacine
Ingrédients inactifs: Dipalmitoylphosphatidylcholine (DPPC) cholestérol chlorure de chlorure de sodium hydroxyde (pour réglage du pH) et de l'eau pour l'injection
Ce guide de médicaments a été approuvé par la Food and Drug Administration des États-Unis.
Instructions pour une utilisation
Arikayce ®
Population limitée
(suspension inhalation des liposomes d'amikacine) pour une utilisation inhalation orale
Lamira ®
Système de nébuliseur
Avant d'utiliser votre système de nébuliseur Lamira, assurez-vous de lire et de comprendre les informations détaillées dans les instructions complètes pour une utilisation fournies avec le système de nébuliseur Lamira. Cela fournira des informations plus complètes sur la façon de mettre en place (assembler) Préparer à utiliser et désinfecter votre système de nébuliseur Lamira. Si vous ne comprenez aucune partie des instructions, contactez Arikares Support au 1-833-Arikare (1-833-274-5273) Avant d'utiliser le système de nébuliseur Lamira.
Rassemblez votre médicament Arikayce. Le kit Arikayce de 28 jours contient:
- 1 Guide de démarrage rapide Arikayce
- 1 Instructions pour une utilisation
- 1 insert d'information de prescription complet
- 1 combiné de nébulizage lamira
- 4 têtes d'aérosol Lamira (1 dans chaque boîte hebdomadaire)
- 28 flacons (1 flacon par jour) d'Arikayce (7 dans chaque boîte hebdomadaire)
Vérifiez que vous disposez de toutes les pièces nécessaires pour votre système de nébuliseur Lamira:
- Casse de transport
- Cordon de connexion
- Contrôleur
- Alimentation A / C
- Batteries AA
 |
COMBAT DE NEBULIZE DE LAMIRA de rechange:
- Cap
- Réservoir de médicaments
- Vanne bleue
- Chambre d'aérosol
- Embouchure
- Tête d'aérosol de rechange
 |
Vous aurez également besoin des fournitures suivantes qui ne viennent pas dans votre kit Arikayce de 28 jours qui vous aidera à prendre soin de votre système de nébuliseur Lamira:
- Savon liquide transparent pour nettoyer le combiné et la tête d'aérosol
- Eau distillée pour désinfecter le combiné et la tête d'aérosol
Choisissez votre alimentation et préparez-la.
un. 4 piles AA
 |
né Alimentation A / C
- Branchez l'alimentation A / C dans le contrôleur.
- Branchez l'alimentation A / C dans la prise murale.
Ne pas insert the A/C Power into thefront of the Contrôleur.
 |
Nettoyage et désinfection
Avant d'utiliser d'abord, rincer et désinfecter votre combiné et votre tête d'aérosol. Aller de l'avant Rinse Nettoyer et désinfecter le combiné, y compris la tête d'aérosol après chaque utilisation.
Lorsque vous recevez votre combiné et la tête d'aérosol, ils ne seront pas stériles. Le nettoyage et la désinfection de votre combiné et de votre tête d'aérosol sont importants pour réduire le risque de maladie et de contamination par l'infection.
- Nettoyage de la tête du combiné et de l'aérosol: Avant d'utiliser d'abord Rinse et nettoyez la tête du combiné et de l'aérosol. Aller de l'avant Rince et nettoyer le combiné, y compris la tête d'aérosol juste après chaque utilisation.
Utilisez uniquement des Papertowels ou des lingettes sèches. Ne pas use towels ou wipes that have any chemicals added to them such as alcohol lotion ou baby wipes.
Faites attention à ne pas nuire aux pièces. N'épuisez pas la tête d'aérosol.
Jetez des serviettes en papier en éliminant des déchets avec des déchets solides.

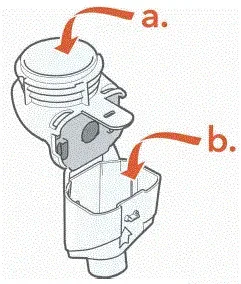
- Démonter (démonter) le combiné pour le nettoyage
- Essuyez doucement toutes les gouttes de la médecine du réservoir de médicaments (A) Chambre aérosol (B) et embout buccal (C) avant de rincer pour réduire les antibiotiques ajoutés aux systèmes d'eau.
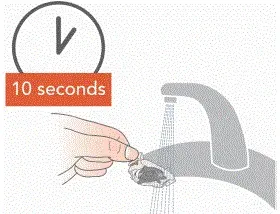
- Rincer chacune des pièces sous l'eau chaude du robinet pour la course pour 10 secondes. Rincer la tête d'aérosol pour 10 secondes de chaque côté.
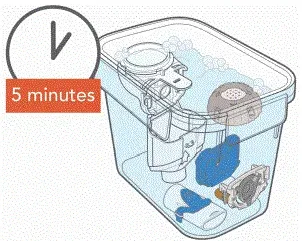
- Nettoyez toutes les pièces du combiné en ajoutant quelques gouttes de savon à vaisselle liquide transparent et de l'eau chaude du robinet à une baignoire ou à un bol propre. Couvrir les pièces du combiné dans l'eau chaude savonneuse et tremper pour 5 minutes Les secouer périodiquement. Ensuite, rincez-les soigneusement sous l'eau chaude du robinet.
- Désinfecter la tête du combiné et de l'aérosol avant d'abord Utiliser Rappel: Désinfectez la tête du combiné et de l'aérosol avant la première utilisation.

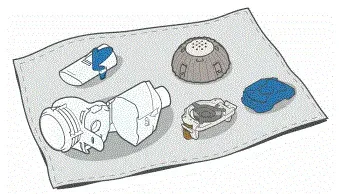
- Assurez-vous que votre combiné et votre tête d'aérosol sont propres avant de désinfecter.
- Assurez-vous que le pot a suffisamment d'eau distillée pour couvrir complètement toutes les pièces du combiné, y compris la tête d'aérosol.
- Chauffer l'eau à ébullition dans un pot propre.
- Placez les pièces du combiné, y compris la tête d'aérosol dans l'eau bouillante.
- Faire bouillir pour un plein 5 minutes . Remarque: il peut être utile d'utiliser une minuterie.
- Sécher à l'air sur un sans peluche serviette. Lorsqu'il est entièrement sec, enveloppez les pièces dans une serviette sans peluche pour le stockage. Vous pouvez les remettre ensemble juste avant de prendre votre prochain traitement.
Assembler votre combiné
Étape 1: Lavez-vous les mains avec savon et eau et dry them well.
 |
Étape 2: Insérez la valve bleue.
Ouvrez le combiné en tirant doucement sur l'onglet du réservoir de médicaments.
Insérez la vanne bleue de sorte qu'elle repose sur le dessus de la chambre aérosol avec les 2 rabats de soupape vers le bas (volets de soupape non pliés).
 |
Aer Osol C Hamber Val VE VALVE VALVE VALVE BLUE
Étape 3: Insérez la tête d'aérosol.
Saisissez la tête d'aérosol par les 2 languettes en plastique flexibles de chaque côté. Assurez-vous que le texte Lamira ® est face à vous et se trouve au sommet de la tête d'aérosol.
Pressez les 2 languettes en plastique flexibles ensemble tout en insérant la tête d'aérosol dans le réservoir de médicaments.
Fermez le combiné lorsque vous avez terminé (pas de lacunes le long du bord de la vanne bleue).
 |
Ne pas touch the silver part of theAerosol Head at any time.
Une fois que la tête d'aérosol a été utilisée 7 fois à lancer (disposer) et remplacer par un nouveau processus de nettoyage. Le combiné Lamira doit être utilisé pendant 28 jours.
 |
Étape 4: Fixez le combiné Toyour de l'embout buccal avec le volet bleu vers le haut.
 |
Étape 5: Fin fixez enfin le combiné au contrôleur.
un. Fixez le cordon de connexion au combiné. a1. Alignez le bas du connecteur avec le bas du combiné.
a2. Poussez vers le haut contre le combiné jusqu'à ce que vous entendiez les pièces se claquer. né Connectez le cordon de connexion au contrôleur.
 |
Prendre Arikayce
Votre Arikayce doit être à température ambiante avant utilisation pour vous assurer que votre système de nébuliseur Lamira fonctionne correctement. Ne pas use other medicines in your Hetset.
Amenez Arikayce à température ambiante en le retirant du réfrigérateur au moins 45 minutes avant utilisation. Ne pas use if your Arikayce has been frozen.
Étape 1: Préparez votre Arikayce.
- Placer le combiné sur une surface stable plate propre.
- Secouez le flacon Arikayce pendant un minimum de 10 à 15 secondes Et jusqu'à ce que le médicament se ressemble tout au long et bien mélangé.
 |
Comment ouvrir le flacon Arikayce
 |
 |
 |
 |
- Soulevez le capuchon d'orange du flacon.
- Saisir l'anneau métallique Au-dessus du flacon et tirez-le doucement jusqu'à ce que 1 côté se casse du flacon mais ne retire pas complètement l'onglet.
- Tirez la bande de métal de autour du haut du flacon dans un mouvement circulaire jusqu'à ce qu'il se détache complètement.
- Supprimer soigneusement le bouchon en caoutchouc.
un. Ouvrez le flacon et versez l'Arikayce dans le réservoir de médicaments.
né Fixez le capuchon de médicaments.
 |
Étape 2: Asseyez-vous dans une position verticale détendue.
- Appuyez et maintenez-le sur le bouton ON / OFF pendant quelques secondes pour allumer la lamira.
- La brume commencera à couler.
 |
Étape 3: Insérez l'embout buccal (mais ne couvrez pas le rabat bleu) et prenez des respirations profondes lentes.
- Ensuite, respirez normalement dans et hors de l'embout buccal jusqu'à ce que votre traitement soit terminé.
- Le traitement doit prendre environ 14 minutes mais peut prendre jusqu'à 20 minutes.
Assurez-vous de maintenir le niveau du combiné tout au long du traitement.
 |
Étape 4: Vérifiez que votre traitement est terminé.
- Le LaMira bip 2 fois.
- Une coche apparaîtra brièvement à l'écran.
- Le contrôleur s'arrête automatiquement.
- Retirez le capuchon de médicaments et Vérifiez le réservoir de médicaments pour vous assurer qu'il ne reste plus quelques gouttes d'Arikayce. Si Arikayce reste remplacer le capuchon de médicaments, appuyez sur le bouton ON / OFF et complétez votre dose.
 |
Pour tous les problèmes que vous pourriez avoir avec votre système de nébuliseur Lamira, voir la section J - Les questions et la section K - la section K - le transport des instructions complètes pour une utilisation accompagnées de votre médicament.
Nettoyage de votre combiné Lamira et de votre tête d'aérosol après utilisation
- Rincez immédiatement le combiné de nettoyage et de désinfecter après chaque utilisation pour réduire la maladie et la contamination par les infections.
- Désinfectez la tête du combiné et de l'aérosol après chaque utilisation.
- Voir le nettoyage et la désinfection au début des instructions pour une utilisation sur la façon de nettoyer et de désinfecter correctement votre combiné et votre tête d'aérosol.
Ces instructions pour une utilisation ont été approuvées par la Food and Drug Administration des États-Unis.






