Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Anticonvulsivants, autresFintepla
Résumé
Qu'est-ce que Fintepla?
Fintepla (fenfluramine) est un anticonvulsante Utilisé pour traiter les convulsions associées au syndrome de Dravet chez les patients de 2 ans et plus.
Quels sont les effets secondaires de Fintepla?
Fintepla
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- Changements d'humeur ou de comportement
- anxiété
- crises de panique
- Difficulté à dormir
- impulsivité
- agitation
- hostilité
- agressions
- agitation
- hyperactivité (mentalement ou physiquement)
- dépression accrue
- Pensées d'automutilation
- douleur thoracique
- battements cardiaques
- flotter dans votre poitrine
- essoufflement
- peau ou lèvres de couleur bleue
- gonflement dans les jambes inférieures
- fatigue inhabituelle
- faiblesse
- étourdissement
- perte d'appétit
- perte de poids
- aggraver les convulsions
- vision floue
- vision du tunnel
- Douleurs oculaires ou rougeur
- voir des halos autour des lumières
- nausée
- vomissement
- maux de tête sévères
- vision floue
- battant dans votre cou ou vos oreilles
- saignement de nez
- fièvre
- transpiration
- hallucinations
- tremblement
- fréquence cardiaque rapide
- raideur musculaire
- contraction
- Croissance ralentie (chez les enfants)
- perte de coordination et
- diarrhée
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires de Fintepla comprennent:
- diminution de l'appétit
- somnolence
- sédation
- léthargie
- diarrhée
- constipation
- échocardiogramme anormal
- fatigue
- Se sentir mal (malaise)
- faiblesse
- Problèmes de coordination musculaire
- trouble de l'équilibre
- perturbation de la marche
- augmentation de la tension artérielle
- baver / excès de salivation
- fièvre
- infection des voies respiratoires supérieures
- vomissement
- perte de poids
- tombe et
- statut epilepticus
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; et des étourdissements soudains étourdisseurs ou s'évanouissant;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Fintepla
La dose initiale de démarrage et de maintenance de Fintepla est de 0,1 mg / kg deux fois par jour, ce qui peut être augmenté chaque semaine en fonction de l'efficacité et de la tolérabilité.
Fintepla chez les enfants
La sécurité et l'efficacité de la Fintepla pour le traitement des crises associées au syndrome de Dravet ont été établies chez les patients de 2 ans et plus. La sécurité et l'efficacité de la Fintepla chez les patients de moins de 2 ans n'ont pas été établies.
Les dystonies et autres symptômes extrapyramidaux associés au métoclopramide sont plus fréquents chez les patients pédiatriques que chez les adultes. De plus, les nouveau-nés ont réduit les niveaux de NADH-cytochrome b5 réductase, ce qui les rend plus sensibles à la méthémoglobinémie une réaction indésirable possible de l'utilisation du métoclopramide chez les nouveau-nés.
Quelles substances ou suppléments de médicaments interagissent avec Fintepla?
Fintepla peut interagir avec d'autres médicaments tels que:
- rifampin
- Stiripentol plus Clobazam
- cyproheptadine
- 5-HT1A 5- HT1D 5-HT2A ou 5-HT2C sérotonine antagonistes des récepteurs et
- Médicaments en vente libre ou suppléments à base de plantes qui augmentent la sérotonine tels que les inhibiteurs sélectifs du recapture de la sérotonine (ISRS) inhibiteurs du recapture de la sérotonine - norepinéphrine (SNRIS) (SNRIS) antidépresseurs tricycliques inhibiteurs de monoamine oxydase
Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Fintepla pendant la grossesse et l'allaitement
Dites à votre médecin si vous êtes enceinte ou prévoyez de devenir enceinte avant d'utiliser Fintepla; On ne sait pas comment cela affecterait un fœtus. Il existe un registre d'exposition à la grossesse qui surveille les résultats de la grossesse chez les femmes exposées à des médicaments antiépileptiques (AED) tels que la Fintepla pendant la grossesse. On ne sait pas si la fintepla passe dans le lait maternel. Consultez votre médecin avant l'allaitement.
Informations Complémentaires
Notre centre de médicaments sur les effets secondaires CIV Fintepla (fenfluramine) CIV offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Ce n'est pas une liste complète des effets secondaires et d'autres peuvent survenir. Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Maladie cardiaque valvulaire et hypertension artérielle pulmonaire
Il existe une association entre les médicaments sérotoninergiques avec une activité agoniste des récepteurs 5-HT2B, notamment la fenfluramine (l'ingrédient actif dans la fintepla) et les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire [voir [voir AVERTISSEMENTS AND PRECAUTIONS ].
Des évaluations de l'échocardiogramme sont nécessaires avant pendant et après le traitement avec Fintepla. Les avantages par rapport aux risques d'initier ou de continuer la Fintepla doivent être considérés sur la base des résultats de l'échocardiogramme [voir Posologie et administration et AVERTISSEMENTS AND PRECAUTIONS ].
En raison des risques des maladies cardiaques valvulaires et de l'hypertension artérielle pulmonaire, la Fintepla est disponible unique AVERTISSEMENTS AND PRECAUTIONS ].
Description de Fintepla
La solution orale de fintepla contient 2,2 mg / ml de fenfluramine équivalente à 2,5 mg / ml du sel de chlorhydrate.
Le chlorhydrate de fenfluramine ingrédient actif est désigné chimiquement en tant que n-éthyl-α-méthyl-3- (trifluorométhyl) du chlorhydrate de phénéthylamine.
La formule structurelle est:
| |
Le chlorhydrate de fenfluramine est un solide cristallin blanc à blanc cassé. Le PKA de la fenfluramine est de 10,2.
Fintepla est une solution incolore claire pH 5.
Fintepla contient les ingrédients inactifs suivants: Flavour des cerises Citric Acid Ethylparaben Hydroxyethylcellulose Methylparaben Potassium Citrate Sucralose and Water.
Fintepla ne contient aucun ingrédient en grain contenant du gluten (orge ou seigle).
Utilisations pour Fintepla
Fintepla est indiquée pour le traitement des crises associées au syndrome de Dravet (DS) et au syndrome de Lennox-Gastaut (LGS) chez les patients de 2 ans et plus.
Dosage pour Fintepla
Évaluations avant de lancer Fintepla
Avant de commencer le traitement par Fintepla, obtenez une évaluation d'échocardiogramme pour évaluer les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire [voir Évaluations pendant et après l'administration de Fintepla et AVERTISSEMENTS AND PRECAUTIONS ].
Dossing Information
Fintepla doit être administrée par voie orale et peut être prise avec ou sans nourriture.
Syndrome de Dravet
- La dose initiale de démarrage et de maintenance pour les patients atteints du syndrome de Dravet est de 0,1 mg / kg deux fois par jour, ce qui peut être augmenté chaque semaine en fonction de l'efficacité et de la tolérabilité. Le tableau 1 fournit le calendrier de titrage recommandé si nécessaire.
- Les patients atteints du syndrome de Dravet ne sont pas sur le stimipentol concomitant qui tolèrent la Fintepla à 0,1 mg / kg deux fois par jour et nécessitent une réduction supplémentaire des crises peuvent bénéficier d'une augmentation de dosage jusqu'à un dosage de maintenance maximal recommandé de 0,35 mg / kg deux fois par jour (dosage quotidien maximum de 26 mg).
- Les patients du syndrome de Dravet prenant du stimipentol et du clobazam concomitants qui tolèrent la fintepla à 0,1 mg / kg deux fois par jour et nécessitent une réduction supplémentaire des crises peuvent bénéficier d'une augmentation de dosage jusqu'à un dosage d'entretien maximal recommandé de 0,2 mg / kg deux fois par jour (dosage quotidien maximum de 17 mg) [voir Interactions médicamenteuses ].
Syndrome de Lennox-Gastaut
- La dose de départ initiale pour les patients atteints du syndrome de Lennox-Gastaut est de 0,1 mg / kg deux fois par jour, ce qui devrait être augmenté chaque semaine en fonction de la tolérabilité. Le tableau 1 fournit le calendrier de titrage recommandé.
- Les patients atteints du syndrome de Lennox-Gastaut qui ne sont pas sur le soripentol concomitant qui tolèrent la Fintepla doivent être titrés à la dose d'entretien recommandée de 0,35 mg / kg deux fois par jour (posologie quotidienne maximale de 26 mg).
- Les patients atteints du syndrome de Lennox-Gastaut prenant un stimipentol concomitant plus le clobazam qui tolèrent la Fintepla doit être titré à la dose d'entretien recommandée de 0,2 mg / kg deux fois par jour (posologie quotidienne maximale de 17 mg) [voir Interactions médicamenteuses ].
Tableau 1: Horaire de titrage recommandé par Fintepla *
| Sans stiripentol concomitant * | Avec du stimipentol concomitant plus du clobazam | |||
| Dose basée sur le poids | Dosage quotidien total maximum ± | Dose basée sur le poids | Dose maximale ± total quotidien | |
| Dose initiale | 0,1 mg / kg deux fois par jour | 26 mg | 0,1 mg / kg deux fois par jour | 17 mg |
| Jour 7 | 0,2 mg / kg deux fois par jour | 26 mg | 0,15 mg / kg deux fois par jour | 17 mg |
| Jour 14 ** | 0,35 mg / kg deux fois par jour | 26 mg | 0,2 mg / kg deux fois par jour | 17 mg |
| * Pour les patients qui ne sont pas sur le stimipentol concomitant chez qui un titrage plus rapide est justifié, la dose peut être augmentée tous les 4 jours. Pour les patients atteints du syndrome de Dravet, le dosage peut être augmenté en fonction de la réponse clinique à la posologie maximale recommandée au besoin. ** Pour les patients atteints du syndrome du syndrome de Lennox-Gastaut, doit être augmenté comme toléré à la dose d'entretien recommandée (c'est-à-dire le jour 14). ± Pour une posologie maximale avec une utilisation concomitante de forts inhibiteurs du CYP1A2 ou du CYP2D6 chez les patients souffrant d'une déficience rénale sévère ou chez les patients souffrant de troubles hépatiques voir Modifications posologiques pour les patients avec une utilisation concomitante de fortes modifications de posologie des inhibiteurs du CYP1A2 ou du CYP2D6 (DS et LGS) pour les patients atteints d'une déficience rénale sévère (DS et LGS) Modifications pour les patients présentant une légère altération hépatique modérée et sévère (DS et LGS) |
Modifications posologiques pour les patients avec une utilisation concomitante de forts inhibiteurs du CYP1A2 ou du CYP2D6 (DS et LGS)
Pour les patients présentant une utilisation concomitante de Fintepla avec un fort inhibiteur du CYP1A2 ou du CYP2D6, une dose quotidienne totale maximale de 20 mg sans stimipentol concomitante et 17 mg avec du soripentol concomitant plus du clobazam est recommandé [voir Interactions médicamenteuses ].
Modifications posologiques pour les patients atteints d'une insuffisance rénale sévère (DS et LGS)
Pour les patients atteints d'une insuffisance rénale sévère (taux de filtration glomérulaire estimé (EGFR) 15 à 29 ml / min / 1,73 m 2 ) Une dose quotidienne totale maximale de 20 mg sans stiripentol concomitante et 17 mg avec du stialintol concomitant plus du clobazam est recommandé [voir Utiliser dans des populations spécifiques ].
Modifications posologiques pour les patients atteints de troubles hépatiques modérés et graves (DS et LGS)
Voir le tableau 2 pour les ajustements et les recommandations de dosage pour les patients souffrant de troubles hépatiques [voir Utiliser dans des populations spécifiques ].
Tableau 2: Modifications et recommandations du dosage Fintepla pour les patients atteints de déficience avec les patients
| Classification des troubles hépatiques | Sans stiripentol concomitant * | Avec du stimipentol concomitant plus du clobazam |
| Dosage quotidien total maximum | Dosage quotidien total maximum | |
| Bénin (Child-Pugh a) | 20 mg | 13 mg * |
| Modéré (Child-Pugh b) | 20 mg | Utiliser non recommandé |
| Grave (Child-Pugh c) | 17 mg | Utiliser non recommandé |
| * Titre comme recommandé [voir Dossing Information |
Évaluations pendant et après l'administration de Fintepla
Pour évaluer les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire, obtenir une évaluation d'échocardiogramme tous les 6 mois pendant le traitement avec Fintepla et 3 à 6 mois après la dose finale de Fintepla [voir AVERTISSEMENTS AND PRECAUTIONS ].
Instructions d'administration
Un dispositif de mesure calibré (une seringue orale de 3 ml ou 6 ml) sera fourni par la pharmacie et sera recommandé pour mesurer et administrer la dose prescrite avec précision [voir Comment fourni ]. A household teaspoon or tablespoon is not an adequate measuring device et should not be used.
Jetez toute solution orale de fintepla inutilisée restant après 3 mois d'ouverture de la bouteille ou de la défausse après la date de la bouteille la plus tôt.
Fintepla est compatible avec les tubes d'alimentation gastriques et nasogastriques disponibles dans le commerce.
Arrêt de la Fintepla
Lors de l'arrêt de la Fintepla, la dose devrait être diminuée progressivement. Comme pour tous les médicaments antiépileptiques, l'arrêt abrupte doit être évité lorsque cela est possible pour minimiser le risque d'augmentation de la fréquence des crises et du statut épileptique [voir AVERTISSEMENTS AND PRECAUTIONS ].
Comment fourni
Formes et forces posologiques
Solution orale : 2,2 mg / ml de fenfluramine comme un liquide à la cerise incolore transparent.
Fintepla La solution orale est un liquide aromatisé en cerise incolore transparent contenant 2,2 mg / ml de fenfluramine et est fourni dans une bouteille en plastique blanche avec une fermeture résistante aux enfants comme suit:
- Carton contenant une bouteille de 360 ml ( NDC 43376-322-36)
- Carton contenant une bouteille de 30 ml ( NDC 43376-322-30)
Avant la distribution, le pharmacien inséra un adaptateur de bouteille de presse dans la bouteille de distribution. La pharmacie fournira 3 ml ou 6 ml de seringues buccales calibrées.
Stockage et manipulation
Stocker la fintepla à température ambiante entre 20 ° C et 25 ° C (68 ° F à 77 ° F); Les excursions sont autorisées entre 15 ° C et 30 ° C (59 ° F à 86 ° F) [voir la température ambiante contrôlée par l'USP].
Ne réfrigérez ni ne congelez. Conservez la bouteille et la seringue ensemble.
Jetez toute portion inutilisée 3 mois après l'ouverture de la bouteille ou la défausse après la date de la bouteille la plus tôt possible.
Pourcentage de réduction par rapport à la fréquence de crise de base de la ligne de base
Proportion de patients (%)
Fabriqué pour: UCB Inc. Smyrna GA 30080. Révisé: avril 2025.
Effets secondaires for Fintepla
Les effets indésirables cliniquement significatifs suivants sont décrits ailleurs dans l'étiquetage:
- Maladie cardiaque valvulaire et hypertension artérielle pulmonaire [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Diminution de l'appétit et diminution du poids [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Somnolence Sédation et léthargie [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Comportement suicidaire et idéation [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Retrait des médicaments antiépileptiques [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Syndrome de Seroton [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Augmentation de la pression artérielle [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Glaucome [voir AVERTISSEMENTS AND PRECAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions de réaction indésirables très variables observées dans les essais cliniques d'un médicament ne peuvent pas être directement comparées aux taux dans les essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans la pratique.
Dans les essais contrôlés et incontrôlés chez les patients atteints du syndrome de Dravet (DS), 341 patients ont été traités par Fintepla, dont 312 patients traités pendant plus de 6 mois 284 patients traités pendant plus d'un an et 138 patients traités pendant plus de 2 ans.
Dans des essais contrôlés et incontrôlés chez les patients atteints du syndrome de Lennox-Gastaut (LGS) 262 patients ont été traités par Fintepla, dont 219 patients traités pendant plus de 6 mois 172 patients traités pendant plus d'un an et 127 patients traités pendant plus de 2 ans.
Syndrome de Dravet
Dans les essais contrôlés par un placebo, des patients atteints de DS prenant un niveau de soins concomitants AEDS 122 patients ont été traités par Fintepla et 84 patients ont reçu un placebo [voir Études cliniques ]. The duration of treatment in these trials was 16 weeks (Étude 1) or 17 weeks (Étude 2).
Dans l'étude 1 et l'étude 2, l'âge moyen était de 9 ans (intervalle de 2 à 19 ans) et environ 46% des patients étaient des femmes et 74% étaient blancs. Tous les patients recevaient au moins un autre AED.
Dans l'étude 1 et l'étude 2, les taux d'arrêt en raison de toute réaction indésirable étaient de 13% 0% et 7% pour les patients traités avec une fintepla 0,7 mg / kg / jour 0,2 mg / kg / jour et 0,4 mg / kg / jour en combinaison avec le soripintol respectivement par rapport à 6% pour les patients sur placebo. La réaction indésirable la plus fréquente conduisant à l'arrêt chez les patients traités avec une dose de fintepla était la somnolence (3%).
Les effets indésirables les plus courants survenus chez les patients traités par Fintepla (incidence au moins 10% et supérieur au placebo) ont diminué l'appétit; Léthargie de la sédation de la somnolence; diarrhée; constipation; échocardiogramme anormal; malaise de la fatigue Asthénie; trouble de l'équilibre de l'ataxie perturbation de la marche; La pression artérielle a augmenté; Hypersécrétion salivaire bave; pyrexie; infection des voies respiratoires supérieures; vomissement; diminution du poids; automne; Statut epilepticus.
Le tableau 4 répertorie les effets indésirables qui ont été signalés chez 5% ou plus des patients traités par Fintepla et à un rythme supérieur à ceux du placebo pendant les phases de titrage et d'entretien de l'étude 1 et 2.
Tableau 4: Réactions indésirables chez 5% ou plus des patients traités par Fintepla et Greater que le placebo dans les essais contrôlés par placebo pour le syndrome de Dravet (étude 1 et 2)
| Réaction indésirable | Fintepla Dose Group | Groupe placebo combiné (2) | ||
| Étude 1 | Étude 2 | |||
| 0,2 mg / kg / jour | 0,7 mg / kg / jour | 0,4 mg / kg / jour (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Diminution de l'appétit | 23 | 38 | 49 | 8 |
| Somnolence sédation léthargie | 26 | 25 | 23 | 11 |
| Échocardiogramme anormal (3) | 18 | 23 | 9 | 6 |
| Diarrhée | 31 | 15 | 23 | 6 |
| Constipation | 3 | 10 | 7 | 0 |
| Fatigue malaise asthenia | 15 | 10 | 30 | 5 |
| Trouble de l'équilibre de l'ataxie perturbation de la marche | 10 | 10 | 7 | 1 |
| Comportement anormal | 0 | 8 | 9 | 0 |
| La pression artérielle a augmenté | 13 | 8 | 0 | 5 |
| Hypersécrétion salivaire bave | 13 | 8 | 2 | 0 |
| Hypotonie | 0 | 8 | 0 | 0 |
| Éruption cutanée | 8 | 8 | 5 | 4 |
| La prolactine sanguine a augmenté | 0 | 5 | 0 | 0 |
| Frissons | 0 | 5 | 2 | 0 |
| Diminution de l'activité | 0 | 5 | 0 | 1 |
| Déshydratation | 0 | 5 | 0 | 0 |
| Insomnie | 0 | 5 | 5 | 2 |
| Pyrexie | 15 | 5 | 21 | 14 |
| Stéréotypes | 0 | 5 | 0 | 0 |
| Infection des voies respiratoires supérieures | 21 | 5 | 7 | 10 |
| Vomissement | 10 | 5 | 5 | 8 |
| Le poids a diminué | 13 | 5 | 7 | 1 |
| Croupe | 5 | 3 | 0 | 1 |
| Infection de l'oreille | 8 | 3 | 9 | 5 |
| Gastro-entérite | 8 | 3 | 2 | 0 |
| Augmentation de la fréquence cardiaque | 5 | 3 | 0 | 2 |
| Irritabilité | 0 | 3 | 9 | 2 |
| Rhinite | 8 | 3 | 7 | 2 |
| Tremblement | 3 | 3 | 9 | 0 |
| Incontinence urinaire | 5 | 3 | 0 | 0 |
| Diminution de la glycémie | 0 | 0 | 9 | 1 |
| Bronchite | 3 | 0 | 9 | 1 |
| Contusion | 5 | 0 | 0 | 0 |
| Eczéma | 0 | 0 | 5 | 0 |
| Énurésie | 5 | 0 | 0 | 0 |
| Automne | 10 | 0 | 0 | 4 |
| Mal de tête | 8 | 0 | 0 | 2 |
| Laryngite | 0 | 0 | 5 | 0 |
| Négativisme | 5 | 0 | 0 | 0 |
| Statut epilepticus | 3 | 0 | 12 | 2 |
| Infection des voies urinaires | 5 | 0 | 5 | 0 |
| Infection virale | 0 | 0 | 5 | 1 |
| (1) 0,4 mg / kg / jour was not an intermediate dose. Patients on the 0,4 mg / kg / jour dose were also taking concomitant Stiripentol plus Clobazam which increases exposure of Fintepla. (2) Les patients des groupes placebo des études 1 et 2 ont été regroupés. (3) Consistait en trace et une régurgitation mitrale légère et une régurgitation aortique trace qui sont considérées comme physiologiques |
Syndrome de Lennox-Gastaut
Dans l'essai contrôlé par placebo, des patients atteints de LGS prenant un niveau de soins concomitants (étude 3) 176 patients ont été traités par Fintepla et 87 patients ont reçu un placebo [voir Études cliniques ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) et 29% of patients were at least 18 years of age 45% of patients were female et 79% were White. All patients were receiving at least one other AED.
Les taux d'arrêt en raison de toute réaction indésirable étaient de 6% et 5% pour les patients traités avec Fintepla 0,7 mg / kg / jour et 0,2 mg / kg / jour respectivement par rapport à 1% pour les patients sur placebo. Les effets indésirables les plus fréquents conduisant à l'arrêt chez les patients traités avec une dose de fintepla ont été la crise (2%) et la somnolence (2%).
Les effets indésirables courants qui se sont produits chez les patients traités par Fintepla (incidence au moins 10% et supérieur au placebo) étaient la diarrhée; diminution de l'appétit; fatigue; somnolence; vomissement.
Le tableau 5 répertorie les effets indésirables qui ont été signalés chez 5% ou plus des patients traités par Fintepla et à un rythme supérieur à ceux du placebo pendant les phases de titrage et d'entretien de l'étude 3.
Tableau 5: Réactions indésirables chez 5% ou plus des patients traités par Fintepla et supérieur au placebo dans l'essai contrôlé par placebo pour le syndrome de Lennox Gastaut (étude 3)
| Réaction indésirable | Fintepla Dose Group | ||
| Étude 3 | Groupe placebo | ||
| 0,2 mg / kg / jour | 0,7 mg / kg / jour | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Diminution de l'appétit | 20 | 36 | 12 |
| Fatigue malaise asthenia | 14 | 24 | 16 |
| Somnolence sédation léthargie | 12 | 22 | 16 |
| Diarrhée | 11 | 13 | 5 |
| Constipation | 6 | 9 | 6 |
| Vomissement | 14 | 8 | 6 |
| Le poids a diminué | 2 | 8 | 2 |
| Infection des voies respiratoires supérieures | 8 | 7 | 3 |
| Crise d'épilepsie | 9 | 5 | 7 |
| Irritabilité | 8 | 3 | 6 |
Évaluations de la sécurité échocardiographique des maladies cardiaques valvulaires et de l'hypertension artérielle pulmonaire
Les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire ont été évaluées dans les études de prolongation de placebocallé et ouverte via une échocardiographie pendant une durée pouvant aller jusqu'à 3 ans pour 341 patients DS et 263 patients LGS [voir AVERTISSEMENTS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation et assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
Dans ces études cliniques, deux patients atteints de LGS ont présenté une légère régurgitation aortique (AR), mais aucun des patients n'avait de signes ou de symptômes cardiaques ou de preuves de changements structurels valvulaires.
Aucun des deux patients n'avait VHD. Les taux d'AR légers sont cohérents avec ceux observés dans la période de dépistage avant le traitement (3 patients en LGS et 1 patient dans les essais cliniques DS).
Expérience de commercialisation de la poste
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de la fintepla. Étant donné que ces réactions sont rapportées volontairement d'une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à l'exposition au médicament.
Troubles psychiatriques : agression
Interactions médicamenteuses for Fintepla
Effet des autres médicaments sur Fintepla
Stiripentol plus Clobazam
La co-administration de fintepla avec le stimipentol plus le clobazam avec ou sans valproate augmente les concentrations plasmatiques de fenfluramine [voir Pharmacologie clinique ]. If Fintepla is coadministered with Stiripentol plus Clobazam the maximum daily dosage of Fintepla is 0,2 mg / kg deux fois par jour (maximum daily dosage of 17 mg) [see Posologie et administration ].
Forts inducteurs CYP1A2 CYP2B6 ou CYP3A
La co-administration de Fintepla avec de forts inducteurs CYP1A2 CYP2B6 ou CYP3A diminuera les concentrations plasmatiques de fenfluramine qui peuvent réduire l'efficacité de la fintepla [voir Pharmacologie clinique ].
Il est recommandé d'éviter la co-administration de forts inducteurs CYP1A2 CYP2B6 ou CYP3A. Si la co-administration d'un fort CYP1A2 CYP2B6 ou du CYP3A avec Fintepla est nécessaire, surveillez le patient pour réduire l'efficacité et envisagez d'augmenter le dosage de la fintepla selon les besoins; Cependant, ne dépassez pas la dose quotidienne maximale de Fintepla [voir Posologie et administration ].
Si un fort inducteur CYP1A2 CYP2B6 ou CYP3A est interrompu pendant le traitement d'entretien avec Fintepla, considérez une réduction progressive de la dose de fintepla à la dose administrée avant de lancer l'inducteur [voir AVERTISSEMENTS AND PRECAUTIONS ].
Forts inhibiteurs du CYP1A2 ou du CYP2D6
La co-administration de Fintepla avec de forts inhibiteurs du CYP1A2 ou du CYP2D6 augmentera les concentrations plasmatiques de fenfluramine [voir Pharmacologie clinique ]. If Fintepla is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of Fintepla is 20 mg [see Posologie et administration ].
Si un fort inhibiteur du CYP1A2 ou du CYP2D6 est interrompu pendant le traitement d'entretien avec Fintepla, envisagez une augmentation progressive de la dose de fintepla à la dose recommandée sans inhibiteurs du CYP1A2 ou du CYP2D6; Cependant, ne dépassez pas la dose quotidienne maximale de Fintepla [voir Posologie et administration ].
Si la fintepla est co-administrée avec du soripentol et un inhibiteur fort du CYP1A2 ou du CYP2D6 ne dépasse pas la dose quotidienne maximale de fintepla de 17 mg [voir Posologie et administration ].
Effets des antagonistes des récepteurs de la sérotonine
La cyproheptadine et puissants 5-HT1A 5-HT1D 5-HT2A et 5-HT2C Les antagonistes des récepteurs de la sérotonine peuvent diminuer l'efficacité de la fintepla. Si la cyproheptadine ou puissant 5 - HT1A 5 - HT1D 5-HT2A ou 5-HT2C Les antagonistes des récepteurs sont co-administrés avec des patients Fintepla doivent être surveillés de manière appropriée.
Drogues sérotoninergiques
L'administration concomitante de fintepla et de médicaments (par exemple SSRI SNRIS TCAS MAO inhibiteurs de la trazodone, etc.) des médicaments en vente libre (par exemple dextrométhorphane) ou des suppléments à base de plantes (par exemple, St. Johns wot) qui augmentent la sérotonine peuvent augmenter le risque du syndrome sérotonine [voir ST. AVERTISSEMENTS AND PRECAUTIONS ]. Concomitant use of Fintepla is contraindicated within 14 days of taking MAOIs. Use Fintepla with caution in patients taking other medications that increase sérotonine.
Avertissements pour Fintepla
Inclus dans le cadre du 'PRÉCAUTIONS' Section
Précautions pour Fintepla
Maladie cardiaque valvulaire et hypertension artérielle pulmonaire
Fintepla can cause valvular heart disease (VHD) et pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in Fintepla) et valvular heart disease et pulmonary arterial hypertension. Although no patients receiving Fintepla developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS et LGS of up to 3 years in duration cases of valvular heart disease et pulmonary arterial hypertension have been reported during use of Fintepla in the postmarketing setting [see Avertissement de boîte et Effets indésirables ].
En raison de ce risque, une surveillance cardiaque est nécessaire avant de commencer le traitement pendant le traitement et après le traitement avec Fintepla. La surveillance cardiaque via l'échocardiogramme peut identifier des preuves de maladies cardiaques valvulaires et d'hypertension artérielle pulmonaire avant qu'un patient ne devienne symptomatique aidant dans la détection précoce de ces conditions.
Surveillance
Avant de commencer le traitement, les patients doivent subir un échocardiogramme pour évaluer les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire.
Les échocardiogrammes doivent être répétés tous les 6 mois et une fois 3 à 6 mois après le traitement avec Fintepla.
Le prescripteur doit prendre en compte les avantages par rapport aux risques d'initiation ou de traitement continu avec Fintepla si l'un des signes suivants est observé via l'écho:
- Anomalie valvulaire ou nouvelle anomalie via l'échocardiogramme.
- VHD comme indiqué par une régurgitation aortique légère ou plus élevée ou une régurgitation mitrale modérée ou supérieure avec des caractéristiques supplémentaires de VHD (par exemple, épaississement de la valve ou mouvement de valve restrictif).
- HAP comme indiqué par la pression élevée du cœur / de l'artère pulmonaire droite (PASP> 35 mm Hg).
Fintepla is available only through a restricted program under a REMS [see Fintepla REMS Program ].
Fintepla REMS Program
Fintepla is available only through a restricted distribution program called the Fintepla REMS program because of the risk of valvular heart disease et pulmonary arterial hypertension [see Maladie cardiaque valvulaire et hypertension artérielle pulmonaire ].
Les exigences notables du programme Fintepla REMS comprennent:
- Les prescripteurs doivent être certifiés en s'inscrivant au programme Fintepla REMS.
- Les prescripteurs doivent conseiller les patients recevant une fintepla sur le risque de maladie cardiaque valvulaire et d'hypertension artérielle pulmonaire comment reconnaître les signes et les symptômes des maladies cardiaques valvulaires et de l'hypertension artérielle pulmonaire la nécessité d'un traitement de base (prétraitement) et d'une surveillance cardiaque périodique via un échocardiogramme sur l'échocardiogramme.
- Les patients doivent s'inscrire au programme REMS et se conformer aux exigences de surveillance continues [voir Maladie cardiaque valvulaire et hypertension artérielle pulmonaire ].
- La pharmacie doit être certifiée en s'inscrivant au programme REMS et ne doit se dispenser qu'aux patients autorisés à recevoir Fintepla.
- Les grossistes et les distributeurs ne doivent distribuer que des pharmacies certifiées.
De plus amples informations sont disponibles sur www.finteplalems.com ou par téléphone au 1-877-964-3649.
Diminution de l'appétit et diminution du poids
Fintepla can cause decreases in appetite et weight. In placebo-controlled studies for DS (Étude 1 et Étude 2 combined) approximately 37% of patients treated with Fintepla reported as an adverse reaction diminution de l'appétit et approximately 9% reported diminution du poids as compared to 8% et 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Étude 3) approximately 28% of patients treated with Fintepla reported as an adverse reaction diminution de l'appétit et approximately 5% reported diminution du poids as compared to 15% et 2% respectively of patients on placebo [see Effets indésirables ]. By the end of the controlled studies 19% (Studies 1 et 2 combined) of DS patients et 7% (Étude 3) of LGS patients treated with Fintepla had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Étude 1 et 2) et 0% (Étude 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on Fintepla 0,7 mg / kg / jour (Étude 1) 19% of patients on Fintepla 0,4 mg / kg / jour in combination with stiripentol (Étude 2) et 13% of patients taking Fintepla 0,2 mg / kg / jour (Étude 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on Fintepla 0,7 mg / kg / jour (Étude 3) et 6% of patients on Fintepla 0,2 mg / kg / jour (Étude 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS et most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with Fintepla should be carefully monitored. Weight should be monitored regularly during treatment with Fintepla et dose modifications should be considered if a decrease in weight is observed.
Sédation de somnolence et léthargie
Fintepla can cause somnolence sédation et léthargie. In controlled studies for DS (Étude 1 et Étude 2 combined) the incidence of somnolence sédation et léthargie was 25% in patients treated with Fintepla compared with 11% of patients on placebo. In the controlled study for LGS (Étude 3) the incidence of somnolence sédation et léthargie was 19% in patients treated with Fintepla compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Effets indésirables ].
Les autres dépresseurs du système nerveux central (SNC), y compris l'alcool, pourraient potentialiser ces effets de la fintepla. Les prescripteurs doivent surveiller les patients pour la somnolence et la sédation et devraient conseiller aux patients de ne pas conduire ou d'exploiter des machines jusqu'à ce qu'ils aient acquis une expérience suffisante sur Fintepla pour évaluer si elle affecte négativement leur capacité à conduire ou à exploiter des machines.
Comportement suicidaire et idéation
Les médicaments antiépileptiques (AED), y compris la fintepla, augmentent le risque de pensées ou de comportement suicidaires chez les patients prenant ces médicaments pour toute indication. Les patients traités avec un DEA pour toute indication doivent être surveillés pour l'émergence ou l'aggravation des pensées ou un comportement suicidaires de dépression ou tout changement inhabituel d'humeur ou de comportement.
Des analyses regroupées de 199 essais cliniques contrôlés par placebo (thérapie mono- et complément) de 11 DEA différents qui n'incluaient pas Fintepla ont montré que les patients randomisés pour l'un des DAE avaient environ twice le risque (risque relatif ajusté 1,8 IC à 95%: 1,2 2,7) de la pensée ou du comportement suicidale par rapport aux patients aléatoire à PlaceBo. Dans ces essais qui avaient une durée médiane de traitement de 12 semaines, le taux d'incidence estimé de comportement suicidaire ou d'idéation chez 27863 patients traités par AED était de 0,43% contre 0,24% chez 16029 patients traités par placebo représentant une augmentation d'environ un cas de réflexion ou de comportement suicidaire pour 530 patients traités. Il y avait quatre suicides chez les patients traités par médicaments dans les essais et aucun chez les patients traités par placebo, mais le nombre est trop petit pour permettre une conclusion sur l'effet du médicament sur le suicide.
Le risque accru de pensées ou de comportements suicidaires avec les DEA a été observé dès 1 semaine après le début du traitement médicamenteux avec des DEA et a persisté pour la durée du traitement évalué. Étant donné que la plupart des essais inclus dans l'analyse ne s'étendent pas au-delà de 24 semaines, le risque de pensées suicidaires ou de comportement au-delà de 24 semaines n'a pas pu être évaluée.
Le risque de pensées ou de comportements suicidaires était généralement cohérent parmi les médicaments dans les données analysées. La conclusion d'un risque accru avec les DEA de mécanismes d'action variables et à travers une gamme d'indications suggère que le risque s'applique à tous les DEA utilisés pour toute indication. Le risque ne varie pas considérablement selon l'âge (5 à 100 ans) dans les essais cliniques analysés. Le tableau 3 montre un risque absolu et relatif par indication pour tous les DEA évalués.
Tableau 3: Risque de pensées ou de comportements suicidaires par indication de médicaments antiépileptiques dans l'analyse regroupée
| Indication | Patients placebo avec des événements pour 1000 patients | Patiens de médicament avec des événements pour 1000 patients | Risque relatif: incidence des événements chez les patients atteints de médicament / incidence chez les patients placebo | Différence de risque: patients atteints de médicament supplémentaires avec des événements pour 1000 patients |
| Épilepsie | 1.0 | 3.4 | 3.5 | 2.4 |
| Psychiatrique | 5.7 | 8.5 | 1.5 | 2.9 |
| Autre | 1.0 | 1.8 | 1.9 | 0.9 |
| Total | 2.4 | 4.3 | 1.8 | 1.9 |
Le risque relatif de pensées ou de comportements suicidaires était plus élevé dans les essais cliniques chez les patients atteints d'épilepsie que dans les essais cliniques chez les patients atteints de conditions psychiatriques ou autres, mais les différences de risque absolues étaient similaires pour l'épilepsie et les indications psychiatriques.
Quiconque envisage de prescrire une fintepla ou tout autre DEA doit équilibrer le risque de pensées ou de comportements suicidaires avec le risque de maladie non traitée. L'épilepsie et de nombreuses autres maladies pour lesquelles les DEA sont prescrites sont elles-mêmes associées à la morbidité et à la mortalité et à un risque accru de pensées et de comportement suicidaires. Si les pensées et le comportement suicidaires émergent pendant le traitement, examinez si l'émergence de ces symptômes chez un patient donné peut être liée à la maladie traitée.
Retrait des médicaments antiépileptiques
Comme pour la plupart des AED, Fintepla doit généralement être retirée progressivement en raison du risque d'augmentation de la fréquence des crises et du statut épileptique. Si le retrait est nécessaire en raison d'une réaction défavorable grave, un arrêt rapide peut être pris en compte.
Syndrome de Seroton
Syndrome de la sérotonine Une condition potentiellement potentiellement mortelle peut se produire avec une fintepla, en particulier avec l'administration concomitante de Fintepla avec d'autres médicaments sérotonergiques, notamment mais sans s'y limiter antidépresseurs (TCAS) Bupropion Triptans Suppléments alimentaires (par exemple les médicaments contre le tryptophane de St. Johns Wort) qui altèrent le métabolisme de la sérotonine (y compris les inhibiteurs de la monoamine oxydase [MAOIS] Contre-indications ] dextrométhorphane Lithium tramadol et antipsychotiques avec activité agoniste sérotoninergique. Les patients doivent être surveillés pour l'émergence de signes et symptômes du syndrome de la sérotonine qui incluent les changements d'état mental (par exemple, les hallucinations d'agitation coma) Instabilité autonome (par exemple, les signes neuromusculaires de la pression artérielle de tachycardie) et / ou les symptômes gastronorestinaux (par exemple, la diomorcole nauséeuse. Si le syndrome de la sérotonine est suspecté, le traitement par Fintepla doit être arrêté immédiatement et le traitement symptomatique doit être démarré.
Augmentation de la pression artérielle
Fintepla can cause an increase in blood pressure [see Effets indésirables ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving Fintepla developed a hypertensive crisis. Monitor blood pressure in patients treated with Fintepla.
Glaucome
La fenfluramine peut provoquer la mydriase et peut précipiter la fermeture d'angle glaucome . Envisagez d'arrêter le traitement avec Fintepla chez les patients présentant une diminution aiguë de l'acuité visuelle ou de la douleur oculaire.
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Guide des médicaments et Instructions for Use ).
Informations sur l'administration
Conseiller les patients qui se sont prescrits Fintepla pour utiliser les seringues postérieures à la dose orale fournies par la pharmacie [voir Posologie et administration et Instructions pour une utilisation ]. Instruct patients to discard any unused Fintepla 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Comment fourni ].
Maladie cardiaque valvulaire et hypertension artérielle pulmonaire
Informez les patients que la surveillance cardiaque doit être effectuée en utilisant l'échocardiographie pour surveiller de graves changements de valve cardiaque ou une pression artérielle élevée dans les artères des poumons [voir AVERTISSEMENTS AND PRECAUTIONS ].
Fintepla REMS Program
Fintepla is available only through a restricted program called the Fintepla REMS program [see AVERTISSEMENTS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- Les patients doivent s'inscrire au programme et se conformer aux exigences en cours de surveillance de l'échocardiogramme [voir AVERTISSEMENTS AND PRECAUTIONS ].
Fintepla is only prescribed by certified health care providers et only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number et website for information on how to obtain the product [see AVERTISSEMENTS AND PRECAUTIONS ].
Diminution de l'appétit et diminution du poids
Conseillez les patients que l'appétit diminué est fréquent pendant le traitement par Fintepla, ce qui peut entraîner une diminution du poids [voir AVERTISSEMENTS AND PRECAUTIONS ].
Sédation de somnolence et léthargie
Informez les patients que la Fintepla peut provoquer une sédation de somnolence et une léthargie. Attention aux patients concernant les machines dangereuses de fonctionnement, y compris les véhicules à moteur jusqu'à ce qu'ils soient raisonnablement certains que Fintepla ne les affecte pas négativement (par exemple, altérer la pensée ou la motricité) [voir AVERTISSEMENTS AND PRECAUTIONS ].
Pensée et comportement suicidaires
Conseiller les patients leurs soignants et leurs familles selon lesquels des médicaments antiépileptiques peuvent augmenter le risque de pensées et de comportements suicidaires et leur conseiller d'être alerte pour l'émergence ou l'aggravation des symptômes de dépression tout changement inhabituel d'humeur ou de comportement ou de l'émergence des pensées suicidaires ou des pensées d'automutilation. Demandez aux patients des soignants et des familles de signaler immédiatement les comportements préoccupants aux prestataires de soins de santé [voir AVERTISSEMENTS AND PRECAUTIONS ].
Retrait des médicaments antiépileptiques (AEDs)
Conseiller aux patients de ne pas interrompre l'utilisation de Fintepla sans consulter leur fournisseur de soins de santé. Fintepla doit normalement être progressivement retirée pour réduire le potentiel de fréquence accrue et de statut d'épilepticus [voir Posologie et administration et AVERTISSEMENTS AND PRECAUTIONS ].
Syndrome de Seroton
Informer les patients du risque de syndrome de sérotonine qui peut être mortel. Conseiller les patients sur les signes et symptômes du syndrome de la sérotonine et que certains médicaments en vente libre et suppléments à base de plantes peuvent augmenter ce risque [voir AVERTISSEMENTS AND PRECAUTIONS ].
Augmentation de la pression artérielle
Informer les patients que la fintepla peut provoquer une augmentation de la pression artérielle [voir AVERTISSEMENTS AND PRECAUTIONS ].
Glaucome
Informez les patients que la Fintepla peut provoquer la mydriase et précipiter le glaucome de fermeture d'angle.
Demandez aux patients de contacter leur fournisseur de soins de santé s'ils ont une diminution aiguë de l'acuité visuelle ou de la douleur oculaire [voir AVERTISSEMENTS AND PRECAUTIONS ].
Registre de grossesse
Conseiller aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant le thérapie par Fintepla. Encouragez les femmes qui prennent Fintepla à s'inscrire au registre de grossesse nord-américain antiépileptique (NAAED) si elles tombent enceintes.
Ce registre collecte des informations sur la sécurité des médicaments antiépileptiques pendant la grossesse [voir Utiliser dans des populations spécifiques ].
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
Cancérogenèse
L'administration orale de fenfluramine aux souris Tg.Rash2 (0 4,3 13,0 34,6 ou 51,8 mg / kg / jour) pendant 26 semaines et aux rats mâles et femelles (0 0,9 2,2 ou 6,9 mg / kg / jour) pendant 89 et 97 semaines respectivement, ce qui n'a résulté des tumeurs induites par les médicaments dans les deux espèces. Chez le rat, les expositions au plasma (ASC) de la fenfluramine et de la norfenfluramine (le métabolite majeur) à la dose la plus élevée testée étaient respectivement environ 5 et 11 fois celles de l'homme à la dose humaine maximale recommandée (MRHD) de 26 mg / jour.
Mutagenèse
La fenfluramine était négative dans un in vitro test de mutation bactérienne (AMES) et un en vain Micronucleus et comète chez le rat.
Altération de la fertilité
L'administration orale de fenfluramine (0 3,0 6,9 ou 17,3 mg / kg / jour) à des rats mâles et femelles avant et tout au long de l'accouplement et de la poursuite des femmes au sperme 7 de la gestation a entraîné une diminution de la fertilité et une augmentation du sperme anormal et un vacuolation épithéliale de la lutteur et de la dose plus élevée de la dose et de la dose plus élevée et de la cyclicité ométrante ont diminué les sociétés et la dose la plus élevée et l'occasionne Implantations et augmentation de l'embryolethalité à la dose moyenne et élevée. Ces doses étaient associées à la toxicité parentale. Les doses de non-effet pour les effets indésirables sur la fertilité et les performances de reproduction chez le rat (NULL,9 et 3,0 mg / kg / jour chez les hommes et les femmes respectivement) ont été associées à des expositions à la fenfluramine plasmatique (AUC) environ 3 et 0,6 fois respectivement et aux expositions Norfenfluramine environ 5 et 3 fois respectivement chez les humains à la MRHD.
Utiliser dans des populations spécifiques
Grossesse
Grossesse Exposure Registry
Il existe un registre d'exposition à la grossesse qui surveille les résultats de la grossesse chez les femmes exposées à des médicaments antiépileptiques (AED) tels que la Fintepla pendant la grossesse. Encouragez les femmes qui prennent Fintepla pendant la grossesse à s'inscrire dans le registre de grossesse antiépileptique nord-américain (NAAED) en appelant le numéro 1-888-233334 sans frais ou en visitant https://www.aedpregnancyregistry.org.
Résumé des risques
Il n'y a pas de données sur l'utilisation de Fintepla chez les femmes enceintes. Les données disponibles des études épidémiologiques avec la fenfluramine ou la dexfenfluramine sont insuffisantes pour évaluer un risque associé au médicament de malformations congénitales majeures ou d'autres résultats indésirables maternels ou fœtaux. Fintepla peut provoquer une diminution de l'appétit et une diminution du poids [voir AVERTISSEMENTS AND PRECAUTIONS ]] Surveillez un gain de poids adéquat pendant la grossesse. In animal studies administration of fenfluramine throughout organogenesis (rat and rabbit) or throughout gestation and lactation (rat) resulted in adverse effects on development (fetal malformations embryofetal and offspring mortality and growth impairment) in the presence of maternal toxicity at clinically relevant maternal plasma levels of fenfluramine and its major active metabolite (see Données ).
Le risque de fond estimé de malformations congénitales majeures et de fausse couche pour la population indiquée est inconnue. Toutes les grossesses ont un risque de fond de délai de congédiement perte ou d'autres résultats négatifs. Dans la population générale américaine, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est respectivement de 2 à 4% et 15 à 20%.
Données
Données sur les animaux
L'administration orale de fenfluramine (0 4,5 8,6 ou 34,6 mg / kg / jour) à des rats enceintes pendant l'organogenèse a entraîné une diminution des poids corporels fœtaux et une augmentation marquée des malformations fœtales (externe viscérale et squelettique) à la dose la plus élevée testée qui était associée à la toxicité maternelle. À la dose sans effet (NULL,6 mg / kg / jour) pour les effets indésirables sur le développement embryofétal chez les expositions au plasma maternel (ASC) de la fenfluramine et de la norfenfluramine (le métabolite majeur) étaient respectivement environ 2 et 5 fois celles en humains à la dose humaine maximale recommandée (MRHD) de 26 mg / jour.
L'administration orale de fenfluramine (0 4,3 8,6 13,0 mg / kg / jour) à des lapins enceintes tout au long de l'organogenèse a entraîné une augmentation de la mortalité embryofétale à toutes les doses et une augmentation des malformations fœtales (externe et squelettique) à la dose la plus élevée testée qui était associée à la toxicité maternelle. Une dose d'effet sans inverse pour les effets néfastes sur le développement embryofétal chez le lapin n'a pas été identifiée. À la dose la plus faible testée chez les lapins (NULL,3 mg / kg / jour), les expositions au plasma maternel de la fenfluramine et de la norfenfluramine étaient inférieures à celles de l'homme au MRHD.
L'administration orale de fenfluramine (0 4,3 86 ou 34,6 mg / kg / jour) à des rats femelles tout au long de la gestation et de la lactation a entraîné une augmentation marquée des chiots morts et du développement de la progéniture néonatale à la dose la plus élevée et retardée de croissance et de développement réflexe pendant la période de préswean à toutes les doses. Le gain de poids corporel maternel a été diminué à toutes les doses pendant la grossesse et aux deux doses les plus élevées pendant la lactation. Une dose de non-effet pour les effets indésirables sur le développement pré et postnatal chez le rat n'a pas été déterminée. À la dose la plus faible testée chez le rat (NULL,3 mg / kg / jour), les expositions plasmatiques maternelles de la fenfluramine et de la norfenfluramine étaient environ 0,5 et 3 fois respectivement celles de l'homme au MRHD.
Lactation
Résumé des risques
Il n'y a pas de données sur la présence de fenfluramine ou ses métabolites dans le lait maternel les effets sur le nourrisson allaité ou les effets sur la production de lait.
Les avantages du développement et de la santé de l'allaitement doivent être pris en compte avec le besoin clinique des mères de Fintepla et tout effet indésirable potentiel sur le nourrisson allaité de Fintepla ou de l'état maternel sous-jacent.
Femmes et mâles de potentiel reproducteur
Infertilité
Dans les études animales, l'administration orale de fenfluramine a entraîné des effets reproductifs négatifs chez les hommes et les femmes à des doses cliniquement pertinentes en présence d'une toxicité parentale [voir Toxicologie non clinique ].
Usage pédiatrique
La sécurité et l'efficacité de la Fintepla pour le traitement des crises associées à DS et LGS ont été établies chez les patients de 2 ans et plus.
L'utilisation de Fintepla pour le traitement des crises associées aux DS chez les patients de 2 ans et plus est soutenue par deux essais randomisés contrôlés par placebo en double aveugle chez 202 patients de 2 à 18 ans. L'utilisation de Fintepla pour le traitement des crises associées à la LGS est soutenue par une étude contrôlée par placebo randomisée en double aveugle chez 263 patients âgés de 2 à 35 ans, dont 187 patients moins de 18 ans [voir Avertissement de boîte AVERTISSEMENTS AND PRECAUTIONS Effets indésirables et Études cliniques ].
Fintepla can cause decreases in appetite et weight. The growth of pediatric patients treated with Fintepla should be carefully monitored.
La sécurité et l'efficacité des patients de moins de 2 ans n'ont pas été établies.
Données d'animaux juvéniles
L'administration orale de fenfluramine (0 3,0 78 ou 17,3 mg / kg / jour) à de jeunes rats pendant 10 semaines à partir du jour postnatal 7 a entraîné une réduction du poids corporel et des changements neurobehavioaux (diminution de l'activité locomotrice et des déficits d'apprentissage et de la mémoire) à toutes les doses testées. Les effets neurobehavioraux ont persisté après la fin du dosage. La taille des os a été diminuée aux doses moyennes et élevées; La taille du cerveau a diminué à la dose la plus élevée. Une récupération partielle ou complète a été observée pour ces critères de terminaison. Une dose sans effet pour la toxicité du développement postnatal n'a pas été identifiée. La dose la plus faible testée (NULL,0 mg / kg / jour) a été associée à des expositions à la fenfluramine plasmatique (AUC) moins que celles chez l'homme à la dose humaine maximale recommandée (MRHD) de 26 mg / jour et à la norfenfluramine (métabolite) exposés (AUC) à environ 2 fois dans l'homme au MRHD.
Utilisation gériatrique
Les études cliniques de Fintepla pour le traitement de DS ou de LGS n'incluaient pas les patients de 65 ans et plus pour déterminer s'ils réagissent différemment des patients plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente qui commence généralement à l'extrémité inférieure de la plage de dosage reflétant la plus grande fréquence de diminution de la fonction rénale ou cardiaque hépatique et de maladie concomitante ou autre médicament.
carafate 1 gm / 10 ml suspendu
Trouble rénal
Chez les patients atteints de taux de filtration glomérulaire estimé (EGFR) 15 à 29 ml / min / 1,73 m 2 Ne dépassez pas la dose quotidienne maximale de Fintepla de 20 mg. Chez les patients atteints d'EGFR 15 à 29 ml / min / 1,73 m 2 et concomitant stiripentol use do not exceed the maximum daily dosage of Fintepla of 17 mg [see Posologie et administration et Pharmacologie clinique ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Trouble hépatique
Les expositions molaires combinées de fenfluramine et de norfenfluramine ont été augmentées chez les sujets avec divers degrés de déficience hépatique (Child-Pugh classe A B et C) nécessitant un ajustement posologique chez ces patients [voir Posologie et administration et Pharmacologie clinique ].
Informations sur la surdose pour Fintepla
Une surdose n'a pas été observée dans le programme d'essais cliniques Fintepla. Cependant, une surdose de fenfluramine L'ingrédient actif de Fintepla a été signalé à des doses plus élevées que celles incluses dans le programme d'essais cliniques. Certains cas étaient fataux. Les événements signalés après une surdose comprennent la mydriase tachycardie des tremblements de rinçage / contractions / spasmes musculaires agitation / agitation / anxiété augmenté le tonus musculaire / rigueur / l'opisthotonos détresse ou défaillance et crise de défaillance. Le coma de crise et l'arrestation cardiorespiratoire ont été signalés dans la plupart des surdoses mortelles.
Il n'y a pas d'antidote spécifique disponible dans les réactions de surdose de la fintepla. En cas de pratique médicale standard de surdose pour la gestion de la surdosage de médicaments, il faut être utilisé. Une oxygénation et une ventilation adéquates des voies respiratoires doivent être assurées; La surveillance du rythme cardiaque et de la mesure des signes vitaux est recommandée. Un centre de contrôle du poison certifié doit être contacté pour des informations mises à jour sur la gestion de la surdose avec Fintepla.
Contre-indications pour Fintepla
Fintepla is contraindicated in patients with:
- Hypersensibilité à la fenfluramine ou à l'un des excipients de Fintepla [voir DESCRIPTION ]
- Utilisation concomitante ou dans les 14 jours suivant l'administration d'inhibiteurs de monoamine oxydase en raison d'un risque accru de syndrome de sérotonine [voir AVERTISSEMENTS AND PRECAUTIONS ]
Pharmacologie clinique for Fintepla
Mécanisme d'action
Le mécanisme précis par lequel la fenfluramine exerce ses effets thérapeutiques dans le traitement des crises associées au syndrome de Dravet et au syndrome de Lennox-Gastaut est inconnue. La fenfluramine et la norfenfluramine métabolite présentent une activité agoniste aux récepteurs de la sérotonine 5-HT2. Il existe une association entre les médicaments sérotoninergiques avec une activité agoniste des récepteurs 5-HT2B, notamment la fenfluramine et la norfenfluramine et les maladies cardiaques valvulaires et l'hypertension artérielle pulmonaire.
Pharmacodynamique
Électrophysiologie cardiaque
À une dose 4 fois, la dose maximale recommandée Fintepla n'a pas prolongé l'intervalle QT lorsqu'il est testé dans une population adulte.
Pharmacocinétique
La pharmacocinétique de la fenfluramine et de la norfenfluramine a été étudiée chez des sujets sains chez les patients pédiatriques atteints de DS et chez des patients pédiatriques et adultes atteints de LGS. L'exposition systémique à l'état d'équilibre (CMAX et AUC) de la fenfluramine était légèrement supérieure à la dose proportionnelle sur la plage de dose de 13 à 51,8 mg de fenfluramine deux fois par jour (c'est-à-dire 1 à 4 fois la dose maximale recommandée). Chez les patients pédiatriques atteints de DS qui ont reçu Fintepla 0,7 mg / kg / jour jusqu'à une dose quotidienne totale de 26 mg de fenfluramine, la fenfluramine à l'état d'équilibre géométrique (coefficient de variation) était de 68,0 (41%) ng / ml et auc0-24h était de 1390 (44%) ng * h / ml.
Absorption
La fenfluramine a un temps pour une concentration plasmatique maximale (TMAX) de 3 à 5 heures à l'état d'équilibre. La biodisponibilité absolue de la fenfluramine est d'environ 68 à 74%. Il n'y a eu aucun effet de nourriture sur la pharmacocinétique de la fenfluramine ou de la norfenfluramine.
Distribution
Le volume apparent géométrique (CV%) de distribution (VZ / F) de la fenfluramine est de 11,9 (NULL,5%) L / kg après l'administration orale de Fintepla chez des sujets sains. La fenfluramine est à 50% liée aux protéines plasmatiques humaines in vitro et binding is independent of drug concentrations.
Élimination
La demi-vie d'élimination de la fenfluramine était de 20 heures et la clairance géométrique moyenne (% CV) (Cl / F) était de 24,8 (29%) L / H après l'administration orale de Fintepla chez des sujets sains.
Métabolisme
Plus de 75% de la fenfluramine est métabolisée en norfenfluramine avant l'élimination principalement par CYP1A2 CYP2B6 et CYP2D6. Les autres enzymes CYP impliquées dans une mineur sont CYP2C9 CYP2C19 et CYP3A4 / 5. La fenfluramine et la norfenfluramine sont pharmacologiquement actives. La norfenfluramine est encore désaminée et oxydée pour former des métabolites inactifs.
Excrétion
La majeure partie d'une dose de fenfluramine administrée par voie orale (supérieure à 90%) est excrétée dans l'urine sous forme de fenfluramine norfenfluramine ou d'autres métabolites avec la fenfluramine et la norfenfluramine représentant moins de 25% du total; Moins de 5% se trouvent dans les excréments.
Populations spécifiques
L'effet de l'âge (extrêmes: 2 à 50 ans) sexe et race n'a eu aucun effet cliniquement significatif sur la pharmacocinétique de la fenfluramine.
Patients souffrant de troubles rénaux
Dans une étude clinique dédiée comparant la pharmacocinétique d'une seule dose de 0,35 mg / kg de fintepla chez des sujets ayant une déficience rénale grave (EGFR <30 mL/min/1.73m 2 déterminé par MDRD) et apparié des volontaires sains, CMAX et AUC0-INF de fenfluramine ont augmenté respectivement de 20% et 88% et CMAX et AUC0-INF de Norfenfluramine ont augmenté de 13% et 21% respectivement chez les sujets ayant une insuffisance rénale sévère [voir [voir Utiliser dans des populations spécifiques ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 (déterminé par MDRD). On ne sait pas si la fenfluramine ou la norfenfluramine est dialysable.
Patients souffrant de déficience hépatique
Dans une étude comparant la pharmacocinétique d'une seule dose de 0,35 mg / kg de fintepla chez des sujets présentant une déficience hépatique modérée légère ou sévère (Child-Pugh classe A B ou C) et les sujets avec une fonction hépatique normale AuSC0-T de la fenfluramine augmentée de 95% 113% et 185% dans les sujets avec une légère importance modérée et sévère des impairment sévères consécutivement. Le CMAX de la fenfluramine a augmenté de 19% 16% et 29% chez les sujets présentant respectivement un léger trouble hépatique modéré et sévère. L'AUC0-T de la norfenfluramine a augmenté de 18% dans une déficience hépatique légère de 4% dans une déficience hépatique modérée et a diminué de 11% des troubles hépatiques graves. Le CMAX de la norfenfluramine a diminué de 21% 36% et 45% chez les sujets présentant respectivement une légère déficience hépatique modérée et sévère. L'auc0-T molaire combiné de la fenfluramine et de la norfenfluramine a augmenté de 55% 56% et 82% chez les sujets présentant respectivement légèrement des troubles hépatiques modérés et sévères. La CMAX molaire combinée de la fenfluramine et de la norfenfluramine a augmenté de 7,5% 1,3% et 8% chez les sujets présentant respectivement légèrement des troubles hépatiques modérés et sévères. La dose quotidienne maximale de Fintepla doit être réduite chez les patients présentant une déficience hépatique légère avec / sans stimipentol plus clobazam. La dose quotidienne maximale de Fintepla doit être réduite chez les patients présentant une déficience hépatique modérée ou sévère sans stimipentol plus Clobazam [voir Posologie et administration et Utiliser dans des populations spécifiques ].
Études d'interaction médicamenteuse
Études cliniques
Effet d'une seule dose de stimipentol clobazam et de combinaison d'acide valproïque
La co-administration d'une seule dose de 0,7 mg / kg de fintepla avec une seule dose de stimipentol clobazam et d'acide valproïque dans des volontaires sains a augmenté l'AUC0-Inf de fenfluramine par 69% et le CMAX par 18% et a diminué l'AUC0-72 HEURES DE NORFENFLURAMINE par 41% administré seul.
Effet du stimipentol en régime permanent plus Clobazam avec ou sans valproate
Des données pharmacocinétiques de fenfluramine ont été collectées auprès des patients après avoir reçu de multiples administrations de fenfluramine dans l'étude 1 ainsi que l'étude 2. La modélisation et la simulation pharmacocinétiques de la population ont été utilisées pour évaluer l'effet du stimipentol plus du clobazam avec ou sans valproate sur la fenfluramine pharmacocinétique. L'effet du stimipentol plus du clobazam avec ou sans valproate sur la pharmacocinétique de fenfluramine est plus élevé lorsque la fintepla est à l'état d'équilibre que pour la première dose de Fintepla. At steady state in the patient population the coadministration of 0.1 mg/kg twice daily (0.2 mg/kg/day) maximum 17 mg/day of FINTEPLA with stiripentol plus clobazam with or without valproate is expected to result in a 166% increase in fenfluramine AUC0-24 and a 38% decrease in norfenfluramine AUC0-24 as compared to 0.2 mg / kg / jour maximum 26 mg / jour dose de fintepla administrée seule [voir Posologie et administration et Interactions médicamenteuses ].
Effet du cannabidiol en régime permanent
La co-administration d'une seule dose de 0,35 mg / kg de fintepla avec des doses répétées de cannabidiol a augmenté l'AUC0-Inf de la fenfluramine de 59% et le CMAX de 10% et a diminué l'AUC0-Inf de Norfenfluramine de 22% et le CMAX par 33% par rapport à la fintepla administrée seule. Cette interaction ne devrait pas être cliniquement significative.
Effet de forts inhibiteurs du CYP1A2 ou du CYP2D6
La co-administration d'une seule dose de 0,35 mg / kg de fintepla avec de la fluvoxamine (un fort inhibiteur du CYP1A2) à l'état stable (50 mg une fois par jour) dans des volontaires sains a augmenté l'AUC0- infr Fintepla administrée seule [voir Interactions médicamenteuses ].
La co-administration d'une seule dose de 0,35 mg / kg de fintepla avec paroxétine (un fort inhibiteur du CYP2D6) à l'état stable (30 mg une fois par jour) dans des volontaires sains a augmenté l'AUC0-Inf de la fenfluramine de 81% et le CMAX de 13% et le CMAX et la CMAX par rapport à la FINLAPLAMIN administré seul [voir Interactions médicamenteuses ].
Effet de forts inducteurs CYP1A2 CYP2B6 ou CYP3A
La co-administration d'une seule dose de 0,35 mg / kg de Fintepla avec rifampin (un CYP1A2 CYP2B6 et l'inducteur CYP3A) à l'état d'équilibre (600 mg une fois par jour) dans des volontaires sains a diminué l'AUC0-inf de la fenfluramine par 58% et le CMAX par 40% et a augmenté le CMEAX de Norfenfluramine de 13% par rapport à la fintepla administrée seule [voir Interactions médicamenteuses ].
Effet de la fintepla sur d'autres médicaments
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination did not affect the pharmacokinetics of stiripentol nor the pharmacokinetics of clobazam or its N.desmethyl-metabolite norclobazam nor the pharmacokinetics of valproic acid as compared to the stiripentol Clobazam et combinaison d'acide valproïque seule. La co-administration d'une seule dose de 0,35 mg / kg de fintepla avec des doses répétées de cannabidiol n'a pas affecté la pharmacocinétique du cannabidiol par rapport au cannabidiol seul.
Études in vitro
La fenfluramine est principalement métabolisée par CYP1A2 CYP2B6 et CYP2D6 in vitro . Les autres enzymes CYP impliquées dans une mineur sont CYP2C9 CYP2C19 et CYP3A4 / 5.
Effet de la fenfluramine et de la norfenfluramine sur les substrats du CYP: Fenfluramine et Norfenfluramine ne sont pas des inhibiteurs ou des inducteurs de CYP1A2 CYP2B6 CYP2C8 CYP2C9 CYP2C19 CYP2D6 ou CYP3A4 à des concentrations cliniquement pertinentes.
Effet des transporteurs sur la fenfluramine et la norfenfluramine: la fenfluramine et la norfenfluramine ne sont pas des substrats des transporteurs P-G BCRP OAT1 OAT3 OCT2 MATE1 ou MATE2-K.
Effet de la fintepla sur les transporteurs: la fenfluramine et la norfenfluramine ne sont pas des inhibiteurs de P-gp BCRP OAT1B1 OATP1B3 OAT1 OAT3 OCT2 MATO1 ou MATE2-K Transporteurs.
Études cliniques
Syndrome de Dravet
L'efficacité de la Fintepla pour le traitement des crises associées aux DS chez les patients de 2 ans et plus a été établie dans deux essais randomisés contrôlés par placebo chez les patients chez les patients de 2 à 18 ans.
Étude 1 (N=117) compared a 0,7 mg / kg / jour et a 0,2 mg / kg / jour dose of Fintepla with placebo in patients who were not receiving stiripentol (NCT02682927 et NCT02826863).
Étude 2 (N=85) compared a 0,4 mg / kg / jour dose of Fintepla with placebo in patients who were receiving stiripentol et either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS et were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic et focal with observable motor signs. The baseline period was followed by retomization into a 2- week (Étude 1) or 3-week (Étude 2) titration period et a subsequent 12-week maintenance period where the dose of Fintepla remained stable.
Dans l'étude, 1 98% des patients prenaient entre 1 et 4 AED concomitants. Les AED concomitants les plus fréquemment utilisés (chez au moins 25% des patients) étaient le valproate (61%) Clobazam (59%) et le topiramate (25%). Dans l'étude, 2 100% des patients prenaient entre 2 et 4 AED concomitants. Les AED concomitants les plus fréquemment utilisés (chez au moins 25% des patients) étaient le stimipentol (100%) Clobazam (94%) et le valproate (89%).
Le critère d'évaluation de l'efficacité primaire dans les deux études a été le changement par rapport à la base de la fréquence des crises convulsives par 28 jours pendant les périodes combinées de 14 semaines (étude 1) ou 15 semaines (étude 2) de titrage et d'entretien (c'est-à-dire la période de traitement). L'intervalle le plus long médian entre les crises convulsifs a également été évalué.
Dans l'étude 1 et l'étude 2, la réduction de la fréquence des crises convulsives par 28 jours était statistiquement significativement plus élevée pour tous les groupes de dose de Fintepla par rapport au placebo (tableau 6). Une réduction des crises convulsives a été observée dans les 3 à 4 semaines suivant le démarrage de Fintepla et l'effet est resté généralement cohérent au cours de la période de traitement de 14 ou 15 semaines.
Tableau 6: Changement de la fréquence des crises convulsives pendant les patients hospitalisés de la période de traitement atteint du syndrome de Dravet (étude 1 et étude 2)
| Fréquence convulsive des crises (par 28 jours) | Placebo | Fintepla 0,2 mg / kg / jour | Fintepla 0,7 mg / kg / jour | Fintepla 0,4 mg / kg / jour |
| Étude 1 | N = 39 | N = 38 | N = 40 | N / A |
| Médiane de la période de base | 29.4 | 18.1 | 18.7 | N / A |
| % Différence par rapport au placebo * | -31,7% | -70,0% | N / A | |
| valeur p par rapport au placebo | 0.043 | <0.001 | ||
| Étude 2 | N = 42 | N / A | N / A | N = 43 |
| Médiane de la période de base | 11.5 | N / A | N / A | 15.0 |
| % Différence par rapport au placebo * | N / A | -59,5% | ||
| valeur p par rapport au placebo | <0.001 | |||
| * Dérivé du modèle d'analyse primaire ± Tous les patients atteints de 0,4 mg / kg / jour prenaient également du soripentol concomitant, ce qui augmente l'exposition de la fintepla. |
Les figures 1 et 2 affichent le pourcentage de patients par catégorie de réponse de crise de la ligne de base en fréquence de crise convulsive (par 28 jours) pendant la période de traitement dans l'étude 1 et l'étude 2 respectivement.
Figure 1: Proportion de patients par catégorie de réponse de crise pour Fintepla et placebo chez les patients atteints du syndrome de Dravet (étude 1)
| |
Figure 2: Proportion de patients par catégorie de réponse de crise pour la fintepla et le placebo chez les patients atteints du syndrome de Dravet (étude 2)
| |
Dans l'étude 1 3 sur 40 (8%), les patients du groupe Fintepla 0,7 mg / kg / jour et 3 des 38 (8%) des patients du groupe Fintepla 0,2 mg / kg / jour n'ont signalé aucune crise de convulsive pendant la période de traitement de 14 semaines par rapport à 0 patients dans le groupe placebo. Dans l'étude 2 1 sur 43 (2%), les patients du groupe Fintepla 0,4 mg / kg / jour n'ont signalé aucune crise convulsive pendant la période de traitement de 15 semaines par rapport à 0 patients dans le groupe placebo.
Dans l'étude 1 et l'étude 2, la Fintepla a été associée à un intervalle plus long statistiquement significatif entre les crises convulsives par rapport au placebo (figure 3).
Figure 3: Intervalle le plus long médian entre les crises convulsives chez les patients atteints du syndrome de Dravet (étude 1 et étude 2)
| |
Syndrome de Lennox-Gastaut
L'efficacité de la Fintepla pour le traitement des crises associées aux LG chez les patients de 2 ans et plus a été établie dans une étude randomisée contrôlée par placebo chez 263 patients de 2 à 35 ans (étude 3; NCT03355209).
Étude 3 compared a 0,7 mg / kg / jour et a 0,2 mg / kg / jour dose of Fintepla with placebo.
Les patients avaient un diagnostic de LGS et ont été insuffisamment contrôlés sur au moins un AED avec ou sans stimulation du nerf vagal et / ou un régime cétogène. L'étude a connu une période de référence de 4 semaines pendant laquelle les patients devaient avoir un minimum de 8 crises de baisse pendant la thérapie AED stable. Les crises de baisse ont été généralisées toniques-cloniques généralisées secondairement généralisées généralisées les crises atoniques toniques ou toniques-atoniques toniques qui ont été confirmées pour entraîner des gouttes. La période de référence a été suivie par la randomisation en une période de titrage de 2 semaines et une période de maintenance de 12 semaines ultérieure où la dose de Fintepla est restée stable.
Dans l'étude, 3 99% des patients prenaient entre 1 et 4 AED concomitants. Les AED concomitants les plus fréquemment utilisés (chez au moins 25% des patients) étaient la lamotrigine (45%) (34%) et le valproate (56%).
Le critère d'évaluation de l'efficacité primaire dans l'étude 3 était le changement médian en pourcentage par rapport à la base de la fréquence des crises de baisse par 28 jours pendant les périodes de titrage et d'entretien combinées de 14 semaines (c'est-à-dire la période de traitement). La proportion de patients qui réalisent l'amélioration (minimale ou très améliorée) dans l'empreinte mondiale clinique du changement (CGI-I), comme évalué par l'investigateur principal, était un critère d'évaluation secondaire.
Dans l'étude 3, le changement médian en pourcentage par rapport à la ligne de base (réduction) de la fréquence des crises de baisse par 28 jours était significativement plus élevé pour le groupe de dose de 0,7 mg / kg / jour de fintepla par rapport au placebo (tableau 7). Une réduction des crises de baisse a été observée dans les 2 semaines suivant le début du traitement avec Fintepla et l'effet est resté généralement cohérent au cours de la période de traitement de 14 semaines.
La réduction médiane en pourcentage par rapport à la base de la fréquence des crises de baisse par 28 jours pour la dose plus faible de Fintepla (NULL,2 mg / kg / jour) n'a pas atteint une signification statistique par rapport au placebo (tableau 7).
Tableau 7: Changement de la fréquence des crises de chute pendant la période de traitement chez les patients avec le syndrome de Lennox-Gastaut (étude 3)
| Fréquence de crise de dépôt (par 28 jours) | Placebo | Fintepla 0,2 mg / kg / jour | Fintepla 0,7 mg / kg / jour |
| Étude 3 | N = 85 * | N = 86 * | N = 83 * |
| Médiane de la période de base Crise d'épilepsie Frequency | 55.0 | 77.8 | 80.0 |
| Changement médian en pourcentage par rapport à la référence pendant le traitement | -8,7% | -13,2% | -23,7% |
| valeur p par rapport au placebo | 0.1917 | 0.0037 | |
| * Le nombre total de patients sur lesquels l'analyse de l'efficacité était basée est inférieure au nombre total randomisé dans l'étude contrôlée par placebo en double aveugle car les patients avec des données manquants ont été exclus de l'analyse d'efficacité. |
La figure 4 présente le pourcentage de patients par catégorie de réduction par rapport à la base de la fréquence des crises de baisse par 28 jours pendant la période de traitement de l'étude 3.
Figure 4: Proportion de patients par catégorie de réponse de crise pour la fintepla et le placebo chez les patients atteints du syndrome de Lennox.Gastaut (étude 3)
| |
Des améliorations numériquement plus importantes sur le CGI-I par l'investigateur ont été observées chez les patients traités par Fintepla par rapport au placebo.
Informations sur les patients pour Fintepla
FinteplaR ®
(Fin-tep-la)
(fenfluramine) Solution orale
Lisez ce guide de médicaments avant de commencer à prendre Fintepla et chaque fois que vous obtenez une recharge. Il peut y avoir de nouvelles informations. Ces informations ne prennent pas la place de parler à votre fournisseur de soins de santé de votre état de santé ou de votre traitement.
Quelles sont les informations les plus importantes que je devrais connaître sur Fintepla?
Fintepla can cause serious side effects including :
1. Problèmes avec les valves dans le cœur (maladie cardiaque valvulaire) et l'hypertension artérielle dans les artères des poumons (hypertension artérielle pulmonaire) ont été associés à Fintepla. Votre fournisseur de soins de santé effectuera un test appelé un échocardiogramme pour vérifier votre cœur et pour l'hypertension artérielle dans les artères des poumons avant de recommencer à reprendre Fintepla tous les 6 mois pendant le traitement et une fois 3 à 6 mois après avoir pris votre dernière dose de Fintepla.
Appelez votre fournisseur de soins de santé immédiatement si vous développez l'un de ces signes et symptômes de problèmes cardiaques ou pulmonaires pendant le traitement avec Fintepla:
- essoufflement
- douleur thoracique
- fatigue ou faiblesse
- sensations d'un rythme cardiaque flottant
- en particulier avec une activité accrue (palpitations)
- étourdissement or évanouissement
- impulsion irrégulière
- chevilles ou pieds enflés
- Couleur bleuâtre à vos lèvres et à la peau (cyanose)
En raison du risque de problèmes de valve cardiaque (maladie cardiaque valvulaire) et de l'hypertension artérielle dans les artères des poumons (hypertension artérielle pulmonaire), la Fintepla n'est disponible que par le biais d'un programme restreint appelé programme Fintepla d'évaluation des risques et d'atténuation (REMS). Avant que vous ou votre enfant ne reçoive Fintepla, votre fournisseur de soins de santé ou pharmacien s'assurera de comprendre comment prendre Fintepla en toute sécurité. Si vous avez des questions sur Fintepla, demandez à votre fournisseur de soins de santé, visitez www.finteplalems.com ou appelez le 1-877-964-3649.
2. diminution de l'appétit et diminution du poids. Diminution de l'appétit et diminution du poids are both serious et common side effects of Fintepla in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Votre poids doit être vérifié régulièrement pendant votre traitement avec Fintepla.
- Votre fournisseur de soins de santé peut avoir besoin d'apporter des modifications à votre dose de fintepla si votre poids diminue. Dans certains cas, Fintepla peut devoir être arrêtée.
3. Somnolence Sédation et manque d'énergie (léthargie). Ce sont des effets secondaires à la fois graves et communs de la Fintepla chez les personnes atteintes du syndrome de Dravet (DS) ou du syndrome de Lennox-Gastaut (LGS). La prise de Fintepla avec des dépresseurs du système nerveux central (SNC), y compris l'alcool, peut augmenter la somnolence. Ne conduisez pas à faire fonctionner des machines lourdes ou faites d'autres activités dangereuses tant que vous ne savez pas comment Fintepla vous affecte.
4. Comme tous les autres médicaments antiépileptiques, Fintepla peut provoquer des pensées ou des actions suicidaires chez un très petit nombre de personnes (environ 1 sur 500).
Appelez votre professionnel de la santé immédiatement si vous avez l'un de ces symptômes, surtout s'ils sont nouveaux pires ou vous inquiétez:
- Réflexions sur le suicide ou la mort
- Anxiété nouvelle ou pire
- Diffusion de sommeil (insomnie)
- Agissant sur des impulsions dangereuses
- tente de se suicider
- Se sentir agité ou agité
- irritabilité nouvelle ou pire
- Une augmentation extrême de l'activité et de la parole (manie)
- Dépression nouvelle ou pire
- crises de panique
- Agir agressif étant en colère ou violent
- Autres changements inhabituels dans le comportement ou l'humeur
Comment puis-je surveiller les symptômes précoces des pensées et des actions suicidaires?
- Faites attention aux changements en particulier des changements soudains dans les pensées ou les sentiments des comportements d'humeur.
- Gardez toutes les visites de suivi avec votre fournisseur de soins de santé comme prévu.
Les pensées ou les actions suicidaires peuvent être causées par des choses autres que les médicaments. Si vous avez des pensées ou des actions suicidaires, votre fournisseur de soins de santé peut vérifier d'autres causes.
5. N'arrêtez pas de prendre Fintepla sans d'abord parler à votre fournisseur de soins de santé. L'arrêt d'une crise de crise comme Fintepla peut soudainement vous faire des crises plus souvent ou des crises qui ne s'arrêtent pas (Status Epilepticus).
Appelez votre fournisseur de soins de santé entre les visites au besoin, surtout si vous vous inquiétez des symptômes.
Qu'est-ce que Fintepla?
- Fintepla is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) et Lennox- Gastaut syndrome (LGS) in patients 2 years of age et older.
- On ne sait pas si Fintepla est sûre et efficace chez les enfants de moins de 2 ans.
Ne prenez pas Fintepla si vous:
- sont allergiques à la fenfluramine ou à l'un des ingrédients de Fintepla. Voir la fin de ce guide de médicaments pour une liste complète des ingrédients dans Fintepla.
- prennent ou ont cessé de prendre des médicaments appelés inhibiteurs de la monoamine oxydase (MAOI) au cours des 14 derniers jours. Cela peut provoquer un problème grave ou mortel appelé syndrome de la sérotonine. Si vous n'êtes pas sûr de savoir si vous prenez ou non l'un de ces médicaments, contactez votre fournisseur de soins de santé.
Avant de prendre Fintepla, dites à votre fournisseur de soins de santé de toutes vos conditions médicales, y compris si vous:
- avoir des problèmes cardiaques
- ont ou ont eu une perte de poids
- avoir ou avoir des problèmes d'humeur de dépression ou des pensées ou un comportement suicidaires
- avoir des problèmes rénaux
- avoir des problèmes de foie
- sont enceintes ou prévoient de devenir enceintes. Dites immédiatement votre professionnel de la santé si vous tombez enceinte en prenant Fintepla. Vous et votre fournisseur de soins de santé déciderez si vous devriez prendre Fintepla pendant que vous êtes enceinte.
- Si vous tombez enceinte en prenant Fintepla, parlez à votre fournisseur de soins de santé de l'inscription auprès du registre de grossesse antiépileptique nord-américain. Vous pouvez vous inscrire à ce registre en appelant le 1-888-233-2334 ou aller sur www.
- aedpregnancyregistry.org. Le but de ce registre est de collecter des informations sur la sécurité des médicaments antiépileptiques pendant la grossesse.
- allaitent ou prévoient d'allaiter. On ne sait pas si Fintepla passe dans votre lait maternel. Parlez à votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé tout en prenant Fintepla.
Parlez à votre fournisseur de soins de santé de tous les médicaments que vous prenez y compris les médicaments sur ordonnance et en vente libre des vitamines et des suppléments à base de plantes.
Connaissez les médicaments que vous prenez. Gardez une liste d'entre eux pour montrer votre fournisseur de soins de santé ou votre pharmacien lorsque vous obtenez un nouveau médicament.
Comment devrais-je prendre Fintepla?
- Lire le Instructions pour une utilisation À la fin de ce guide de médicaments pour des informations sur la bonne façon d'utiliser Fintepla.
- Prenez Fintepla exactement car votre fournisseur de soins de santé vous dit de le prendre.
- Votre fournisseur de soins de santé vous dira combien Fintepla prendre et quand le prendre.
- Fintepla may be taken with or without food.
- Mesurez votre dose de Fintepla à l'aide de la seringue de dosage fournie par la pharmacie. N'utilisez pas une cuillère à café ou une cuillère à soupe.
- Fintepla can be given through gastric et nasogastric feeding tubes
Que dois-je éviter en prenant Fintepla?
- Ne pas Conduisez des machines lourdes ou effectuez d'autres activités dangereuses jusqu'à ce que vous sachiez comment Fintepla vous affecte. Fintepla peut vous faire dormir.
Quels sont les effets secondaires possibles de Fintepla?
Fintepla may cause serious side effects including:
Appelez immédiatement votre fournisseur de soins de santé si vous présentez l'un des symptômes suivants du syndrome de la sérotonine.
- Voir «Quelles sont les informations les plus importantes que je devrais connaître sur Fintepla?
- sérotonine syndrome. Le syndrome de la sérotonine est un problème mortel qui peut se produire chez les personnes qui prennent Fintepla, surtout si Fintepla est prise avec certains autres médicaments pour inclure:
- Médicaments antidépresseurs appelés SSRIS SNRIS TCAS et MAOI
- Mur de St. Johns
- tryptophane
- dextrométhorphane
- lithium
- tramadol
- antipsychotiques
- Modifications de l'état mental telles que voir des choses qui ne sont pas là (hallucinations) l'agitation ou le coma
- rythme cardiaque rapide
- nausées vomissements diarrhée
- changements de tension artérielle
- Température corporelle élevée
- muscles serrés
- Problème de marche
- Hypertension artérielle (hypertension). L'hypertension est à la fois un effet secondaire grave et commun. Fintepla peut entraîner l'augmentation de votre tension artérielle même si vous n'avez jamais eu d'hypertension artérielle auparavant. Votre fournisseur de soins de santé vérifiera votre tension artérielle pendant que vous prenez Fintepla.
- une pression accrue dans votre œil (glaucome). Les symptômes du glaucome peuvent inclure:
- yeux rouges
- diminution de la vision
- voir des halos ou des couleurs vives autour des lumières
- douleur ou inconfort des yeux
- nausées ou vomissements
- vision floue
Si vous avez l'un de ces symptômes, appelez immédiatement votre fournisseur de soins de santé.
Les effets secondaires les plus courants de Fintepla lorsqu'ils sont utilisés pour traiter le syndrome de Dravet (DS) comprennent:
- diminution de l'appétit
- diarrhée
- faible énergie
- envie de dormir
- Problèmes d'équilibre des mouvements et de marche
- Agmentation de la bave
- infection respiratoire
- augmentation de la tension artérielle
- diminution du poids
- vomissement
- fièvre
- chute
- constipation
- convulsions qui ne s'arrêtent pas
- échocardiogramme anormal
- faiblesse
Les effets secondaires les plus courants de Fintepla lorsqu'ils sont utilisés pour traiter le syndrome de Lennox-Gastaut (LGS) comprennent:
- diarrhée
- fatigue
- vomissement
- envie de dormir
- diminution de l'appétit
Ce ne sont pas tous les effets secondaires possibles de Fintepla. Pour plus d'informations, demandez à votre fournisseur de soins de santé ou à votre pharmacien.
Dites à votre fournisseur de soins de santé si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Comment dois-je stocker Fintepla?
- Stocker la fintepla à température ambiante entre 68 ° F à 77 ° F (20 ° C et 25 ° C).
- Ne pas réfrigérer ou congeler.
- Conservez la bouteille et la seringue Fintepla dans une zone propre.
- Jeter (rejeter) toute fintepla inutilisée 3 mois après l'ouverture de la bouteille ou si le défausse après la date du colis ou de la bouteille s'est écoulé. Quel que soit le premier.
Gardez Fintepla et tous les médicaments hors de portée des enfants.
Informations générales sur l'utilisation sûre et efficace de Fintepla.
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide de médicaments. N'utilisez pas Fintepla pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas de fintepla à d'autres personnes même si elles présentent les mêmes symptômes que vous. Cela peut leur faire du mal.
Vous pouvez demander à votre pharmacien ou fournisseur de soins de santé pour des informations sur Fintepla qui sont écrits pour les professionnels de la santé.
Quels sont les ingrédients de Fintepla?
Ingrédient actif: chlorhydrate de fenfluramine
Ingrédients inactifs: Flavour des cerises Acide citrique éthylparabène Hydroxyéthylcellulose méthylparaben potassium Citrate sucralose et eau.
Fintepla contains no ingredient made from gluten-containing grain (wheat barley or rye) et contains not more than 0.1% of glucides qui provient de l'arôme de cerise.
Ce guide de médicaments a été approuvé par la Food and Drug Administration des États-Unis.
Instructions pour une utilisation
Fintepla ®
(Fin-tep-la)
(fenfluramine) Solution orale 2.2 mg/mL
Assurez-vous que vous lisez comprendre et suivez ces instructions avant de commencer à utiliser la solution orale Fintepla et chaque fois que vous obtenez une recharge. Il peut y avoir de nouvelles informations.
Ces instructions d'utilisation contient des informations sur la façon de prendre Fintepla. Ces informations ne prennent pas la place de parler à votre fournisseur de soins de santé de votre état de santé ou de votre traitement.
Qu'est-ce qui est inclus avec Fintepla?
Les articles suivants sont inclus pour préparer et donner une dose orale de Fintepla:
- 1 bouteille de solution orale de fintepla (NULL,2 mg / ml)
- 2 seringues orales réutilisables
| |
Appelez le pharmacien au 1-844-288-5007 si vous n'avez pas reçu les éléments énumérés ci-dessus ou si vous avez besoin d'aide en les utilisant.
Informations importantes sur Fintepla
- Fintepla is an oral medicine (taken by mouth) et is given 2 fois tous les jours . Suivez les instructions de vos prestataires de soins de santé pour prendre ou donner des doses de Fintepla.
- Si vous avez des questions sur la façon de préparer ou de donner Fintepla, contactez votre fournisseur de soins de santé ou appelez votre pharmacien.
- Utilisez toujours les seringues orales fournies avec Fintepla pour vous assurer que la bonne dose est donnée. Si vous avez besoin d'une nouvelle seringue, contactez votre pharmacien. Ne pas Utilisez une cuillère à café de ménage ou une cuillère à soupe.
Seringues orales fournies par la pharmacie.
Avec Fintepla, vous recevrez 2 seringues orales réutilisables.
2 seringues orales qui peuvent mesurer jusqu'à 3 ml
OU
2 seringues orales qui peuvent mesurer jusqu'à 6 ml
| |
Appelez le pharmacien au 1-844-288-5007 si vous avez des questions sur les seringues fournies avec Fintepla.
Parties de la seringue orale
| |
Préparer une dose
Étape 1 . Assurez-vous d'avoir:
- La bouteille de solution orale Fintepla et
- Une seringue orale réutilisable à sec propre qui a été fournie avec Fintepla.
Étape 2. Vérifiez la défausse après la date (mm / dd / yyyy).
| |
- Ne pas Utilisez le médicament si la date de lancer (défausse) est passée.
- Si la date est proche de contacter votre pharmacie ou votre fournisseur de soins de santé pour obtenir une recharge ou une nouvelle ordonnance.
- Si la date a été adoptée à disposer de toute fintepla inutilisée.
Étape 3. Appuyez vers le bas et tournez le capuchon à l'épreuve des enfants vers la gauche (dans le sens antihoraire) et retirez-le de la bouteille.
- Mettez le capuchon de côté (ne jetez pas).
| |
Étape 4. Assurez-vous que l'adaptateur est sur la bouteille.
- Si la bouteille n'a pas d'adaptateur, contactez le pharmacien.
- Laissez toujours l'adaptateur en place dans la bouteille de médecine.
| |
Étape 5. Retirez une seringue orale de son emballage si nécessaire.
Utilisez uniquement les seringues orales fournies avec Fintepla.
Si une seringue orale est endommagée ou si vous ne pouvez pas lire les marques de dose:
- Utilisez l'autre seringue orale fournie ou
- Contactez le pharmacien pour en obtenir un nouveau.
| |
Étape 6. Assurez-vous que le piston est poussé tout le long de la seringue orale.
| |
Étape 7. Tenez fermement la bouteille de médicaments sur une surface plate dure.
Étape 8. Poussez la pointe de la seringue orale dans l'ouverture de l'adaptateur jusqu'à ce qu'elle ne puisse pas être poussée plus loin.
| |
Étape 9. Tenez la seringue orale et le bouteille ensemble et retournez.
| |
Étape 10. Tirez lentement le piston de la seringue orale pour retirer la dose prescrite.
| |
| |
| |
Préparer une dose (suite)
Étape 11. Alignez l'extrémité du piston avec la marque pour la dose prescrite sur la seringue orale.
Conseils pour obtenir la bonne dose
- Si vous tirez trop de médicaments:
- Laissez la seringue orale dans l'adaptateur.
- Repousser lentement le piston dans la seringue jusqu'à ce que vous atteigniez la dose prescrite.
- Si vous voyez des bulles d'air dans le médicament:
- Laissez la seringue orale dans l'adaptateur.
- Tirez le piston plus bas vers le bas.
- Permettez aux bulles de monter à la pointe de la seringue.
- Poussez le piston dans tout le chemin.
- Tirez lentement le piston vers la dose prescrite.
Note: De très petites bulles dans le liquide sont normales.
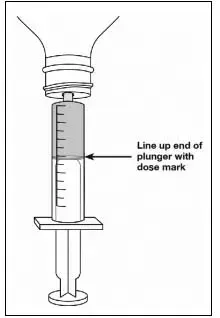
Étape 12. Tenez la seringue orale et la bouteille ensemble, puis tournez la bouteille à droite.
| |
Étape 13. Tenir la bouteille fermement retirer doucement la seringue orale de l'adaptateur de bouteille.
| |
Étape 14. Assurez-vous que la dose dans la seringue orale correspond toujours à la dose prescrite.
Si la dose ne correspond pas:
- Remettez la seringue dans l'adaptateur.
- Voir les étapes 9 à 11 pour ajuster la dose au besoin.
Donner Fintepla
Étape 15. Placez la pointe de la seringue orale contre l'intérieur de la joue.
Étape 16. Poussez doucement le piston jusqu'à ce que tous les médicaments de la seringue orale soient donnés.
| |
- Ne pas Magir ou pousser avec force le médicament à l'arrière de la gorge. Cela peut provoquer un étouffement.
Étape 17. Placez le bouchon en arrière sur la bouteille en tournant le bouchon à droite (dans le sens des aiguilles d'une montre) jusqu'à ce qu'il s'arrête.
- Laissez toujours l'adaptateur en place in the bottle
- Le capuchon s'adaptera dessus.
| |
Nettoyer la seringue
- Rincez la seringue orale à l'eau du robinet propre et laissez-la sécher à l'air après chaque utilisation.
- Assurez-vous de rincer l'intérieur de la seringue et du piston.
Conseils de nettoyage:
- Tirez l'eau du robinet propre dans la seringue avec le piston et poussez-la plusieurs fois pour nettoyer la seringue.
- Retirez le piston du baril de la seringue orale
- Rincer les deux pièces sous l'eau du robinet
- Assurez-vous que la seringue et le piston sont complètement secs avant la prochaine utilisation.
- La seringue est également sûre à nettoyer dans le lave-vaisselle.
| |
Comment dois-je stocker Fintepla?
- Conservez la fintepla à température ambiante entre 68 ° F à 77 ° F (20 ° C à 25 ° C).
- Ne pas réfrigérer ou congeler.
- Gardez le bouchon bien fermé et la bouteille debout.
- Conservez la bouteille et la seringue Fintepla dans une zone propre.
- Jeter (rejeter) toute fintepla inutilisée 3 mois après l'ouverture de la bouteille ou si le défausse après la date du colis ou de la bouteille s'est écoulé. Quel que soit le premier.
- Gardez Fintepla et tous les médicaments hors de portée des enfants.
Ces instructions pour une utilisation ont été approuvées par la Food and Drug Administration des États-Unis.
