Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
ProgestatifsKyleena
Résumé
Qu'est-ce que Kyleena?
Kyleena (système intra-utérin à libération de lévonorgestrel) est un système intra-utérine contenant des progestatifs (IU) indiqué pour la prévention de la grossesse jusqu'à 5 ans.
Quels sont les effets secondaires de Kyleena?
Kyleena peut provoquer des effets secondaires graves, notamment:
- Augmentation des saignements vaginaux
- Douleurs abdominales ou douleurs pelviennes
- devise expulsion
- acné et
- crampes menstruelles
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires courants de Kyleena comprennent:
- démangeaisons vaginales et décharge
- kystes ovariens
- douleurs abdominales
- douleur pelvienne
- Maux de tête ou migraine
- acné
- crampes abdominales
- Douleur ou inconfort du sein
- Augmentation des saignements vaginaux
- dépression et
- perte de cheveux.
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; et des étourdissements soudains étourdisseurs ou s'évanouissant;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Kyleena
Kyleena est insérée par un fournisseur de soins de santé formé. Le taux de libération de Levonorgestrel (GNL) à Kyleena est de 17,5 mcg / jour après 24 jours et diminue à 7,4 mcg / jour après 5 ans; Kyleena doit être retirée ou remplacée après 5 ans.
Combien de norcos pour devenir haut
Quelles substances ou suppléments de médicaments interagissent avec Kyleena?
Kyleena peut interagir avec d'autres médicaments. Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Kyleena pendant la grossesse et l'allaitement
Dites à votre médecin si vous êtes enceinte avant d'utiliser Kyleena. Kyleena n'est pas recommandée pour une utilisation pendant la grossesse. Kyleena doit être enlevée si la grossesse se produit avec Kyleena en place. Consultez votre médecin avant l'allaitement.
Informations Complémentaires
Notre centre de médicaments à effets secondaires de Kyleena (Système intra-utérin de libération de lévonorgestrel) offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
Description de Kyleena
Kyleena (système intra-utérin libérant par levonorgestrel) contient 19,5 mg de GNL par progestatif et est destiné à fournir un taux de libération initial d'environ 17,5 mcg / jour de GNL après 24 jours.
Levonorgestrel USP (-) - 13-éthyl-17-hydroxy-1819-Dinor-17α-Pregn-4-EN-20-AN-3-one L'ingrédient actif de Kyleena a un poids moléculaire de 312,4 une formule moléculaire de C de C de C 21 H 28 O 2 et la formule structurelle suivante:
 |
Kyleena
Kyleena consists of a T-shaped polyethylene frame (T-body) with a steroid reservoir (hormone elastomer core) around the vertical stem. The white T-body has a loop at one end of the vertical stem et two horizontal arms at the other end. The reservoir consists of a whitish or pale yellow cylinder made of a mixture of LNG et silicone (polydimethylsiloxane) containing a total of 19.5 mg LNG. The reservoir is covered by a semi-opaque silicone membrane composed of polydimethylsiloxane et colloidal silica. A ring composed of 99.95% pure silver is located at the top of the vertical stem close to the horizontal arms et is visible by ultrasound. The polyethylene of the T-body is compounded with barium sulfate which makes it radiopaque. A monofilament blue polypropylene removal thread is attached to a loop at the end of the vertical stem of the T-body. The polypropylene of the removal thread contains <0.5% phthalocyaninato(2-) copper as a colorant (see Figure 10).
Les composants de Kyleena, y compris ses emballages, ne sont pas fabriqués à l'aide de latex en caoutchouc naturel.
Figure 10: Kyleena
 |
Inserter
Kyleena is packaged sterile within an inserter. The inserter (Figure 11) which is used for insertion of Kyleena into the uterine cavity consists of a symmetric two-sided body et slider that are integrated with flange lock pre-bent insertion tube et plunger. The outer diameter of the insertion tube is 3.8 mm. The vertical stem of Kyleena is loaded in the insertion tube at the tip of the inserter. The arms are pre-aligned in the horizontal position. The removal threads are contained within the insertion tube et hetle. Once Kyleena has been placed the inserter is discarded.
Figure 11: Diagramme de l'inserteur
 |
Utilisations pour Kyleena
Kyleena is indicated to prevent pregnancy for up to 5 years. Replace the system after 5 years if continued use is desired.
Dosage pour Kyleena
Dosing au fil du temps
Kyleena contains 19.5 mg of lévonorgestrel (LNG) released en vain À un taux d'environ 17,5 mcg / jour après 24 jours. Ce taux diminue progressivement à 9,8 mcg / jour après 1 an et à 7,4 mcg / jour après 5 ans. La moyenne en vain Le taux de libération du GNL est d'environ 12,6 mcg / jour au cours de la première année et 9,0 mcg / jour sur une période de 5 ans. [Voir Pharmacologie clinique ]
Kyleena must be removed by the end of the fifth year et can be replaced at the time of removal with a new Kyleena if continued contraceptive protection is desired.
Kyleena can be physically distinguished from other intrauterine systems (IUSs) by the combination of the visibility of the silver ring on ultrasound et the blue color of the removal threads.
Kyleena is supplied in a sterile package within an inserter that enables single-heted loading (see Figure 1). Do not open the package until required for insertion [see DESCRIPTION ]. N'utilisez pas si le sceau de l'ensemble stérile est cassé ou semble compromis. Utilisez des techniques aseptiques strictes tout au long de la procédure d'insertion [voir Avertissements et précautions ].
 |
Instructions d'insertion
- Obtenez des antécédents médicaux et sociaux complets pour déterminer les conditions qui pourraient influencer la sélection d'un système intra-utérin libérant par levonorgestrel (LNG IUS) pour la contraception. Si indiqué, effectuez un examen physique et des tests appropriés pour toutes les formes d'infections génitales ou autres transmissions sexuelles. [Voir Contre-indications et Avertissements et précautions ] Parce que les saignements / taches irréguliers sont courants au cours des premiers mois d'utilisation de Kyleena, excluez la pathologie de l'endomètre (polypes ou cancer) avant l'insertion de Kyleena chez les femmes avec des saignements persistants ou inhabituels [voir [voir Avertissements et précautions ].
- Suivez les instructions d'insertion exactement comme décrit pour assurer un placement approprié et éviter la libération prématurée de Kyleena de l'inserteur. Une fois libéré, Kyleena ne peut pas être rechargée.
- Vérifier la date d'expiration de Kyleena avant de lancer l'insertion.
- Kyleena should be inserted by a trained healthcare provider. Healthcare providers should become thoroughly familiar with the insertion instructions before attempting insertion of Kyleena.
- L'insertion peut être associée à certaines douleurs et / ou des saignements ou des réactions vasovagales (par exemple la syncope bradycardie) ou avec des crises en particulier chez les patients présentant une prédisposition à ces conditions. Envisagez d'administrer des analgésiques avant l'insertion.
Timing de l'insertion
Tableau 1: Quand insérer Kyleena
| Démarrage de Kyleena chez les femmes qui n'utilisent pas actuellement la contraception hormonale ou intra-utérine |
|
| Passer à Kyleena d'un contraceptif hormonal transdermique oral |
|
| Passant à Kyleena à partir d'un contraceptif progestatif injectable |
|
| Passer à Kyleena à partir d'un implant contraceptif ou d'un autre ius |
|
| Insertion de Kyleena après l'avortement ou la fausse couche du premier trimestre |
|
| Insertion de Kyleena après l'accouchement ou un avortement ou une fausse couche au deuxième trimestre | |
|
|
| Insertion d'intervalle suite à une involution complète de l'utérus |
|
Outils pour l'insertion
Note
L'inserteur fourni avec Kyleena (voir figure 1) et la procédure d'insertion décrite dans cette section ne sont pas applicables à l'insertion immédiate après un avortement ou une fausse couche au deuxième trimestre. Pour l'insertion immédiate, supprimez Kyleena de l'inserteur par premier chargement (voir figure 2), puis libérant (voir figure 7) Kyleena de l'inserteur et insérer en fonction de la pratique acceptée.
Préparation
- Gants
- Spéculum
- Son utérin stérile
- Tenaculum stérile
- Applicateur de solution antiseptique
Procédure
- Gants stériles
- Kyleena with inserter in sealed package
- Instruments et anesthésie pour bloc paraacervical si prévu
- Envisagez d'avoir une Kyleena de secours non ouverte disponible
- Ciseaux incurvés aigus stériles
Préparation for insertion
- Excluez la grossesse et confirmez qu'il n'y a pas d'autres contre-indications à l'utilisation de Kyleena.
- Avec le patient confortablement en position de lithotomie, faites un examen bimanuel pour établir la forme et la position de l'utérus.
- Insérez doucement un spéculum pour visualiser le col de l'utérus.
- Nettoyez soigneusement le col de l'utérus et le vagin avec une solution antiseptique appropriée.
- Préparez-vous à sonner la cavité utérine. Saisissez la lèvre supérieure du col de l'utérus avec une pince de tenaculum et appliquez doucement la traction pour stabiliser et aligner le canal cervical avec la cavité utérine. Effectuez un bloc paracervical si nécessaire. Si l'utérus est rétroverti, il peut être plus approprié de saisir la lèvre inférieure du col de l'utérus. Le Tenaculum doit rester en position et une douce traction sur le col doit être maintenue tout au long de la procédure d'insertion.
- Insérez doucement un son utérin pour vérifier la perméabilité du col de l'utérus, la profondeur de la cavité utérine dans les centimètres confirme la direction de la cavité et détecte la présence de toute anomalie utérine. Si vous rencontrez des difficultés ou une sténose cervicale, utilisez une dilatation et non la force pour surmonter la résistance. Si une dilatation cervicale est requise, envisagez d'utiliser un bloc paracervical.
Procédure d'insertion
Procéder avec l'insertion uniquement après avoir terminé les étapes ci-dessus et vérifier que le patient est approprié pour Kyleena.
Assurez l'utilisation de la technique aseptique tout au long de la procédure.
Étape 1-ouvrage du package
Figure 1. Ouverture du package Kyleena
 |
- Ouvrez le package (figure 1). Le contenu de l'emballage est stérile.
- À l'aide de gants stériles, soulevez la poignée de l'inserteur stérile et retirez de l'emballage stérile.
Étape 2 - chargez Kyleena dans le tube d'insertion
Figure 2. Déplacez le curseur jusqu'à la position avant pour charger Kyleena
 |
- Pousser le curseur avant Dans la mesure du possible dans le sens de la flèche, déplace ainsi le tube d'insertion sur le kyleena t-corps pour charger Kyleena dans le tube d'insertion (figure 2). Les pointes des bras se réuniront pour former une extrémité arrondie qui s'étend légèrement au-delà du tube d'insertion.
- Maintenez la pression vers l'avant avec votre pouce ou votre index sur le curseur. Ne déplacez pas le curseur vers le bas pour le moment car cela peut libérer prématurément les fils de Kyleena. Une fois que le curseur est déplacé en dessous du Mark, Kyleena ne peut pas être rééchargé.
Étape 3 - Pétablissement de la bride
- En tenant le curseur dans cette position vers l'avant, le bord supérieur de la bride correspondait à la profondeur utérine (en centimètres) mesurée pendant le son (figure 3).
Figure 3. Réglage de la bride
 |
Étape 4 - Kyleena est maintenant prête à être insérée
- Continuez à tenir le curseur dans cette position à terme. Avancez l'inserteur à travers le col de l'utérus jusqu'à ce que la bride soit à environ 1,5 à 2 cm du col de l'utérus, puis s'arrêtez (figure 4).
Figure 4. Avocation du tube d'insertion jusqu'à ce que la bride soit de 1,5 à 2 cm du col de l'utérus
 |
Ne forcez pas l'inserteur. Si nécessaire, dilatez le canal cervical.
Étape 5 - Open des bras
- Tout en maintenant l'inserteur stable Déplacez le curseur vers le bas pour libérer les bras de Kyleena (figure 5). Attendez 10 secondes pour que les bras horizontaux s'ouvrent complètement.
Figure 5. Remplacez le curseur vers la marque pour libérer et ouvrez les bras
 |
Étape 6 - Advance à la position fondamentale
Avancez doucement l'inserteur vers le fond de l'utérus Jusqu'à ce que la bride touche le col de l'utérus. Si vous rencontrez une résistance fondamentale, ne continuez pas à avancer. Kyleena est maintenant en position fondamentale (figure 6). Le positionnement final de Kyleena est important pour prévenir l'expulsion.
Figure 6. Déplacez Kyleena en position fondamentale
 |
Étape 7 - Reliez Kyleena et retirez l'inserteur
Figure 7. Déplacez le curseur tout le long pour libérer Kyleena du tube d'insertion
 |
Figure 8. Couper les fils
 |
- Tenant l'inservateur entier fermement en place libére Kyleena en déménageant le curseur tout le long (Figure 7).
- Continuez à maintenir le curseur tout au long du chemin pendant que vous retirez lentement et doucement l'inserter de l'utérus.
- À l'aide d'un ciseaux courbes pointus, coupez les fils Perpendiculaire en laissant environ 3 cm visibles à l'extérieur du col de l'utérus [les fils de coupe à un angle peuvent laisser des extrémités nettes (figure 8)]. N'appliquez pas la tension ou ne tirez pas sur les filetages lors de la coupe pour éviter le déplacement de Kyleena.
Kyleena insertion is now complete. Prescribe analgesics if indicated. Record the Kyleena lot number in the patient records.
Informations importantes à considérer pendant ou après l'insertion
- Si vous soupçonnez que Kyleena n'est pas dans le placement de vérification de position correcte (par exemple en utilisant l'échographie transvaginale). Retirez Kyleena s'il n'est pas complètement positionné dans l'utérus. Ne réinsérez pas une Kyleena retirée.
- S'il existe une préoccupation clinique exceptionnelle de douleur ou de saignement pendant ou après l'insertion, prenez immédiatement des mesures (telles que l'examen physique et l'échographie) pour exclure la perforation.
Suivi du patient
- Réexaminez et évaluez les patients 4 à 6 semaines après l'insertion et une fois par an par la suite ou plus fréquemment si vous êtes cliniquement indiqué.
Retrait de Kyleena
Timing de la suppression
- Kyleena should not remain in the uterus after 5 years.
- Si la grossesse n'est pas souhaitée, supprimez Kyleena pendant les 7 premiers jours du cycle menstruel à condition que la femme éprouve toujours des règles régulières. Si le déménagement se produira à d'autres moments pendant le cycle ou si la femme ne ressent pas de règles régulières, elle risque de se faire une grossesse; Commencez une nouvelle méthode contraceptive une semaine avant le retrait de ces femmes. [Voir Continuation de la contraception après le retrait ]
Outils pour la suppression
Préparation
- Gants
- Spéculum
Procédure
- Pince stérile
Procédure de suppression
Figure 9. Retrait de Kyleena
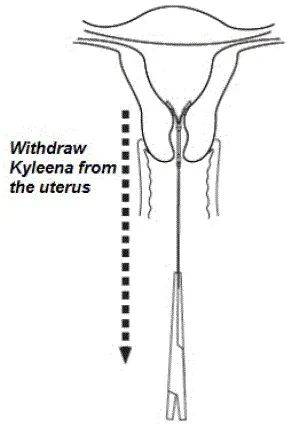
- Retirez Kyleena en appliquant une traction douce sur les fils avec des pinces (figure 9).
- Si les fils ne sont pas visibles, déterminez l'emplacement de Kyleena par échographie [voir Avertissements et précautions ].
- Si Kyleena se trouve dans la cavité utérine à l'examen échographique, elle peut être supprimée à l'aide d'une pince étroite telle qu'une pince d'alligator. Cela peut nécessiter une dilatation du canal cervical. Après le retrait de Kyleena, examinez le système pour s'assurer qu'il est intact.
- Si vous ne pouvez pas éliminer avec une traction douce, déterminez l'emplacement de Kyleena et excluez la perforation par échographie ou autre imagerie [voir Avertissements et précautions ].
- Le retrait peut être associé à certains:
- Douleur et / ou saignement ou réactions vasovagales (par exemple la bradycardie syncope) ou la saisie, en particulier chez les patients présentant une prédisposition à ces conditions.
- rupture ou intégration de kyleena dans le myomètre qui peut rendre le retrait difficile [voir Avertissements et précautions ]. Analgesia paracervical anesthesia cervical dilation alligator forceps or other grasping instrument or hysteroscopy may be used to assist in removal.
Continuation de la contraception après le retrait
- Si la grossesse n'est pas souhaitée et si une femme souhaite continuer à utiliser Kyleena, un nouveau système peut être inséré immédiatement après le retrait à tout moment pendant le cycle.
- Si un patient avec des cycles réguliers veut démarrer une autre méthode contraceptive l'élimination du temps et l'initiation de la nouvelle méthode pour assurer une contraception continue. Soit supprimer Kyleena pendant les 7 premiers jours du cycle menstruel et démarrer la nouvelle méthode immédiatement après, soit démarrer la nouvelle méthode au moins 7 jours avant d'éliminer Kyleena si le retrait doit se produire à d'autres moments pendant le cycle.
- Si un patient atteint de cycles irréguliers ou d'aménorrhée veut démarrer une méthode contraceptive différente, commencez la nouvelle méthode au moins 7 jours avant le retrait.
Comment fourni
Formes et forces posologiques
Kyleena est un IUS libérant du GNL (un type de dispositif intra-utérine ou DIU) composé d'un cadre en polyéthylène en forme de T avec un réservoir de stéroïdes contenant un total de 19,5 mg de GNL.
Stockage et manipulation
Kyleena (Système intra-utérine de libération de lévonorgestrel) contenant un total de 19,5 mg de GNL est disponible dans un carton d'une unité stérile - NDC
Kyleena is supplied sterile. Kyleena is sterilized with ethylene oxide. Do not resterilize. For single use only. Do not use if the inner package is damaged or open. Insert before the end of the month shown on the label.
Stocker à 25 ° C (77 ° F); avec des excursions autorisées entre 15 et 30 ° C (59–86 ° F) [voir la température ambiante contrôlée par l'USP].
Fabriqué pour: Bayer Healthcare Pharmaceuticals Inc. Whippany NJ 07981. Révisé: mars 2023
Effets secondaires pour Kyleena
Les réactions indésirables graves ou autrement importantes sont discutées ailleurs dans l'étiquetage:
- Grossesse extra-utérine [voir Avertissements et précautions ]
- Grossesse intra-utérine [voir Avertissements et précautions ]
- Groupe A Sepsis streptococcique (gaz) [Voir Avertissements et précautions ]
- Maladie inflammatoire pelvienne [voir Avertissements et précautions ]
- Perforation [voir Avertissements et précautions ]
- Expulsion [voir Avertissements et précautions ]
- Kystes ovariens [voir Avertissements et précautions ]
- Altérations de saignement [voir Avertissements et précautions ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions de réaction indésirables très variables observées dans les essais cliniques d'un médicament ne peuvent pas être directement comparées aux taux dans les essais cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique clinique.
Les données décrites ci-dessous reflètent l'exposition de 1697 en bonne santé de 18 à 41 ans (âge moyen de 27,8 ± 5,2 ans) à Kyleena. Ces données proviennent de deux essais contraceptifs multicentriques: une étude de phase 2 avec une durée de 3 ans a été menée en Europe, inscrivant des femmes généralement en bonne santé de 21 à 41 ans; 217 sujets ont été exposés à Kyleena pendant un an et 174 ont achevé trois ans. Les données de cet essai couvrent environ 8 000 cycles d'exposition. Une étude de phase 3 avec une durée de 3 ans et une extension facultative de l'utilisation de Kyleena jusqu'à 5 ans ont été menées aux États-Unis (États-Unis) Canada Europe et en Amérique latine. La population était généralement en bonne santé de 18 à 35 ans. Au total, 1208 sujets ont été exposés à Kyleena pendant au moins un an; 707 femmes sont entrées dans la phase d'extension en option après 3 ans et 550 ont terminé cinq ans. Les données de cet essai couvrent environ 60000 cycles.
Au total, pour les deux études, 1425 sujets ont été exposés pendant au moins 1 an et 550 sujets terminés 5 ans d'utilisation. Sur le total de 1697, les sujets exposés à Kyleena 563 étaient des États-Unis et 1134 étaient d'Europe Canada et d'Amérique latine; 623 (37%) étaient nullipares (âge moyen de 24,6 ± 4,5 ans) et 1074 (63%) étaient parole (âge moyen 29,7 ± 4,7 ans). La plupart des femmes qui ont reçu Kyleena étaient du race blanche (83%) ou noires / afro-américaines (NULL,4%); 9,4% des femmes étaient une ethnie hispanique. Les essais cliniques n'avaient aucune limite de poids supérieur ou de masse corporelle (IMC). L'IMC moyen des sujets de Kyleena était de 25,2 kg / m 2 (Gamme 15,2 - 57,6 kg / m 2 )); 16% avaient un IMC ≥ 30 kg / m 2 et 2.0% had a BMI ≥ 40 kg/m 2 . Les fréquences des effets indésirables signalés représentent des incidences brutes.
Les réactions indésirables les plus courantes (survenant chez ≥ 5% d'utilisateurs) étaient la vulvovaginite (24%) kyste ovarien (22%) Douleurs abdominales / douleurs pelviennes (21%) maux de tête / migraine (15%) acné / séborrhée (15%) dysménorrhée / spasme utérin (8%).
Dans les études combinées, 22% ont arrêté prématurément en raison d'une réaction indésirable. Les réactions indésirables les plus courantes (> 1%) conduisant à l'arrêt ont augmenté les saignements (NULL,5%) de la douleur abdominale / douleur pelvienne (NULL,2%) expulsion de dispositif (NULL,1%) acné / séborrhée (NULL,3%) et dysménorrhée / spasme utérin (NULL,3%).
Les effets indésirables courants (survenant chez ≥ 1% d'utilisateurs) sont résumés dans le tableau 4 (présenté comme des incidents bruts).
Tableau 4: Réactions indésirables qui se sont produites chez au moins 1% des utilisateurs de Kyleena dans les essais cliniques par la classe d'organes du système (SOC)
| Classe d'organes système | Réaction indésirable | Incidence (%) (N = 1697) |
| Système reproductif et troubles mammaires | Vulvovaginite | 24.3 |
| Kyste ovarien a | 22.2 | |
| Dysménorrhée / spasme utérine | 8.0 / 2.4 | |
| Augmentation des saignements b | 7.9 | |
| Douleur / inconfort du sein | 7.1 / 3.5 | |
| Libération génitale | 4.5 | |
| Expulsion des appareils (complet et partiel) | 3.5 | |
| Infection des voies génitales supérieures | 1.5 | |
| Troubles gastro-intestinaux | Douleur abdominale / douleur pelvienne | 13.3 / 8.2 |
| Nausée | 4.7 | |
| Troubles de la peau et des tissus sous-cutanés | Acné / séborrhée | 14.1 / 1.8 |
| Alopécie | 1.0 | |
| Troubles du système nerveux | Maux de tête / migraine | 12.9 / 3.3 |
| Troubles psychiatriques | Dépression / humeur déprimée | 4.4 / 0,2 |
| a Les kystes ovariens ont été signalés comme des événements indésirables s'ils étaient des kystes anormaux non fonctionnels et / ou avaient un diamètre> 3 cm à l'échographie b Toutes les modifications de saignement n'ont pas été capturées comme des réactions indésirables [voir Avertissements et précautions ]. |
Dans les essais cliniques, de graves effets indésirables se produisant dans plus d'un seul sujet comprenaient: la grossesse extra-utérine / la grossesse extra-utérine rompue (10 sujets); maladie inflammatoire pelvienne (6 sujets); avortement manqué / avortement spontané incomplet / avortement spontané (4 sujets); kyste ovarien (3 sujets); douleurs abdominales (4 sujets); Dépression / trouble affectif (4 sujets); et le dispositif de perforation utérine / intégrée (perforation myométriale) (3 sujets).
Expérience de commercialisation /
Réaction indésirables From Postmarketing Spontaneous Reports
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de l'IUSS libérant du GNL. Étant donné que ces réactions sont rapportées volontairement d'une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à l'exposition au médicament.
- Événements thromboemboliques thrombotiques et veineux et veineux, y compris les cas d'embolie pulmonaire, la thrombose veineuse profonde et l'AVC
- Rupture de l'appareil
- Hypersensibilité (y compris l'urticaire éruption
- Augmentation de la tension artérielle
Signalé des réactions indésirables des études post-commercialisation
Évaluation de la perforation et de l'expulsion de l'étude des dispositifs intra-utérins (APEX DIU)
Apex DIU était une grande étude de cohorte rétrospective américaine pour évaluer l'impact de l'allaitement maternel et du calendrier de l'insertion du DIU post-partum sur la perforation utérine et l'expulsion du DIU. Les analyses comprenaient un total de 326658 insertions de 30% (97824 insertions) qui ont été effectuées chez les femmes avec une livraison au cours des 12 mois précédents. Pour les insertions effectuées chez les femmes qui avaient livré ≤ 52 semaines avant l'insertion du DIU, la majorité des insertions post-partum 57,3% (56047 insertions) ont eu lieu entre 6 et 14 semaines après le post-partum. Les données de l'allaitement maternel étaient disponibles dans 94817 insertions effectuées chez les femmes 52 semaines ou moins après l'accouchement.
Les résultats de l'étude ont indiqué que le risque de perforation utérine était le plus élevé chez les femmes atteintes d'insertion du DIU ≤ 6 semaines après l'accouchement. Les résultats immédiats de l'insertion post-partum (0 à 3 jours) sont limités en raison du nombre relativement faible d'insertions se produisant dans cet intervalle de temps. Les femmes qui allaitent au moment de l'insertion étaient à 33% de risque de perforation (rapport de risque ajusté [HR] = 1,33 intervalle de confiance à 95% [IC]: 1,07–1,64) par rapport aux femmes qui n'allaitement pas au moment de l'insertion. Un risque progressivement plus faible de perforation utérine a été observé dans les fenêtres de temps post-partum au-delà de 6 semaines chez les femmes allaitées et non allaitées. Le tableau 5 présente les taux de perforation utérins pour le GNL Stratified par statut d'allaitement et intervalle post-partum.
Tableau 5: perforation utérine 1 tarifs pour les ius de GNL par statut d'allaitement et intervalle post-partum
| Allaitement au moment de l'insertion | Ne pas allaiter au moment de l'insertion | |||
| Intervalle post-partum au moment de l'insertion | Nombre d'événements / insertions | Taux de perforation utérine pour 1000 insertions | Nombre d'événements / insertions | Taux de perforation utérine pour 1000 insertions |
| 0 à 3 jours | 8/1896 | 4.22 | 0/277 | 0.00 |
| 4 jours à ≤ 6 semaines | 120/10735 | 11.18 | 28/2377 | 11.78 |
| > 6 à ≤ 14 semaines | 268/29677 | 9.03 | 30/32011 | 6.66 |
| > 14 à ≤ 52 semaines | 43/6139 | 7.00 | 22/9089 | 2.42 |
| > 52 semaines ou pas de livraison | Aucune donnée disponible | 243/184733 | 1.32 | |
| 1 La perforation utérine comprend une perforation complète et partielle |
Le risque d'expulsion était variable sur les intervalles post-partum pendant 52 semaines. Les femmes qui allaitent étaient à 28% un risque plus faible d'expulsion du DIU (HR ajustée = 0,72 IC à 95%: 0,64-0,80) par rapport aux femmes qui n'allaitement pas au moment de l'insertion. Le tableau 6 présente les taux d'expulsion du DIU pour les IU GNL stratifiés par statut d'allaitement et intervalle post-partum.
Tableau 6: Expulsion 1 Tarifs pour les ius de GNL par statut d'allaitement et intervalle post-partum
| Allaitement au moment de l'insertion | Ne pas allaiter au moment de l'insertion | |||
| Intervalle post-partum au moment de l'insertion | Nombre d'événements / insertions | Taux d'expulsion pour 1000 insertions | Nombre d'événements / insertions | Taux d'expulsion pour 1000 insertions |
| 0 à 3 jours | 187/1896 | 98.63 | 12/277 | 43.32 |
| 4 jours à ≤ 6 semaines | 185/10735 | 17.23 | 52/2377 | 21.88 |
| > 6 à ≤ 14 semaines | 421/29677 | 14.19 | 306/2011 | 25.48 |
| > 14 à ≤ 52 semaines | 120/6139 | 19.55 | 273/9089 | 30.04 |
| > 52 semaines ou pas de livraison | Aucune donnée disponible | 5481/184733 | 29.67 | |
| 1 L'expulsion comprend une expulsion complète et partielle |
Interactions médicamenteuses pour Kyleena
Aucune étude d'interaction médicament-médicament n'a été menée avec Kyleena.
Les médicaments ou les produits à base de plantes qui induisent ou inhibent les enzymes métabolisantes de GNL, y compris le CYP3A4, peuvent diminuer ou augmenter respectivement les concentrations sériques de GNL pendant l'utilisation de Kyleena. Cependant, l'effet contraceptif de Kyleena est médié via la libération directe du GNL dans la cavité utérine et est peu susceptible d'être affecté par les interactions médicamenteuses via l'induction ou l'inhibition enzymatique.
Avertissements pour Kyleena
Inclus dans le cadre du 'PRÉCAUTIONS' Section
Précautions pour Kyleena
Risque de grossesse extra-utérine
Évaluez les femmes pour une grossesse extra-utérine si elles tombent enceintes de Kyleena en place car la probabilité d'une grossesse est augmentée avec Kyleena. Environ la moitié des grossesses qui se produisent avec Kyleena en place sont susceptibles d'être ectopiques. Considérez également la possibilité d'une grossesse extra-utérine dans le cas de douleurs abdominales inférieures, en particulier en association avec les règles manquées ou si une femme amenorrhée commence à saigner.
L'incidence de la grossesse extra-utérine dans les essais cliniques avec Kyleena qui excluait les femmes ayant des antécédents de grossesse extra-utérine était d'environ 0,2% par an. Le risque de grossesse extra-utérine chez les femmes qui ont des antécédents de grossesse extra-utérine et d'utilisation de Kyleena est inconnue. Les femmes ayant des antécédents de chirurgie tubaire de grossesse extra-utérine ou une infection pelvienne comportent un risque plus élevé de grossesse extra-utérine. La grossesse extra-utérine peut entraîner une perte de fertilité.
Risques avec une grossesse intra-utérine
Si la grossesse se produit pendant l'utilisation de Kyleena, retirez Kyleena, car la laisser en place peut augmenter le risque d'avortement spontané et de travail prématuré. L'élimination de Kyleena ou le sondage de l'utérus peut également entraîner un avortement spontané. En cas de grossesse intra-utérine avec Kyleena, considérez ce qui suit:
Avortement septique
Chez les patients tombant enceintes d'un IUS en place, un avortement septique - avec un choc septique de septicémie et une mort - peut se produire.
Continuation de la grossesse
Si une femme tombe enceinte de Kyleena en place et si Kyleena ne peut pas être supprimée ou si la femme choisit de ne pas le supprimer, avertissez-vous que le fait de ne pas enlever Kyleena augmente le risque de spécialisation de la fission. Conseillez-lui des rapports isolés de virilisation de la fœtus femelle après une exposition locale au GNL pendant la grossesse avec un LNG IUS en place [voir Utiliser dans des populations spécifiques ]. Follow her pregnancy closely et advise her to report immediately any symptom that suggests complications of the pregnancy.
État septique
Une infection grave ou une septicémie, y compris une septicémie streptococcique (gaz) du groupe A, a été signalée après l'insertion d'un IUS libérant du GNL. Dans certains cas, une douleur intense s'est produite dans les heures suivant l'insertion suivie d'une septicémie en quelques jours. Parce que la mort du gaz est plus probable si le traitement est retardé, il est important d'être conscient de ces infections rares mais graves. La technique aseptique lors de l'insertion de Kyleena est essentielle afin de minimiser les infections graves telles que le gaz.
Infection pelvienne
Examinez rapidement les utilisateurs avec des plaintes de basse douleur abdominale ou pelvienne décharge odorante des lésions ou des plaies génitales de fièvre saigneuse inexpliquée. Retirer Kyleena en cas d'endométrite récurrente ou de maladie inflammatoire pelvienne ou si une infection pelvienne aiguë est grave ou ne répond pas au traitement.
Maladie inflammatoire pelvienne (PID)
Kyleena is contraindicated in the presence of known or suspected PID or in women with a history of PID unless there has been a subsequent intrauterine pregnancy [see Contre-indications ]. IUDs have been associated with an increased risk of PID most likely due to organisms being introduced into the uterus during insertion. In clinical trials PID was observed in 0.5% of women overall et occurred more frequently within the first year et most often within the first month after insertion of Kyleena.
Les femmes à risque accru de PID
Le PID est souvent associé à une infection sexuellement transmissible (IST) et Kyleena ne protège pas contre STI. Le risque de PID est plus élevé pour les femmes qui ont plusieurs partenaires sexuels et aussi pour les femmes dont les partenaires sexuels ont plusieurs partenaires sexuels. Les femmes qui ont eu un PID courent un risque accru de récidive ou de réinfection. Vérifiez en particulier si la femme présente un risque accru d'infection (par exemple, le syndrome de la carence immunitaire a acquis la leucémie [AID] abus de drogues intraveineux).
Pid subclinique
Le PID peut être asymptomatique mais entraîne toujours des lésions tubaires et ses séquelles.
Traitement du PID
Après un diagnostic de PID ou suspecté d'échantillons bactériologiques PID doit être obtenu et l'antibiothérapie doit être initiée rapidement. L'élimination de Kyleena après le début de l'antibiothérapie est généralement appropriée.
Actinomycose
Actinomycose has been associated with IUDs. Remove Kyleena from symptomatic women et treat with antibiotics. The significance of actinomyces-like organisms on Pap smear in an asymptomatic IUD user is unknown et so this finding alone does not always require Kyleena removal et treatment. When possible confirm a Pap smear diagnosis with cultures.
Perforation
Perforation (total or partial including penetration/embedment of Kyleena in the uterine wall or cervix) may occur most often during insertion although the perforation may not be detected until sometime later. The incidence of perforation during clinical trials was <0.1%.
Le risque de perforation utérine est augmenté chez les femmes qui ont récemment accouché et chez les femmes qui allaitent au moment de l'insertion. Dans une grande étude de sécurité post-commercialisation menée aux États-Unis, le risque de perforation utérine était le plus élevé lorsque l'insertion s'est produite dans ≤ 6 semaines post-partum et également plus élevée avec l'allaitement au moment de l'insertion [voir Effets indésirables ].
Le risque de perforation peut être augmenté si Kyleena est insérée lorsque l'utérus est fixe rétroverti ou n'est pas complètement involutique.
Si la perforation se produit, localisez et retirez Kyleena. Une chirurgie peut être nécessaire. La détection ou l'élimination retardée de Kyleena en cas de perforation peut entraîner une migration en dehors des adhérences de la cavité utérine et une péritonite des perforations intestinales abcès d'obstruction intestinale et l'érosion des viscères adjacents. De plus, la perforation peut réduire l'efficacité des contraceptifs et entraîner une grossesse.
Expulsion
Une expulsion partielle ou complète de Kyleena peut se produire entraînant une perte d'efficacité. L'expulsion peut être associée à des symptômes de saignement ou de douleur ou il peut être asymptomatique et passer inaperçu. Kyleena diminue généralement les saignements menstruels au fil du temps; Par conséquent, une augmentation des saignements menstruelles peut indiquer une expulsion. Envisagez une imagerie diagnostique supplémentaire telle que les rayons X si l'expulsion est suspectée sur la base de l'échographie [voir Considérations cliniques pour une utilisation et un retrait ]. In clinical trials a 5-year expulsion rate of 3.5% (59 out of 1690 subjects) was reported.
Le risque d'expulsion est augmenté avec les insertions immédiatement après la livraison et semble être augmenté avec l'insertion après un avortement au deuxième trimestre sur la base de données limitées. Dans une grande étude de sécurité post-commercialisation menée aux États-Unis, le risque d'expulsion était plus faible avec le statut d'allaitement [voir Effets indésirables ].
Retirez une Kyleena partiellement expulsée. Si l'expulsion s'est produite, une nouvelle Kyleena peut être insérée à chaque fois que le fournisseur peut être raisonnablement certain que la femme n'est pas enceinte.
Kystes ovariens
Parce que l'effet contraceptif de Kyleena est principalement dû à ses effets locaux au sein des cycles ovulatoires de l'utérus avec une rupture folliculaire se produit généralement chez les femmes d'âge fertile à l'aide de Kyleena. Les kystes ovariens (rapportés comme des effets indésirables s'ils étaient des kystes anormaux non fonctionnels et / ou avaient un diamètre> 3 cm à un examen à ultrasons) ont été signalés au moins une fois au cours des essais cliniques chez 22% des femmes à l'aide de Kyleena et 0,6% des sujets interrompus à cause d'un kyste ovarien. La plupart des kystes ovariens sont asymptomatiques, bien que certains puissent être accompagnés d'une douleur pelvienne ou d'une dyspareunie. Dans la plupart des cas, les kystes ovariens disparaissent spontanément pendant deux à trois mois d'observation. Évaluer les kystes ovariens persistants. L'intervention chirurgicale n'est généralement pas requise.
Altérations du modèle de saignement
Kyleena can alter the bleeding pattern et result in spotting irregular bleeding heavy bleeding oligomenorrhea et amenorrhea. During the first 3–6 months of Kyleena use the number of bleeding et spotting days may be higher et bleeding patterns may be irregular. Thereafter the number of bleeding et spotting days usually decreases but bleeding may remain irregular.
Dans les essais cliniques de Kyleena, l'aménorrhée développée à la fin de la première année d'utilisation dans environ 12% des utilisateurs de Kyleena. Un total de 81 sujets sur 1697 (NULL,8%) ont interrompu en raison de plaintes de saignement utérines. Le tableau 2 montre les schémas de saignement documentés dans les essais cliniques de Kyleena sur la base des périodes de référence de 90 jours. Le tableau 3 montre le nombre de jours de saignement et de repérage basés sur des équivalents de cycle de 28 jours.
Tableau 2: Modèles de saignement rapportés avec Kyleena dans les études de contraception (par périodes de référence de 90 jours)
| Kyleena | 90 premiers jours N = 1566 | Second 90 jours N = 1511 | Fin de l'année 1 N = 1371 | Fin de l'année 3 N = 975 | Fin de l'année 5 N = 530 |
| Aménorrhée 1 | <1% | 5% | 12% | 20% | 23% |
| Saignement peu fréquente 2 | 10% | 20% | 26% | 26% | 26% |
| Saignement fréquent 3 | 25% | 10% | 4% | 2% | 2% |
| Saignement prolongé 4 | 57% | 14% | 6% | 2% | 1% |
| Saignement irrégulier 5 | 43% | 25% | 17% | 10% | 9% |
| 1 Défini comme des sujets sans saignement / taches tout au long de la période de référence de 90 jours 2 Défini comme des sujets avec 1 ou 2 épisodes de saignement / repérage dans la période de référence de 90 jours 3 Défini comme des sujets avec plus de 5 épisodes de saignement / repérage au cours de la période de référence de 90 jours 4 Défini comme des sujets avec des épisodes de saignement / repérage durant plus de 14 jours au cours de la période de référence de 90 jours. Les sujets présentant des saignements prolongés peuvent également être inclus dans l'une des autres catégories (à l'exclusion de l'aménorrhée) 5 Défini comme des sujets avec 3 à 5 épisodes de saignement / repérage et moins de 3 intervalles de saignement / sans repérage de 14 jours ou plus |
Tableau 3: Nombre moyen de jours de saignement et de repérage par cycle de 28 jours équivalent
| Cycle de 28 jours Équivalent | Cycle 1 N = 1619 | Cycle 4 N = 1575 | Cycle 7 N = 1518 | Cycle 13 N = 1394 | Cycle 39 N = 913 | Cycle 65 N = 322 |
| Jours de traitement | 1–28 | 85–112 | 169–196 | 337–364 | 1065-1092 | 1793-1820 |
| Signifier (SD) | Signifier (SD) | Signifier (SD) | Signifier (SD) | Signifier (SD) | Signifier (SD) | |
| Nombre de jours de saignement | 7.2 (5.9) | 3.2 (3.6) | 2.2 (3.0) | 1.5 (2.4) | 1.0 (2.0) | 0.9 (1.8) |
| Nombre de jours de repérage | 8.6 (6.0) | 4.6 (4.4) | 3.5 (3.4) | 2.9 (3.0) | 2.2 (2.6) | 2.1 (2.4) |
Si un changement significatif dans les saignements se développe pendant une utilisation prolongée, prenez des mesures diagnostiques appropriées pour exclure la pathologie de l'endomètre. Considérez la possibilité d'une grossesse si les menstruations ne se produisent pas dans les six semaines suivant le début d'une menstruation précédente. Une fois la grossesse, les tests de grossesse répétés ne sont généralement pas nécessaires chez les femmes amenorrhéiques, sauf si c'est indiqué par exemple par d'autres signes de grossesse ou par des douleurs pelviennes.
Cancer du sein
Les femmes qui ont actuellement ou ont eu un cancer du sein ou qui soupçonnent un cancer du sein ne devraient pas utiliser la contraception hormonale, y compris Kyleena, car certains cancers du sein sont sensibles aux hormones [voir Contre-indications ].
Des rapports spontanés sur le cancer du sein ont été reçus lors de l'expérience de la post-commercialisation avec un IUS libérant du GNL. Les études d'observation du risque de cancer du sein avec l'utilisation d'un IUS libérant du GNL ne fournissent pas de preuves concluantes d'un risque accru.
Considérations cliniques pour une utilisation et un retrait
Utilisez Kyleena avec prudence après une évaluation minutieuse si l'une des conditions suivantes existe et envisagez de retirer le système si l'une d'entre elles survient pendant l'utilisation:
- Coagulopathie ou utilisation d'anticoagulants
- Migraine focale migraine avec perte visuelle asymétrique ou autres symptômes indiquant une ischémie cérébrale transitoire
- Maux de tête exceptionnellement graves
- Augmentation marquée de la pression artérielle
- Maladie artérielle grave telle que l'AVC ou l'infarctus du myocarde
En outre, envisagez de retirer Kyleena si l'une des conditions suivantes survient pendant l'utilisation:
- Maligne utérine ou cervicale
- Jaunisse
Si les fils ne sont pas visibles ou ne sont considérablement raccourcis, ils peuvent avoir cassé ou rétracté dans le canal cervical ou l'utérus. Considérez la possibilité que le système ait été déplacé (par exemple expulsé ou perforé l'utérus) [voir Perforation Expulsion ]. Exclude pregnancy et verify the location of Kyleena for example by sonography X-ray or by gentle exploration of the cervical canal with a suitable instrument. If Kyleena is displaced remove it. A new Kyleena may be inserted at that time or during the next menses if it is certain that conception has not occurred. If Kyleena is in place with no evidence of perforation no intervention is indicated.
Imagerie par résonance magnétique (IRM) Informations de sécurité
 |
Des tests non cliniques ont démontré que Kyleena est MR conditionnelle. Un patient atteint de Kyleena peut être scanné en toute sécurité dans un système MR en tenant compte des conditions suivantes:
- Champ magnétique statique de 3,0 t ou moins
- Gradient de champ spatial maximal de 36000 Gauss / cm (360 T / m)
- Le système MR maximum a rapporté le taux d'absorption spécifique en moyenne (SAR) de 4W / kg (mode de fonctionnement contrôlé de premier niveau)
Dans les conditions de balayage définies au-dessus du Kyleena IUS, devrait produire une augmentation de température maximale inférieure à 2 ° C après 15 minutes de balayage continu.
Dans des tests non cliniques, l'artefact d'image causé par l'IUS s'est étendu jusqu'à 5 mm de l'IUS lorsqu'il est imaginé avec une séquence d'impulsion d'écho de gradient et un système IRM de 3,0 T.
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Informations sur les patients ).
- Infections sexuellement transmissibles: Informez le patient que ce produit ne protège pas contre l'infection par le VIH (SIDA) et d'autres infections sexuellement transmissibles (IST).
- Risque de grossesse extra-utérine: Conseillez le patient sur les risques de la grossesse extra-utérine, y compris la perte de fertilité. Apprenez-lui à reconnaître et à faire rapport à son fournisseur de soins de santé rapidement tous les symptômes de la grossesse extra-utérine. [Voir Avertissements et précautions ]
- Risques de la grossesse intra-utérine: Conseille à la patiente de contacter son professionnel de la santé si elle pense qu'elle pourrait être enceinte. Informez le patient des risques de la grossesse intra-utérine tout en utilisant Kyleena, y compris les risques de laisser Kyleena en place et les risques d'élimination de Kyleena ou de sonder l'utérus. Si Kyleena ne peut pas être supprimée chez une patiente enceinte, elle conseille de signaler immédiatement un symptôme qui suggère des complications de la grossesse. Conseillez-la des rapports isolés de virilisation du fœtus femelle après une exposition locale au GNL pendant la grossesse avec un IUS de GNL en place. [Voir Avertissements et précautions et Utiliser dans des populations spéciales ]
- État septique: Informez le patient selon lequel une infection grave ou une septicémie, y compris une septicémie streptococcique (GAS), peut survenir dans les premiers jours après l'insertion de Kyleena. Demandez-lui de contacter immédiatement un fournisseur de soins de santé si elle développe une douleur intense ou de la fièvre peu de temps après l'insertion de Kyleena. [Voir Avertissements et précautions ]
- Infection pelvienne: Conseiller le patient sur la possibilité d'infections pelviennes, y compris la PID et que ces infections peuvent causer des dommages tubaires entraînant une grossesse ou de l'infertilité extraordinaire ou rarement peut nécessiter une hystérectomie ou provoquer la mort. Apprenez aux patients à reconnaître et à faire rapport à leur fournisseur de soins de santé rapidement tout symptôme d'infection pelvienne. Ces symptômes comprennent le développement de troubles menstruels (saignements prolongés ou lourds) des décharges vaginales inhabituelles ou une douleur abdominale ou pelvienne ou une sensibilité aux frissons de dyspareunia et de la fièvre. [Voir Avertissements et précautions .]
- Perforation et Expulsion: Informez la patiente que l'IUS peut être expulsée ou perforer l'utérus et lui demander comment elle peut vérifier que les fils dépassent toujours le col de l'utérus. Informez-la qu'une douleur excessive ou des saignements vaginaux pendant le placement de Kyleena aggravant la douleur ou les saignements après le placement ou l'incapacité à sentir les cordes de Kyleena peut se produire avec la perforation et l'expulsion de Kyleena. Mettez en garde elle de ne pas tirer sur les fils et de déplacer Kyleena. Informez-la qu'il n'y a pas de protection contraceptive si Kyleena est déplacée ou expulsée. Demandez à la patiente de contacter son fournisseur de soins de santé si elle ne peut pas ressentir les fils et d'éviter les rapports sexuels ou d'utiliser un contraception de secours non hormonal (comme les préservatifs ou le spermicide) jusqu'à ce que l'emplacement de Kyleena ait été confirmé. Informez-lui que si la perforation se produit, Kyleena devra être localisée et retirée; une chirurgie peut être nécessaire. [Voir Avertissements et précautions ]
- Kystes ovariens: Conseiller le patient concernant le risque de kystes ovariens et que les kystes peuvent provoquer des symptômes cliniques, notamment des douleurs abdominales de douleur pelvienne ou une dyspareunie. Conseille à la patiente de contacter son fournisseur de soins de santé si elle éprouve ces symptômes. [Voir Avertissements et précautions ]
- Altérations du modèle de saignement: Informez le patient selon lequel des saignements et des taches irréguliers ou prolongés et / ou des crampes peuvent survenir au cours des premières semaines après l'insertion. Informez le patient que pendant les 6 premiers mois de Kyleena, utilisez le nombre de jours de saignement et de repérage peut être plus élevé et que les schémas de saignement peuvent être irréguliers. Si ses symptômes continuent ou sont graves, elle devrait les signaler à son fournisseur de soins de santé. [Voir Avertissements et précautions ]
- Considérations cliniques à utiliser et à retirer: Conseille à la patiente de contacter son fournisseur de soins de santé si elle vit l'une des éléments suivants:
- Un accident vasculaire cérébral ou crise cardiaque
- Maux de tête très graves ou migraineux
- Fièvre inexpliquée
- Jaunissement de la peau ou des blancs des yeux car il peut s'agir de signes de graves problèmes hépatiques
- Grossesse ou grossesse suspectée
- Douleur pelvienne douleur abdominale ou douleur pendant les relations sexuelles
- Séroconversion séropositive en elle-même ou son partenaire
- Exposition possible aux IST
- Décharge vaginale inhabituelle ou plaies génitales
- Saignement vaginal sévère ou saignement qui dure longtemps ou si elle manque une période menstruelle
- Incapacité à sentir les fils de Kyleena
- Imagerie par résonance magnétique (IRM) Informations de sécurité: Informer le patient que Kyleena ne peut être scanné en toute sécurité avec l'IRM uniquement dans des conditions spécifiques [voir Avertissements et précautions ]. Instruct patients who will have an MRI to tell their doctor that they have Kyleena.
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
[Voir Avertissements et précautions ]
Utiliser dans des populations spécifiques
Grossesse
Résumé des risques
L'utilisation de Kyleena est contre-indiquée pendant la grossesse ou avec une grossesse suspectée et Kyleena peut provoquer des résultats de grossesse défavorables [voir Contre-indications Avertissements et précautions ]. If a woman becomes pregnant with Kyleena in place the likelihood of ectopic pregnancy is increased et there is an increased risk of miscarriage sepsis premature labor et premature delivery. Remove Kyleena if possible if pregnancy occurs in a woman using Kyleena. If Kyleena cannot be removed follow the pregnancy closely [see Avertissements et précautions ].
Il y a eu des cas isolés de virilisation des organes génitaux externes du fœtus femelle après une exposition locale au GNL pendant la grossesse avec un IUS de GNL en place. Des études de reproduction animale n'ont pas été menées avec Kyleena.
Lactation
Résumé des risques
Des études publiées rapportent la présence de GNL dans le lait maternel. De petites quantités de progestatifs (environ 0,1% du total des doses maternelles) ont été détectées dans le lait maternel des mères infirmières qui ont utilisé d'autres IUS de libération de GNL entraînant une exposition du GNL aux nourrissons allaités. Il n'y a aucun rapport d'effets indésirables chez les nourrissons allaités avec une utilisation maternelle de contraceptifs progestatifs uniquement. Des cas isolés de diminution de la production de lait ont été signalés avec un IUS libérant du GNL. Les avantages du développement et de la santé de l'allaitement doivent être pris en compte avec le besoin clinique de la mère de Kyleena et tout effet indésirable potentiel sur l'enfant allaité de Kyleena ou de l'état maternel sous-jacent.
Femmes et mâles de potentiel reproducteur
Retour à la fertilité après avoir arrêté Kyleena
Environ 71% des 163 femmes qui ont souhaité la grossesse après l'arrêt de l'étude et ont fourni des informations de suivi conçues dans les 12 mois suivant le retrait de Kyleena.
Usage pédiatrique
L'innocuité et l'efficacité de Kyleena ont été établies chez les femmes d'âge reproducteur. L'efficacité devrait être la même pour les femmes postpubertales de moins de 18 ans que pour les utilisateurs de 18 ans et plus. L'utilisation de ce produit avant la ménarche n'est pas indiquée.
Utilisation gériatrique
Kyleena has not been studied in women over age 65 et is not approved for use in this population.
Informations sur la surdose pour Kyleena
Aucune information fournie
Contre-indications pour Kyleena
L'utilisation de Kyleena est contre-indiquée lorsqu'une ou plusieurs des conditions suivantes existent:
- Grossesse or suspicion of pregnancy [see Avertissements et précautions Utiliser dans des populations spécifiques ]
- Pour une utilisation comme contraception post-coïtale (contraception d'urgence)
- Anomalie utérine congénitale ou acquise, y compris les fibromes qui déforment la cavité utérine
- Maladie inflammatoire pelvienne aiguë (PID) ou antécédents de PID à moins qu'il y ait eu une grossesse intra-utérine ultérieure [voir Avertissements et précautions ]
- Endométrite post-partum ou avortement infecté au cours des 3 derniers mois
- Maligne utérine ou cervicale connue ou suspectée
- Un cancer du sein connu ou suspecté ou un autre cancer sensible au progestatif maintenant ou dans le passé
- Saignement utérine de l'étiologie inconnue
- Cuvicite aiguë non traitée ou vaginite, y compris la vaginose bactérienne ou d'autres infections des voies génitales inférieures jusqu'à l'infection
- Maladie du foie aiguë ou tumeur hépatique (bénigne ou malin)
- Conditions associées à une sensibilité accrue aux infections pelviennes [voir Avertissements et précautions ]
- Un dispositif intra-utérine (DIU) précédemment inséré qui n'a pas été supprimé
- Hypersensibilité à tout composant de ce produit [voir Effets indésirables et DESCRIPTION ]
Pharmacologie clinique for Kyleena
Mécanisme d'action
Le mécanisme local par lequel le GNL libéré en continu contribue à l'efficacité contraceptive de Kyleena n'a pas été démontré de manière concluante. Des études sur les prototypes de Kyleena et de LNG similaires ont suggéré plusieurs mécanismes qui empêchent la grossesse: épaississement du mucus cervical empêchant le passage du sperme dans l'inhibition de l'utérus de la capacité ou de la survie et de l'altération de l'endomètre.
Pharmacodynamique
Kyleena has mainly local progestogenic effects in the uterine cavity. The local concentrations of LNG lead to morphological changes including stromal pseudodecidualization gletular atrophy a leukocytic infiltration et a decrease in gletular et stromal mitoses.
Dans les essais cliniques avec l'ovulation de Kyleena, a été évalué sur la base des valeurs de progestérone sériques> 2,5 ng / ml dans une étude et des valeurs de progestérone sériques> 2,5 ng / ml avec des taux sériques d'estradiol <27.24 pg/mL in another study. Evidence of ovulation by these criteria was seen in 23 out of 26 women in the first year in 19 out of 20 women in the second year et in all 16 women in the third year. In the fourth year evidence of ovulation was observed in the one woman remaining in the subset et in the fifth year no women remained in this subset.
Pharmacocinétique
Absorption
De faibles doses de GNL sont administrées dans la cavité utérine avec le système de livraison intra-utérine de Kyleena. Le en vain Le taux de libération est d'environ 17,5 mcg / jour après 24 jours et est réduit à environ 15,3 mcg / jour après 60 jours et à 9,8 mcg / jour après 1 an. Il baisse ensuite progressivement à environ 7,9 mcg / jour après 3 ans et 7,4 mcg / jour après 5 ans. Le GNL moyen en vain Le taux de libération est d'environ 12,6 mcg / jour au cours de la première année et 9,0 mcg / jour sur la période de 5 ans.
Dans un sous-ensemble de 6 sujets, la concentration maximale de GNL sérique observée (moyenne ± ET) était de 302 ± 170 pg / ml atteint après 7,5 jours (médiane) d'insertion de Kyleena. Par la suite, les concentrations sériques de GNL (moyenne ± ET) à l'année 1 2 3 4 et 5 étaient de 199 ± 171 pg / ml (n = 6) 120 ± 57 pg / ml (n = 6) 122 ± 65 pg / ml (n = 6) 79 ± 12 pg / ml (n = 3) et 65 ± 15 pg / ml (n = 3) respectivement. Une évaluation pharmacocinétique de la population basée sur une base de données plus large (> 1000 patients) a montré un profil de concentration en baisse similaire avec 175 ± 74 pg / ml à 7 jours après le placement 125 ± 50 pg / ml à 1 an 99 ± 41 pg / ml après 3 ans et 90 ± 35 pg / ml après 5 ans.
Dosage de cypionate de testostérone pour la perte de poids
Distribution
Le volume apparent de distribution de GNL serait d'environ 1,8 L / kg. Le GNL est lié de manière non spécifique à l'albumine sérique et spécifiquement à la globuline de liaison des hormones sexuelles (SHBG). En conséquence, les changements dans la concentration de SHBG dans le sérum entraînent une augmentation (à une concentration de SHBG plus élevée) ou une diminution (à une concentration de SHBG plus faible) de la concentration totale de GNL dans le sérum. Dans un sous-ensemble de 6 sujets, la concentration de SHBG a diminué en moyenne d'environ 30% au cours des 3 premiers mois après l'insertion de Kyleena et est resté relativement stable sur la période d'utilisation de 5 ans. Moins de 2% du GNL en circulation est présent sous forme de stéroïde libre.
Élimination
Après l'administration intraveineuse de 0,09 mg de GNL à des volontaires sains, la clairance totale du GNL est d'environ 1 ml / min / kg et la demi-vie d'élimination est d'environ 20 heures. Les taux de dédouanement métaboliques peuvent différer entre les individus par plusieurs fois, ce qui peut expliquer en partie des variations individuelles larges des concentrations de GNL observées chez les individus utilisant des produits contraceptifs contenant du GNL.
Métabolisme
Le GNL d'absorption suivant est largement métabolisé. Les voies métaboliques les plus importantes sont la réduction du groupe Δ4-3-OXO et les hydroxylations aux positions 2α 1β et 16β suivie d'une conjugaison. Des quantités significatives de 3α 5β - conjuguée et non conjuguée sont également présentes dans le sérum ainsi que des quantités beaucoup plus petites de 3α 5α-tétrahydrolevonorgestrel et 16β-hydroxylevonorgestrel. Le CYP3A4 est l'enzyme principale impliquée dans le métabolisme oxydatif du GNL.
Excrétion
Les métabolites de la GNL et de ses phase I sont excrétés principalement sous forme de conjugués de glucuronide. Environ 45% du GNL et ses métabolites sont excrétés dans l'urine et environ 32% sont excrétés dans les matières fécales principalement sous forme de conjugués de glucuronide.
Populations spécifiques
Pédiatrique
L'innocuité et l'efficacité de Kyleena ont été établies chez les femmes d'âge reproducteur. L'utilisation de ce produit avant la ménarche n'est pas indiquée.
Gériatrique
Kyleena has not been studied in women over age 65 et is not approved for use in this population.
Course
Aucune étude n'a évalué l'effet de la race sur la pharmacocinétique de Kyleena.
Trouble hépatique
Aucune étude n'a été menée pour évaluer l'effet de la maladie hépatique sur la disposition de Kyleena.
Trouble rénal
Aucune étude formelle n'a été menée pour évaluer l'effet des maladies rénales sur la disposition de Kyleena.
Interactions médicament-médicament
Aucune étude d'interaction médicament-médicament n'a été menée avec Kyleena [voir Interactions médicamenteuses ].
Études cliniques
L'efficacité contraceptive de Kyleena a été évaluée dans un essai clinique qui a inscrit des femmes généralement en bonne santé âgées de 18 à 35 ans, dont 1452 ont reçu Kyleena. Parmi ces 40% (574), les femmes nullipares 870 (60%) ont terminé 3 ans de l'étude 707 (49%) élues pour s'inscrire à une prolongation de la montée à un total de 5 ans et 550 (38%) ont effectué 5 ans d'utilisation. L'essai a été une étude multi-nationale randomisée en plein air réalisée dans 11 pays en Europe en Amérique latine les États-Unis et le Canada. Les femmes de moins de six semaines post-partum avec des antécédents de grossesse extra-utérine avec des kystes ovariens cliniquement significatifs ou avec le VIH ou autrement à haut risque d'infections sexuellement transmissibles ont été exclues. Un total de 563 (39%) ont été traités sur des sites américains et 889 (61%) étaient sur des sites non américains. La démographie raciale des femmes inscrites qui a reçu Kyleena était: Caucasien (80%) noir / afro-américain (NULL,1%) d'autres (NULL,6%) et asiatiques (NULL,2%); 11% ont indiqué l'ethnicité hispanique. L'essai clinique n'avait ni poids supérieur ou inférieur ni limite d'IMC. La plage de poids était de 38 à 173 kg (poids moyen: 68,7 kg) et l'IMC moyen était de 25,3 kg / m 2 (Gamme 15,2–57,6 kg / m 2 ). Of Kyleena-treated women 22% discontinued the study treatment due to an adverse reaction 5.0% were lost to follow-up 2.3% withdrew for unspecified reasons 1.2% discontinued due to a protocol deviation 0.9% discontinued due to pregnancy et 20% discontinued due to other reasons.
Le taux de grossesse calculé comme l'indice des perles (PI) chez les femmes âgés de 18 à 35 ans était le principal critère d'efficacité utilisé pour évaluer la fiabilité contraceptive. Le PI a été calculé sur la base de cycles d'exposition équivalents de 28 jours; Des cycles évaluables ont exclu ceux dans lesquels la contraception de secours a été utilisée à moins qu'une grossesse ne se soit produite dans ce cycle. L'année 1 PI était basée sur 2 grossesses et le taux de grossesse cumulatif à 5 ans était basé sur 13 grossesses survenues après le début du traitement et dans les 7 jours suivant l'élimination ou l'expulsion de Kyleena. Le tableau 5 montre les taux de grossesse annuels et cumulatifs calculés.
Tableau 7: Indices de perles par an et taux de grossesse cumulatif à 5 ans
| Kyleena Clinical Trial | Index de perle | Taux de Kaplan Meier cumulatif à 5 ans | ||||
| Année 1 | Année | Année 3 | Année 4 | 5e année | ||
| Nombre de cycles d'évaluation de 28 jours d'exposition16207 | 16207 | 13853 | 11610 | 8556 | 7087 | 57313 |
| Grossesse Rate (95% Confidence Interval) | 0.16 (NULL,02 0,58) | 0.38 (NULL,10 0,96) | 0.45 (NULL,12 1,15) | 0.15 (NULL,00 0,85) | 0.37 (NULL,04 1,33) | 1.45 (NULL,82 2,53) |
Informations sur les patients pour Kyleena
Kyleena
(Ki-lee-nah)
(Système intra-utérine libérant le lévonorgestrel)
Lisez attentivement ces informations sur les patients avant de décider si Kyleena vous convient. Ces informations ne prennent pas la place de parler avec votre gynécologue ou un autre fournisseur de soins de santé spécialisé dans la santé des femmes. Si vous avez des questions sur Kyleena, demandez à votre fournisseur de soins de santé. Vous devez également en savoir plus sur d'autres méthodes de contraception pour choisir celle qui vous convient le mieux.
Kyleena does not protect against HIV infection (AIDS) et other sexually transmitted infections (STIs).
Qu'est-ce que Kyleena?
- Kyleena is a hormone-releasing system placed in your uterus by your healthcare provider to prevent pregnancy for up to 5 years.
- Kyleena can be removed by your healthcare provider at any time.
- Kyleena can be used whether or not you have given birth to a child.
Kyleena is a small flexible plastic T-shaped system that slowly releases a progestin hormone called lévonorgestrel (LNG) that is often used in birth control pills . Because Kyleena releases LNG into your uterus only small amounts of the hormone enter your blood. Kyleena does not contain estrogen .
Deux fils minces sont fixés à la tige (extrémité inférieure) de Kyleena. Les fils sont la seule partie de Kyleena que vous pouvez ressentir lorsque Kyleena est dans votre utérus; Cependant, contrairement à une chaîne de tampon, les fils ne s'étendent pas à l'extérieur de votre corps.
 |
Kyleena is small
 |
et Flexible
Kyleena is small et Flexible
Et si j'ai besoin d'un contrôle des naissances pendant plus de 5 ans?
Kyleena must be removed after 5 years. Your healthcare provider can place a new Kyleena during the same office visit if you choose to continue using Kyleena.
Et si je veux arrêter d'utiliser Kyleena?
Kyleena is intended for use up to 5 years but you can stop using Kyleena at any time by asking your healthcare provider to remove it. You could become pregnant as soon as Kyleena is removed so you should use another method of birth control if you do not want to become pregnant. Talk to your healthcare provider about the best birth control methods for you because your new method may need to be started 7 days before Kyleena is removed to prevent pregnancy.
Et si je change d'avis sur le contrôle des naissances et que je veux devenir enceinte en moins de 5 ans?
Votre fournisseur de soins de santé peut éliminer Kyleena à tout moment. Vous pouvez devenir enceinte dès que Kyleena est enlevée. Environ 7 femmes sur 10 qui veulent devenir enceintes deviendront enceintes au cours de la première année après le retrait de Kyleena.
Comment fonctionne Kyleena?
Kyleena may work in several ways including thickening cervical mucus inhibiting sperm movement reducing sperm survival et thinning the lining of your uterus. It is not known exactly how these actions work together to prevent pregnancy.
 |
Dans quelle mesure Kyleena fonctionne-t-elle pour la contraception?
Le tableau suivant montre la possibilité de tomber enceinte pour les femmes qui utilisent différentes méthodes de contrôle des naissances. Chaque boîte du graphique contient une liste de méthodes de contraception qui sont similaires en efficacité. Les méthodes les plus efficaces sont en haut du graphique. La boîte au bas du graphique montre la possibilité de tomber enceinte pour les femmes qui n'utilisent pas le contrôle des naissances et essaient de tomber enceinte.
Kyleena an intrauterine device (IUD) also known as an intrauterine system (IUS) is in the box at the top of the chart.
Qui pourrait utiliser Kyleena?
Vous pouvez choisir Kyleena si vous:
- veulent un contrôle des naissances à long terme qui offre une faible chance de tomber enceinte (moins de 1 sur 100)
- veulent un contrôle des naissances qui fonctionne en continu jusqu'à 5 ans
- veulent un contrôle des naissances qui est réversible
- Vous voulez une méthode de contracepulation que vous n'avez pas besoin de prendre quotidiennement
- sont disposés à utiliser une méthode de contraception qui est placée dans l'utérus
- veulent un contrôle des naissances qui ne contient pas d'œstrogènes
N'utilisez pas Kyleena si vous:
- sont ou peuvent être enceintes; Kyleena ne peut pas être utilisée comme contraceptif d'urgence
- Avoir une infection pelvienne grave appelée maladie inflammatoire pelvienne (PID) ou avoir eu un PID dans le passé à moins que vous n'ayez eu une grossesse normale après que l'infection disparaisse
- avoir une infection génitale non traitée maintenant
- ont eu une grave infection pelvienne au cours des 3 derniers mois après une grossesse
- peut obtenir facilement les infections. Par exemple si vous:
- avoir plusieurs partenaires sexuels ou votre partenaire a plusieurs partenaires sexuels
- avoir des problèmes avec votre système immunitaire
- utiliser ou abuser des drogues intraveineuses
- avoir ou soupçonner que vous pourriez avoir un cancer de l'utérus ou du col de l'utérus
- avoir des saignements du vagin qui n'ont pas été expliqués
- avoir une maladie du foie ou une tumeur hépatique
- avoir un cancer du sein ou tout autre cancer sensible au progestatif (une hormone féminine) maintenant ou dans le passé
- avoir déjà un appareil intra-utérine dans votre utérus
- avoir une condition de l'utérus qui change la forme de la cavité utérine telle que les grandes tumeurs fibromes
- sont allergiques au lévonorgestrel silicone polyéthylène argent silice barium sulfate de barium en polypropylène ou phtalocyanine de cuivre
Avant de faire placer Kyleena, dites à votre fournisseur de soins de santé de toutes vos conditions médicales, y compris si vous:
- avoir l'une des conditions énumérées ci-dessus
- ont eu une crise cardiaque
- ont eu un accident vasculaire cérébral
- sont nés avec une maladie cardiaque ou ont des problèmes avec vos vannes cardiaques
- avoir des problèmes avec la coagulation du sang ou prendre des médicaments pour réduire la coagulation
- avoir une pression artérielle élevée
- a récemment eu un bébé ou allaiter
- ont des maux de tête sévères ou des maux de tête de migraine
- avoir le SIDA VIH ou toute autre infection sexuellement transmissible
Parlez à votre fournisseur de soins de santé de tous les médicaments que vous prenez, y compris les vitamines et suppléments à base de médicaments sur ordonnance et en vente libre.
Comment Kyleena est-elle placée?
Kyleena is placed by your healthcare provider during an in-office visit or immediately after giving birth.
Tout d'abord, votre fournisseur de soins de santé examinera votre bassin pour trouver la position exacte de votre utérus. Votre fournisseur de soins de santé nettoiera ensuite votre vagin et votre col avec une solution antiseptique et fera glisser un tube en plastique mince contenant Kyleena à travers le col de l'utérus dans votre utérus.
Votre fournisseur de soins de santé retirera ensuite le tube en plastique et laissera Kyleena dans votre utérus.
Votre fournisseur de soins de santé coupera les fils sur la bonne longueur.
Vous pouvez ressentir des saignements de douleur ou des étourdissements pendant et après le placement. Si vos symptômes ne passent pas dans les 30 minutes suivant le placement, Kyleena n'a peut-être pas été placé correctement.
Votre fournisseur de soins de santé vous examinera pour voir si Kyleena doit être supprimée ou remplacée.
Dois-je vérifier que Kyleena est en place?
Oui, vous devez vérifier que Kyleena est en position appropriée en ressentant les fils de retrait. C'est une bonne habitude de le faire 1 fois par mois. Votre professionnel de la santé devrait vous apprendre à vérifier que Kyleena est en place. Lavez d'abord les mains avec du savon et de l'eau. Vous pouvez vérifier en atteignant le haut de votre vagin avec des doigts propres pour sentir les fils de retrait. Ne tirez pas sur les fils. Si vous ressentez plus que les fils ou si vous ne pouvez pas sentir les fils, Kyleena peut ne pas être dans la bonne position et peut ne pas empêcher la grossesse. Évitez les rapports sexuels ou utilisez un contraception de secours non hormonal (comme les préservatifs ou le spermicide) et demandez à votre fournisseur de soins de santé de vérifier que Kyleena est toujours au bon endroit.
Combien de temps après le placement de Kyleena dois-je retourner à mon fournisseur de soins de santé?
Appelez votre fournisseur de soins de santé si vous avez des questions ou des préoccupations (voir quand dois-je appeler mon fournisseur de soins de santé?). Sinon, vous devriez retourner à votre fournisseur de soins de santé pour une visite de suivi 4 à 6 semaines après que Kyleena soit placée pour s'assurer que Kyleena est dans la bonne position.
Puis-je utiliser des tampons ou des tasses menstruelles avec Kyleena?
Oui, les tampons ou les tasses menstruelles peuvent être utilisées avec Kyleena. Changer les tampons ou les tasses menstruelles avec soin pour éviter de tirer les fils de Kyleena. Si vous pensez que vous avez peut-être retiré Kyleena à sa place, évitez les rapports sexuels ou utilisez un contraception de secours non hormonal (comme les préservatifs ou le spermicide) et contactez votre fournisseur de soins de santé.
Et si je tombais enceinte en utilisant Kyleena?
Appelez votre professionnel de la santé immédiatement si vous pensez être enceinte. Si possible, faites également un test de grossesse urinaire. Si vous tombez enceinte en utilisant Kyleena, vous pouvez avoir une grossesse extra-utérine. Cela signifie que la grossesse n'est pas dans l'utérus. Des saignements vaginaux inhabituels ou des douleurs abdominales peuvent être un signe de grossesse extra-utérine.
La grossesse extra-utérine est une urgence médicale qui nécessite souvent une intervention chirurgicale. La grossesse extra-utérine peut provoquer une infertilité interne et même la mort.
Il existe également des risques si vous tombez enceinte en utilisant Kyleena et que la grossesse est dans l'utérus. Une fausse couche d'infection sévère l'accouchement prématuré et même la mort peuvent survenir avec des grossesses qui se poursuivent avec un dispositif intra-utérine (DIU). Pour cette raison, votre professionnel de la santé peut essayer de retirer Kyleena même si le retirer peut provoquer une fausse couche. Si Kyleena ne peut pas être supprimée, parlez avec votre fournisseur de soins de santé des avantages et des risques de poursuivre la grossesse et les effets possibles de l'hormone sur votre bébé à naître.
Si vous continuez votre grossesse, consultez régulièrement votre fournisseur de soins de santé. Appelez votre fournisseur de soins de santé immédiatement si vous obtenez des symptômes de la grippe fièvre frisson de crampes à crampes saignant des débits vaginaux ou des fluides qui fuient de votre vagin. Il peut s'agir de signes d'infection.
Comment Kyleena changera-t-elle mes règles?
Pendant les 3 à 6 premiers mois, vos règles peuvent devenir irrégulières et le nombre de jours de saignement peut augmenter. Vous pouvez également avoir des taches ou des saignements légers fréquents. Certaines femmes ont des saignements lourds pendant cette période. Vous pouvez également avoir des crampes au cours des premières semaines. Après avoir utilisé Kyleena pendant un certain temps, le nombre de jours de saignement et de repérage devrait diminuer. Pour certaines femmes, les périodes s'arrêteront complètement. Lorsque Kyleena est supprimée, vos règles menstruelles doivent revenir.
Est-il sûr d'allaiter lors de l'utilisation de Kyleena?
Vous pouvez utiliser Kyleena lorsque vous allaitez. Kyleena est peu susceptible d'affecter la qualité ou la quantité de lait maternel ou la santé de votre bébé d'allaitement. Cependant, des cas isolés de diminution de la production de lait ont été signalés. Le risque que Kyleena entre dans le mur de l'utérus (devenant intégré) ou passant par le mur de l'utérus est augmenté si Kyleena est insérée pendant que vous allaitez.
Kyleena interférera-t-elle avec les rapports sexuels?
Vous et votre partenaire ne devriez pas ressentir Kyleena pendant les rapports sexuels. Kyleena est placée dans l'utérus et non dans le vagin. Parfois, votre partenaire peut ressentir les fils. Si cela se produit ou si vous ou votre partenaire ressentez de la douleur pendant le sexe, parlez avec votre fournisseur de soins de santé.
Puis-je avoir une IRM avec Kyleena en place?
Kyleena can be safely scanned with MRI only under specific conditions. Before you have an MRI tell your healthcare provider that you have Kyleena an intrauterine device (IUD) in place.
Quels sont les effets secondaires possibles de Kyleena?
Kyleena can cause serious side effects including:
Dites immédiatement à votre fournisseur de soins de santé si vous avez l'un de ces signes de PID: longlast ou saignement lourd décharge vaginale inhabituelle faible abdominal (zone de l'estomac) douloureux sexe douloureux feverts fièvre lésions ou plaies génitales.
- Risques de la grossesse extra-utérine et de la grossesse intra-utérine. Il y a des risques si vous tombez enceinte en utilisant Kyleena (voyez si je tombe enceinte en utilisant Kyleena?).
- Infection potentiellement mortelle. Une infection potentiellement mortelle peut se produire dans les premiers jours suivant la place de Kyleena. Appelez immédiatement votre fournisseur de soins de santé si vous développez une douleur intense ou de la fièvre peu de temps après la place de Kyleena.
- Maladie inflammatoire pelvienne (PID). Certains utilisateurs du DIU obtiennent une grave infection pelvienne appelée maladie inflammatoire pelvienne. Le PID est généralement transmissible sexuellement. Vous avez plus de chances d'obtenir un PID si vous ou votre partenaire avez des relations sexuelles avec d'autres partenaires. Le PID peut provoquer de graves problèmes tels que l'infertilité de la grossesse extra-utérine ou des douleurs pelviennes qui ne disparaissent pas. Le PID est généralement traité avec des antibiotiques. Des cas plus graves de PID peuvent nécessiter une intervention chirurgicale, y compris l'élimination de l'utérus (hystérectomie). Dans de rares cas, les infections qui commencent comme le PID peuvent même provoquer la mort.
- Perforation. Kyleena may go into the wall of the uterus (become embedded) or go through the wall of the uterus. This is called perforation. If this occurs Kyleena may no longer prevent pregnancy. If perforation occurs Kyleena may move outside the uterus et can cause internal scarring infection or damage to other organs et you may need surgery to have Kyleena removed. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with perforation. The risk of perforation is increased if Kyleena is inserted while you are breastfeeding or if you have recently given birth.
- Expulsion. Kyleena may come out by itself. This is called expulsion. Expulsion occurs in about 4 out of 100 women. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with expulsion. You may become pregnant if Kyleena comes out. If you think that Kyleena has come out avoid intercourse or use a non-hormonal back-up birth control (such as condoms or spermicide) et call your healthcare provider. The risk of expulsion is increased with insertion right after delivery or second-trimester abortion.
Les effets secondaires courants de Kyleena comprennent:
- Saignement de la douleur ou étourdissements pendant et après le placement. Si ces symptômes ne s'arrêtent pas 30 minutes après le placement, Kyleena n'a peut-être pas été placée correctement. Votre fournisseur de soins de santé vous examinera pour voir si Kyleena doit être supprimée ou remplacée.
- Changements de saignement. Vous pouvez avoir des saignements et des repérations entre les périodes menstruelles, en particulier au cours des 3 à 6 premiers mois. Parfois, le saignement est plus lourd que d'habitude au début. Cependant, le saignement devient généralement plus léger que d'habitude et peut être irrégulier. Appelez votre fournisseur de soins de santé si le saignement reste plus lourd que d'habitude ou augmente après qu'il a été léger depuis un certain temps.
- Périodes menstruelles manquées. Environ 12 femmes sur 100 cessent d'avoir des règles après 1 an d'utilisation de Kyleena. Si vous avez des inquiétudes que vous pourriez être enceintes en utilisant Kyleena, faites un test de grossesse d'urine et appelez votre fournisseur de soins de santé. Si vous n'avez pas de règles pendant 6 semaines pendant Kyleena, utilisez, appelez votre fournisseur de soins de santé. Lorsque Kyleena est supprimée, vos règles menstruelles doivent revenir.
- Kystes sur l'ovaire. Environ 22 femmes sur 100 utilisant Kyleena développent un kyste sur l'ovaire. Ces kystes disparaissent généralement par eux-mêmes en 2 à 3 mois. Cependant, les kystes peuvent provoquer des douleurs et parfois les kystes auront besoin d'une intervention chirurgicale.
Les autres effets secondaires courants comprennent:
- Inflammation ou infection de la partie extérieure de votre vagin (vulvovaginite)
- douleur abdominale ou pelvienne
- Maux de tête ou migraine
- acné or greasy skin
- périodes douloureuses
- seins douloureux ou douloureux
Ce ne sont pas tous les effets secondaires possibles avec Kyleena. Pour plus d'informations, demandez à votre fournisseur de soins de santé.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088. Vous pouvez également signaler les effets secondaires à Bayer Healthcare Pharmaceuticals au 1-888-842-2937.
Après que Kyleena ait été placée quand devrais-je appeler mon fournisseur de soins de santé?
Si Kyleena est accidentellement enlevée et que vous avez eu des rapports vaginaux au cours de la semaine précédente, vous risquez de risquer une grossesse et vous devriez parler à un fournisseur de soins de santé.
Appelez votre fournisseur de soins de santé si vous avez des inquiétudes concernant Kyleena. Assurez-vous d'appeler si vous:
- Je pense que tu es enceinte
- avoir des douleurs abdominales ou douleurs abdominales pendant les relations sexuelles
- ont des débits vaginaux inhabituels ou des plaies génitales
- ont des symptômes ou des frissons en forme de grippe inexpliqués
- pourrait être exposé à des infections sexuellement transmissibles (IST)
- craignent que Kyleena ait été expulsée (est sortie)
- ne peut pas sentir les fils de Kyleena
- développer des maux de tête très graves ou migraineux
- Ayez le jaunissement de la peau ou des blancs des yeux. Il peut s'agir de signes de problèmes hépatiques.
- ont eu un accident vasculaire cérébral or crise cardiaque
- devenir séropositif ou votre partenaire devient séropositif
- ont des saignements vaginaux sévères ou des saignements qui durent longtemps ou qui vous concernent
Conseils généraux sur l'utilisation sûre et efficace de Kyleena.
Les médicaments sont parfois prescrits pour des conditions autres que celles énumérées dans les dépliants d'information des patients. Si vous souhaitez plus d'informations, parlez avec votre fournisseur de soins de santé. Vous pouvez demander à votre professionnel de la santé des informations sur Kyleena qui est écrite pour les professionnels de la santé.
Quels sont les ingrédients de Kyleena?
Ingrédient actif: lévonorgestrel
Ingrédients inactifs: silicone polyéthylène argent silice barium sulfate de barium Polypropylène cuivre phtalocyanine
Ces informations sur les patients ont été approuvées par la Food and Drug Administration des États-Unis.

