Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Antibiotiques, linosamideCléocine IV
Résumé
Qu'est-ce que Cléocine?
La cléocine (clindamycine) est un antibiotique utilisé pour le traitement des infections graves causées par des bactéries anaérobies sensibles. Le cléocine est disponible sous forme générique.
Quels sont les effets secondaires du cléocine?
Cléocine IV
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- Diarrhée persistante
- douleurs abdominales
- crampes
- sang ou mucus dans vos tabourets
- douleur ou gonflement sur le site d'injection
- urine sombre
- jaunissement de la peau ou des yeux (jaunisse)
- nausées ou vomissements persistants
- Changement de la quantité d'urine
- ecchymoses ou ecchymoses faciles
- douleurs articulaires
- fièvre
- mal de gorge persistant
- rythme cardiaque lent ou irrégulier rapide
- des évanouissements et
- étourdissements sévères
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires de la cléocine comprennent:
La méthylprednisolone vous fait prendre du poids
- douleurs abdominales
- pseudomembranous colite
- œsophagite
- nausée
- vomissement
- diarrhée
- Taste désagréable ou métallique dans la bouche (si le cléocine est injecté dans une veine)
- Douleur et gonflement sur le site d'injection (si la cléocine est injectée dans un muscle)
- Réactions d'hypersensibilité (éruptions cutanées et ruches)
- démangeaison
- infection vaginale et
- jaunissement de la peau et des yeux (jaunisse).
Dites à votre médecin si vous avez des effets secondaires graves du cléocine, notamment:
- Douleur ou gonflement au site d'injection (si ce médicament est injecté dans une veine)
- urine sombre
- les yeux ou la peau jaunissent
- nausées ou vomissements persistants
- un changement de quantité d'urine
- ecchymoses ou saignements faciles
- Douleur dans plusieurs articulations
- Nouveaux signes d'infection (par exemple la fièvre persistante mal de gorge)
- rythme cardiaque rapide / lent / irrégulier ou
- évanouissement.
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; et des étourdissements soudains étourdisseurs ou s'évanouissant;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour le cléocine
La dose recommandée de cléocine pour les adultes est de 150 à 450 mg par voie orale toutes les 6 heures ou des doses intraveineuses de 600-2700 mg par jour en 2 à 4 doses divisées.
Quelles substances ou suppléments de médicaments interagissent avec le cléocine?
La cléocine peut interagir avec d'autres agents de blocage neuromusculaires de l'érythromycine et du contrôle des naissances hormonales. Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Cléocine pendant la grossesse et l'allaitement
Le cléocine n'a pas été correctement évalué chez les femmes enceintes. Le cléocine ne doit être utilisé pendant la grossesse que s'il est clairement nécessaire. Le cléocine passe dans le lait maternel et pourrait avoir des effets indésirables sur un nourrisson infirmier. Consultez votre médecin avant l'allaitement.
Informations Complémentaires
Notre centre de médicaments sur les effets secondaires Cleocin offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Dosage
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Précautions
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
C Lostridium dur - La diarrhée associée (CDAD) a été signalée avec l'utilisation de presque tous les agents antibactériens, y compris le phosphate de cléocine et peut aller en gravité de la diarrhée légère à la colite mortelle. Le traitement avec des agents antibactériens modifie la flore normale du côlon conduisant à la prolifération de C. difficile .
Étant donné que le traitement par la cléocine phosphate a été associé à une colite sévère qui peut se terminer mortellement, elle devrait être réservée aux infections graves où des agents antimicrobiens moins toxiques sont inappropriés comme décrit dans la section des indications et de l'utilisation. Il ne doit pas être utilisé chez les patients atteints d'infections non bactériennes telles que la plupart des infections des voies respiratoires supérieures. C. difficile produit des toxines A et B qui contribuent au développement de la CDAD. Hypertoxine produisant des souches de C. difficile provoquer une morbidité et une mortalité accrues car ces infections peuvent être réfractaires en thérapie antimicrobienne et peuvent nécessiter une colectomie. La CDAD doit être considérée chez tous les patients qui présentent une diarrhée après une utilisation antibiotique. Des antécédents médicaux attentifs sont nécessaires car la CDAD se produirait sur deux mois après l'administration d'agents antibactériens.
Si la CDAD est suspectée ou confirmée l'utilisation d'antibiotiques en cours non dirigée contre C. difficile peut avoir besoin d'être interrompu. Supplémentation des protéines de fluide et d'électrolyte appropriée Traitement antibiotique de C. difficile et l'évaluation chirurgicale doit être instituée comme indiqué cliniquement.
Description de Cléocine I.V.
La solution stérile du cléocine phosphate dans les flacons contient du phosphate de clindamycine une ester soluble dans l'eau de la clindamycine et de l'acide phosphorique. Chaque ML contient l'équivalent de 150 mg de clindamycine 0,5 mg d'aménagement de disodium et de 9,45 mg d'alcool benzylique ajouté comme conservateur dans chaque ML. La clindamycine est un antibiotique seminthétique produit par un 7 (s) -chloro-substitution du groupe 7 (R) -hydroxyle du composé parent de la lincomycine.
Le nom chimique du phosphate de clindamycine est l- direction -annonce- galacto -Octopyranoside méthyl-7-chloro-678-trideoxy-6 - [[(1-méthyl-4-propyl-2-pyrrolidinyl) carbonyl] amino] -1-thio- 2- (phosphate de dihydrogène) (2S- trans ) -.
La formule moléculaire est C 18 H 34 Manger 2 0 8 PS et le poids moléculaire est de 504,96.
La formule structurelle est représentée ci-dessous:
 |
Le phosphate de cléocine dans le flacon complémentaire est destiné à une utilisation intraveineuse uniquement après une dilution supplémentaire avec un volume approprié de solution de base diluée complémentaire (voir Directions à utiliser ).
La solution de cléocine phosphate IV dans le récipient en plastique galaxie à usage intraveineuse est composée de phosphate de clindamycine équivalente à 300 600 et 900 mg de clindamycine préalée à 5% de dextrose comme solution stérile. L'évétate de disodium a été ajouté à une concentration de 0,04 mg / ml. Le pH a été ajusté avec de l'hydroxyde de sodium et / ou de l'acide chlorhydrique.
Le récipient en plastique est fabriqué à partir d'un plastique multicouche spécialement conçu PL 2501. Les solutions en contact avec le récipient en plastique peuvent lixiviation de certains de ses composants chimiques en très petites quantités dans la période d'expiration. L'adéquation du plastique a été confirmée dans les tests chez les animaux en fonction des tests biologiques USP pour les récipients en plastique ainsi que par des études de toxicité de la culture tissulaire.
Utilisations de Cléocine I.V.
Les produits de cléocine phosphate sont indiqués dans le traitement des infections graves causées par des bactéries anaérobies sensibles.
Les produits de cléocine phosphate sont également indiqués dans le traitement des infections graves en raison de souches sensibles de streptocoques pneumocoques et de staphylocoques. Son utilisation doit être réservée aux patients allergiques à la pénicilline ou à d'autres patients pour lesquels le jugement du médecin, une pénicilline est inappropriée. En raison du risque de colite pseudomembrane associée aux antibiotiques Avertissement en boîte Avant de sélectionner la clindamycine, le médecin doit considérer la nature de l'infection et la pertinence d'alternatives moins toxiques (par exemple l'érythromycine).
Des études bactériologiques doivent être réalisées pour déterminer les organismes causaux et leur sensibilité à la clindamycine.
Des procédures chirurgicales indiquées doivent être effectuées conjointement avec l'antibiothérapie.
Le phosphate de cléocine est indiqué dans le traitement des infections graves causées par des souches sensibles des organismes désignés dans les conditions énumérées ci-dessous:
Infections des voies respiratoires inférieures, y compris l'empyème de la pneumonie et l'abcès pulmonaire causés par les anaérobies Streptococcus pneumoniae Autres streptocoques (sauf E. faecalis ) et Staphylococcus aureus.
Infections de la peau et de la structure cutanée causées par Streptococcus pyogenes staphylococcus aureus et Anaerobes.
Les infections gynécologiques, y compris l'endométrite, la cellulite pelvienne de l'abcès tubo-ovarien non ovarien et l'infection vaginale post-chirurgicale causée par des anaérobies sensibles.
Les infections intra-abdominales, y compris la péritonite et l'abcès intra-abdominal causées par des organismes anaérobies sensibles.
Septicémie causée par Staphylococcus aureus streptocoques (sauf Enterococcus faecalis ) et susceptible anaerobes.
Des infections osseuses et articulaires, y compris une ostéomyélite hématogène aiguë causée par Staphylococcus aureus et en tant que thérapie complémentaire dans le traitement chirurgical des infections osseuses chroniques et articulaires en raison d'organismes sensibles.
Pour réduire le développement de bactéries résistantes aux médicaments et maintenir l'efficacité du phosphate de cléocine et d'autres médicaments antibactériens, la cléocine phosphate doit être utilisée uniquement pour traiter ou prévenir les infections qui sont prouvées ou fortement suspectées comme causées par des bactéries sensibles. Lorsque des informations sur la culture et la sensibilité sont disponibles, elles doivent être prises en compte dans la sélection ou la modification de la thérapie antibactérienne. En l'absence de telles données, les modèles d'épidémiologie et de sensibilité locaux peuvent contribuer à la sélection empirique de la thérapie.
Dosage pour le cléocine I.V.
Si la diarrhée se produit pendant la thérapie, cet antibiotique doit être interrompu (voir Avertissement de boîte ).
L'administration de la clindamycine phosphate IM doit être utilisée non diluée.
synthroid 200 mcg et perte de poids
L'administration de clindamycine phosphate IV doit être diluée (voir Dilution pour l'utilisation IV et les taux de perfusion IV ci-dessous).
Adultes
Parenter (IM ou IV Administration): infections graves dues à un cocci à grammes aérobies et aux anaérobies plus sensibles (n'incluant généralement pas Bacteroides fragilis peptococcus espèces et Clostridium espèces autres que Clostridium perfringens ):
600.1200 mg / jour en 2 3 ou 4 doses égales.
Des infections plus graves, en particulier celles due à des Bacteroides fragilis peptococcus espèce ou Clostridium species à part Clostridium perfringens:
1200,2700 mg / jour en 2 3 ou 4 doses égales.
Pour les infections plus graves, ces doses peuvent devoir être augmentées. Dans les situations potentiellement mortelles dues à des aérobes ou aux anaérobies, ces doses peuvent être augmentées. Des doses jusqu'à 4800 mg par jour ont été données par voie intraveineuse aux adultes. Voir Dilution pour l'utilisation IV et les taux de perfusion IV Section ci-dessous.
Les injections intramusculaires uniques de plus de 600 mg ne sont pas recommandées.
Alternativement, le médicament peut être administré sous la forme d'une seule perfusion rapide de la première dose suivie d'une perfusion IV continue comme suit:
| Pour maintenir les taux sériques de clindamycine | Taux de perfusion rapide | Taux de perfusion d'entretien |
| Au-dessus de 4 mcg / ml | 10 mg / min pendant 30 min | 0,75 mg / min |
| Au-dessus de 5 mcg / ml | 15 mg / min pendant 30 min | 1,00 mg / min |
| Au-dessus de 6 mcg / ml | 20 mg / min pendant 30 min | 1,25 mg / min |
Nourbelles (moins de 1 mois)
15 à 20 mg / kg / jour en 3 à 4 doses égales. La dose inférieure peut être adéquate pour les petites prématures.
Patients pédiatriques 1 mois à 16 ans
Administration parentérale (IM ou IV): 20 à 40 mg / kg / jour en 3 ou 4 doses égales. Les doses plus élevées seraient utilisées pour des infections plus graves. Comme alternative au dosage sur une base corporelle, les patients pédiatriques peuvent être dosés sur la base de la surface du corps des mètres carrés: 350 mg / m 2 / jour pour les infections graves et 450 mg / m 2 / jour pour des infections plus graves.
La thérapie parentérale peut être changée en pédiatricr de cléocin oral ® Granules aromatisés (chlorhydrate de clindamycine palmitate) ou Cleocin HCLR ® Capsules (chlorhydrate de clindamycine) lorsque la condition garantit et à la discrétion du médecin.
Dans les cas d'infections streptococciques β-hémolytiques, le traitement doit être poursuivi pendant au moins 10 jours.
Dilution pour l'utilisation IV et les taux de perfusion IV: The concentration of clindamycin in diluent for infusion should not exceed 18 mg per mL. Infusion rates should not exceed 30 mg per minute. Les dilutions et taux de perfusion habituels sont les suivants:
| Dose | Diluant | Temps |
| 300 mg | 50 ml | 10 min |
| 600 mg | 50 ml | 20 min |
| 900 mg | 50-100 ml | 30 min |
| 1200 mg | 100 ml | 40 min |
L'administration de plus de 1200 mg dans une seule perfusion d'une heure n'est pas recommandée.
Les médicaments parentéraux doivent être inspectés visuellement pour les particules et la décoloration avant l'administration chaque fois que la solution et le permis de conteneur.
Dilution et compatibilité
Les études de compatibilité physique et biologique surveillée pendant 24 heures à température ambiante n'ont démontré aucune inactivation ou incompatibilité avec l'utilisation d'une solution stérile de cléocine phosphate (phosphate de clindamycine) dans des solutions IV contenant du chlorure de sodium calcium ou de potassium et des solutions contenant du complexe de vitamine B à des concentrations généralement utilisées cliniquement. Aucune incompatibilité n'a été démontrée avec les antibiotiques Cephalothin kanamycine gentamicine pénicilline ou carbénicilline.
Les médicaments suivants sont physiquement incompatibles avec le phosphate de clindamycine: les barbituriques d'ampicilline sodium phénytoine sodium au gluconate de calcium d'aminophylline et de sulfate de magnésium.
La compatibilité et la durée de la stabilité des adjuvoirs de médicament varieront en fonction de la concentration et d'autres conditions. Pour les informations actuelles concernant les compatibilités du phosphate de clindamycine dans des conditions spécifiques, veuillez contacter la pharmacide de l'unité d'information médicale et de médicament
Stabilité physico-chimique des solutions diluées de la température ambiante du cléocine phosphate
6 9 et 12 mg / ml (équivalent à la base de la clindamycine) dans l'injection de dextrose à 5% d'injection de chlorure de sodium 0,9% ou l'injection de ringers lactadiée dans des bouteilles en verre ou des minibags ont démontré une stabilité physique et chimique pendant au moins 16 jours à 25 ° C. Également 18 mg / ml (équivalent à la base de la clindamycine) dans l'injection de dextrose 5% dans les minibags ont démontré une stabilité physique et chimique pendant au moins 16 jours à 25 ° C.
Réfrigération
6 9 et 12 mg / ml (équivalent à la base de la clindamycine) dans l'injection de dextrose à 5% d'injection de chlorure de sodium 0,9% ou l'injection de ringers lactadiée dans des bouteilles en verre ou des minibags ont démontré une stabilité physique et chimique pendant au moins 32 jours à 4 ° C.
IMPORTANT: Ces informations sur la stabilité chimique n'indique en rien qu'il serait acceptable de bien utiliser ce produit après l'heure de préparation. Une bonne pratique professionnelle suggère que les adjuvants composés devraient être administrés dès la préparation, comme cela est possible.
Congelé
6 9 et 12 mg / ml (équivalent à la base de la clindamycine) dans l'injection de dextrose à 5% d'injection de chlorure de sodium 0,9% ou l'injection de ringers lactadiée dans les minibags ont démontré une stabilité physique et chimique pendant au moins huit semaines à -10 ° C.
Congelé solutions should be èmeawed at room temperature and not refrozen.
Directions pour la distribution
Ensemble de pharmacie en vrac
Pas pour la perfusion directe
L'ensemble de pharmacie est destiné à une utilisation dans un service de mélange de pharmacie uniquement sous un capot de flux laminaire. L'entrée dans le flacon doit être effectuée avec un ensemble de transfert stérile de petit diamètre ou un autre dispositif de dispensation stérile de petit diamètre et un contenu distribué dans des aliquotes en utilisant une technique aseptique. Plusieurs entrées avec une aiguille et une seringue ne sont pas recommandées. Après l'entrée, utilisez rapidement le contenu du flacon. Toute partie inutilisée doit être rejetée dans les 24 heures suivant l'entrée initiale.
Directions à utiliser
Cléocine phosphate IV Solution dans Galaxy Plastic Container
La solution prémélangée de cléocine phosphate IV concerne l'administration intraveineuse à l'aide d'un équipement stérile. Vérifiez fermement les fuites de minuscules en serrant fermement. Si les fuites se trouvent à défaussez la solution car la stérilité peut être altérée. N'ajoutez pas de médicaments supplémentaires. Les médicaments parentéraux doivent être inspectés visuellement pour les particules et la décoloration avant l'administration chaque fois que la solution et le permis de conteneur. Ne pas utiliser à moins que la solution ne soit claire et que le sceau soit intact.
Prudence
N'utilisez pas de contenants en plastique dans les connexions en série. Une telle utilisation pourrait entraîner l'embolie d'air en raison du fait que l'air résiduel est tiré du récipient principal avant l'administration du liquide du conteneur secondaire est terminé.
Préparation de l'administration
- Suspendre le conteneur à partir du support des œillets.
- Retirez le protecteur du port de sortie en bas du conteneur.
- Joindre le jeu d'administration. Reportez-vous à l'ensemble des directions complètes.
Préparation du phosphate de cléocine dans le système de survie complémentaire - .Pour IV Utilisation uniquement. Phosphate de cléocine 300 mg 600 mg et 900 mg peut être reconstitué dans 50 ml (pour 300 mg et 600 mg) ou 100 ml (pour 900 mg) d'injection de dextrose à 5% ou injection de chlorure de sodium 0,9% dans le récipient addile. Reportez-vous à des instructions distinctes pour le système de surface complémentaire.
Comment fourni
Chaque ml de Cléocine phosphate La solution stérile contient du phosphate de clindamycine équivalent à 150 mg de clindamycine 0,5 mg d'aménagement de disodium édétét 9,45 mg d'alcool benzylique ajouté comme conservateur. Lorsque le pH nécessaire est ajusté avec l'hydroxyde de sodium et / ou l'acide chlorhydrique. Le phosphate de cléocine est disponible dans les packages suivants:
25-2 ml de flacons NDC 0009-0870-26
25 à 4 ml de flacons NDC 0009-0775-26
25 à 6 ml de flacons NDC 0009-0902-18
Ensemble en vrac de pharmacie de 5-60 ml NDC 0009-0728-09
Cléocine phosphate est fourni dans les flacons complémentaires comme suit:
| NDC | Taille du flacon | Total de clindamycine phosphate / flacon |
| 0009-6582-01 | 25-2 ml de flacons | 300 mg |
| 0009-3124-03 | 25 à 4 ml de flacons | 600 mg |
| 0009-3447-03 | 25 à 6 ml de flacons | 900 mg |
Conserver à température ambiante contrôlée de 20 ° à 25 ° C (68 ° à 77 ° F) [voir USP].
Cléocine phosphate IV Solution Dans la galaxie, les conteneurs en plastique sont une solution stérile de phosphate de clindamycine avec 5% de dextrose. Les contenants en plastique Galaxy à dose unique sont disponibles comme suit:
CONTEURS DE 24-300 MG / 50 ML NDC 0009-3381-02
CONTEURS DE 24 à 600 mg / 50 ml NDC 0009-3375-02
CONTEURS DE 24 à 900 mg / 50 ml NDC 0009-3382-02
L'exposition des produits pharmaceutiques à la chaleur doit être minimisée. Il est recommandé que les conteneurs en plastique Galaxy soient stockés à température ambiante (25 ° C). Évitez les températures supérieures à 30 ° C.
Distribué par: Pfizer Pharmacia
Effets secondaires for Cleocin I.V.
Les réactions suivantes ont été rapportées avec l'utilisation de la clindamycine.
Infections et infestations: Clostridium difficile colite
Gastro-intestinal: Colite associée aux antibiotiques (voir AVERTISSEMENTS ) Pseudomembranous Colite Douleur abdominale Nausée et vomissements. Le début des symptômes de colite pseudomembranous peut se produire pendant ou après un traitement antibactérien (voir AVERTISSEMENTS ). An unpleasant or metallic taste has been reported after intravenous administration of èmee higher doses of clindamycin phosphate.
Réactions d'hypersensibilité: Des éruptions maculopapulaires et de l'urticaire ont été observées pendant le traitement médicamenteux. Les éruptions cutanées de type morbilliforme légères généralisées à modérées sont les plus fréquemment rapportées de toutes les effets indésirables.
Des réactions cutanées sévères telles que la nécrolyse épidermique toxique certains avec des résultats mortels ont été signalés (voir AVERTISSEMENTS ). Cases of Acute Généralized Exanèmeematous Pustulosis (AGEP) eryèmeema multiforme some resembling Stevens-Johnson syndrome have been associated wième clindamycin. Anaphylactic shock anaphylactic reaction and hypersensitivity have also been reported (voir AVERTISSEMENTS ).
Peau et muqueuses: Prurit vaginite angio-œdème et rares instances de dermatite exfoliative ont été signalées (voir Réactions d'hypersensibilité ).
Foie: La jaunisse et les anomalies des tests de fonction hépatique ont été observées pendant le traitement par la clindamycine.
Rénal: Bien qu'aucune relation directe de la clindamycine avec les dommages rénales n'ait été établie une dysfonction rénale comme en témoigne l'azotémie oligurie et / ou la protéinurie.
Hématopoïétique: La neutropénie transitoire (leukopénie) et l'éosinophilie ont été signalées. Des rapports d'agranulocytose et de thrombocytopénie ont été faits. Aucune relation étiologique directe à la thérapie simultanée de la clindamycine n'a pu être établie dans l'une des précédentes.
Système immunitaire: Des cas de réaction médicamenteuse avec l'éosinophilie et les symptômes systémiques (robe) ont été signalés.
Réactions locales: L'induration de la douleur d'irritation du site d'injection et un abcès stérile ont été signalés après injection intramusculaire et thrombophlebititis après perfusion intraveineuse. Les réactions peuvent être minimisées ou évitées en donnant des injections intramusculaires profondes et en évitant une utilisation prolongée de cathéters intraveineux à séduction.
Musculo-squelette: Des cas de polyarthrite ont été signalés.
Cardiovasculaire: Une arrestation et une hypotension cardiopulmonaires ont été signalées après une administration intraveineuse trop rapide (voir Posologie et administration ).
Interactions médicamenteuses for Cleocin I.V.
Il a été démontré que la clindamycine a des propriétés de blocage neuromusculaires qui peuvent améliorer l'action d'autres agents de blocage neuromusculaires. Par conséquent, il doit être utilisé avec prudence chez les patients recevant de tels agents.
choses à faire au Vietnam
La clindamycine est métabolisée principalement par le CYP3A4 et dans une moindre mesure par le CYP3A5 vers le métabolite majeure de la clindamycine sulfoxyde et le métabolite mineur N-déméthylclindamycine. Par conséquent, les inhibiteurs du CYP3A4 et du CYP3A5 peuvent augmenter les concentrations plasmatiques de clindamycine et les inducteurs de ces isoenzymes peuvent réduire les concentrations plasmatiques de clindamycine. En présence de forts inhibiteurs du CYP3A4 surveillent les effets indésirables. En présence de forts inducteurs CYP3A4 tels que le moniteur de rifampicine pour la perte d'efficacité.
In vitro Des études indiquent que la clindamycine n'inhibe pas CYP1A2 CYP2C9 CYP2C19 CYP2E1 ou CYP2D6 et inhibe uniquement modérément CYP3A4.
L'antagonisme a été démontré entre la clindamycine et l'érythromycine in vitro . En raison de la signification clinique possible, les deux médicaments ne doivent pas être administrés simultanément.
Avertissements for Cleocin I.V.
Voir Avertissement de boîte .
Clostridium Difficile Associated Diarrhea
Clostridium difficile La diarrhée associée (CDAD) a été signalée avec l'utilisation de presque tous les agents antibactériens, y compris le cléocine phosphate, et peut aller de la gravité de la diarrhée légère à la colite mortelle. Le traitement avec des agents antibactériens modifie la flore normale du côlon conduisant à la prolifération de C. difficile .
C. difficile produit des toxines A et B qui contribuent au développement de la CDAD. Hypertoxine produisant des souches de C. difficile provoquer une morbidité et une mortalité accrues car ces infections peuvent être réfractaires en thérapie antimicrobienne et peuvent nécessiter une colectomie. La CDAD doit être considérée chez tous les patients qui présentent une diarrhée après une utilisation antibiotique. Des antécédents médicaux attentifs sont nécessaires car la CDAD se produirait sur deux mois après l'administration d'agents antibactériens.
Si la CDAD est suspectée ou confirmée l'utilisation d'antibiotiques en cours non dirigée contre C. difficile peut avoir besoin d'être interrompu. Supplémentation des protéines de fluide et d'électrolyte appropriée Traitement antibiotique de C. difficile et l'évaluation chirurgicale doit être instituée comme indiqué cliniquement.
Réactions d'hypersensibilité anaphylactiques et sévères
Des chocs anaphylactiques et des réactions anaphylactiques ont été signalés (voir Effets indésirables ).
Des réactions d'hypersensibilité sévères, y compris des réactions cutanées graves, telles que la nécrolyse épidermique toxique (dix) réaction médicamenteuse avec l'éosinophilie et les symptômes systémiques (robe) et le syndrome de Stevens-Johnson (SJS) certains ayant des résultats mortels ont été signalés (voir (voir Effets indésirables ).
Dans le cas d'une telle réaction d'hypersensibilité anaphylactique ou sévère, arrêtez le traitement de façon permanente et instituent un traitement approprié.
Une enquête minutieuse doit être faite concernant les sensibilités antérieures aux médicaments et aux autres allergènes.
Toxicité de l'alcool benzylique chez les patients pédiatriques (syndrome de halètement)
Ce produit contient de l'alcool benzylique comme conservateur. L'alcool benzylique conservateur a été associé à des événements indésirables graves, notamment le syndrome du GGASPing et la mort chez les patients pédiatriques. Bien que les doses thérapeutiques normales de ce produit fournissent normalement des quantités d'alcool benzylique qui sont sensiblement inférieures à celles rapportées en association avec le syndrome d'ASPPE, la quantité minimale d'alcool benzylique où peut se produire est connue.
Le risque de toxicité d'alcool benzylique dépend de la quantité administrée et de la capacité du foie et des reins à détoxifier le produit chimique. Les nourrissons prématurés et à faible poids à la naissance peuvent être plus susceptibles de développer une toxicité.
Utilisation de la méningite
Étant donné que la clindamycine ne se diffuse pas adéquatement dans le liquide céphalo-rachidien, le médicament ne doit pas être utilisé dans le traitement de la méningite.
Précautions for Cleocin I.V.
Général
L'examen de l'expérience à ce jour suggère qu'un sous-groupe de patients plus âgés atteints d'une maladie grave associée peut tolérer moins bien la diarrhée. Lorsque la clindamycine est indiquée chez ces patients, ils doivent être soigneusement surveillés pour le changement de la fréquence intestinale.
Cléocine phosphate products should be prescribed wième caution in individuals wième a history of gastrointestinal disease particularly colite.
Cléocine phosphate should be prescribed wième caution in atopic individuals.
Certaines infections peuvent nécessiter une incision et un drainage ou d'autres procédures chirurgicales indiquées en plus de l'antibiothérapie.
L'utilisation du phosphate de cléocine peut entraîner une prolifération d'organismes non sensibles aux levures en particulier. Si des surinfections se produisent des mesures appropriées doivent être prises comme indiqué par la situation clinique.
Cléocine phosphate should not be injected intravenously undiluted as a bolus but should be infused over at least 10-60 minutes as directed in èmee Posologie et administration section.
La modification du dosage de la clindamycine peut ne pas être nécessaire chez les patients atteints d'une maladie rénale. Chez les patients atteints d'une prolongation de maladie hépatique modérée à sévère, une demi-vie de clindamycine a été trouvée. Cependant, il a été postulé à partir d'études qui, lorsqu'elles sont données toutes les huit heures, l'accumulation devraient rarement se produire. Par conséquent, la modification de la posologie chez les patients atteints d'une maladie du foie peut ne pas être nécessaire. Cependant, des déterminations périodiques des enzymes hépatiques doivent être faites lors du traitement des patients atteints d'une maladie hépatique sévère.
Il est peu probable que la prescription de cléocine phosphate en l'absence d'une infection bactérienne éprouvée ou fortement suspectée ou d'une indication prophylactique offrirait un bénéfice au patient et augmente le risque de développement de bactéries antidroélectriques.
Informations pour les patients
Les patients doivent être informés que les médicaments antibactériens, y compris le phosphate de cléocine, ne doivent être utilisés que pour traiter les infections bactériennes. Ils ne traitent pas les infections virales (par exemple le rhume). Lorsque le phosphate de cléocine est prescrit pour traiter une infection bactérienne, il convient de dire que, bien qu'il soit courant de se sentir mieux au début du traitement, le médicament doit être pris exactement comme indiqué. Sauter les doses ou ne pas terminer le cours complet du traitement peut (1) diminuer l'efficacité du traitement immédiat et (2) augmenter la probabilité que les bactéries développent une résistance et ne seront pas traitées par la cléocine phosphate ou d'autres médicaments antibactériens à l'avenir.
La diarrhée est un problème courant causé par les antibiotiques qui se termine généralement lorsque l'antibiotique est interrompu. Parfois, après avoir commencé le traitement avec des antibiotiques, les patients peuvent développer des selles aqueuses et sanglantes (avec ou sans crampes d'estomac et fièvre) même aussi tard que deux mois ou plus après avoir pris la dernière dose de l'antibiotique. Si cela se produit, les patients doivent contacter leur médecin dès que possible.
Tests de laboratoire
Pendant la thérapie prolongée, des tests de fonction hépatique et rénaux périodiques et des numéros sanguins doivent être effectués.
Carcinogenèse Mutagenèse A trouble de la fertilité
Des études à long terme chez les animaux n'ont pas été réalisées avec la clindamycine pour évaluer le potentiel cancérigène. Les tests de génotoxicité effectués comprenaient un test de micronucléus de rat et un test de réversion d'Ames Salmonella. Les deux tests étaient négatifs.
Études de fertilité chez le rat traité par voie orale avec jusqu'à 300 mg / kg / jour (environ 1,1 fois la dose humaine adulte la plus élevée à base de Mg / m 2 ) n'a révélé aucun effet sur la fertilité ou la capacité d'accouplement.
Grossesse
Effets tératogènes
Dans les essais cliniques avec des femmes enceintes, l'administration systémique de clindamycine au cours des deuxième et troisième trimestres n'a pas été associée à une fréquence accrue d'anomalies congénitales.
La clindamycine ne doit être utilisée au cours du premier trimestre de la grossesse uniquement si elle est clairement nécessaire. Il n'y a pas d'études adéquates et bien contrôlées chez les femmes enceintes au cours du premier trimestre de la grossesse. Étant donné que les études de reproduction animale ne sont pas toujours prédictives de la réponse humaine, ce médicament ne doit être utilisé pendant la grossesse que s'il est clairement nécessaire.
Des études de reproduction réalisées chez le rat et les souris en utilisant des doses orales de clindamycine jusqu'à 600 mg / kg / jour (NULL,1 et 1,1 fois la dose humaine adulte la plus élevée à base de mg / m 2 respectivement) ou des doses sous-cutanées de clindamycine jusqu'à 250 mg / kg / jour (NULL,9 et 0,5 fois la dose humaine adulte la plus élevée à la base de mg / m 2 respectivement) n'a révélé aucune preuve de tératogénicité.
Cléocine phosphate Sterile Solution contains benzyl alcohol. Benzyl alcohol can cross èmee placenta. see AVERTISSEMENTS .
Mères qui allaitent
La clindamycine apparaîtrait dans le lait maternel dans la plage de 0,7 à 3,8 mcg / ml à des doses de 150 mg par voie orale à 600 mg par voie intraveineuse. La clindamycine a le potentiel de provoquer des effets indésirables sur la flore gastro-intestinale du nourrisson allaité. Si une clindamycine orale ou intraveineuse est requise par une mère infirmière, ce n'est pas une raison pour interrompre l'allaitement, mais un autre médicament peut être préféré. Surveillez le nourrisson pour d'éventuels effets indésirables sur la flore gastro-intestinale tels que la diarrhée candidose (éruption cutanée de la couche) ou rarement du sang dans les selles indiquant une éventuelle colite associée aux antibiotiques.
Les avantages du développement et de la santé de l'allaitement doivent être pris en compte avec le besoin clinique de la mère de la mère de la mère et tout effet indésirable potentiel sur l'enfant allaité de la clindamycine ou de l'état maternel sous-jacent.
comment obtenir des offres sur les chambres d'hôtel
Usage pédiatrique
Lorsque la solution stérile du cléocine phosphate est administrée à la population pédiatrique (naissance à 16 ans), une surveillance appropriée des fonctions du système d'organe est souhaitable.
Utilisation chez les nouveau-nés et les nourrissons
Ce produit contient de l'alcool benzylique comme conservateur. L'alcool benzylique a été associé à un «syndrome de halètement» mortel chez les nourrissons prématurés. voir AVERTISSEMENTS .
Le potentiel d'effet toxique dans la population pédiatrique à partir de produits chimiques qui peut lixiviation de la préparation IV prémélangée à dose unique dans le plastique n'a pas été évalué. voir AVERTISSEMENTS .
Utilisation gériatrique
Les études cliniques de la clindamycine n'ont pas inclus un nombre suffisant de patients âgés de 65 ans et plus pour déterminer s'ils réagissent différemment des patients plus jeunes. Cependant, d'autres expérience clinique signalée indique que la colite et la diarrhée associées aux antibiotiques (en raison de Clostridium difficile ) Vu en association avec la plupart des antibiotiques se produisent plus fréquemment chez les personnes âgées (> 60 ans) et peuvent être plus graves. Ces patients doivent être soigneusement surveillés pour le développement de la diarrhée.
Les études pharmacocinétiques avec la clindamycine n'ont montré aucune différence cliniquement importante entre les jeunes et les personnes âgées avec une fonction hépatique normale et une fonction rénale normale (ajustée à l'âge) après une administration orale ou intraveineuse.
Informations sur la surdose pour Cléocine I.V.
Une mortalité significative a été observée chez la souris à une dose intraveineuse de 855 mg / kg et chez un rat à une dose orale ou sous-cutanée d'environ 2618 mg / kg. Dans les convulsions des souris et la dépression a été observée.
L'hémodialyse et la dialyse péritonéale ne sont pas efficaces pour éliminer la clindamycine du sérum.
Contre-indications pour Cléocine I.V.
Ce médicament est contre-indiqué chez les personnes ayant des antécédents d'hypersensibilité aux préparations contenant de la clindamycine ou de la lincomycine.
Pharmacologie clinique for Cleocin I.V.
Distribution
Le phosphate de clindamycine biologiquement inactif est converti en clindamycine active. À la fin de la perfusion intraveineuse à court terme, les taux sériques de clindamycine actifs sont atteints.
Après l'injection intramusculaire de la clindamycine phosphate, les niveaux de pic de clindamycine actifs sont atteints dans les 3 heures chez l'adulte et 1 heure chez les patients pédiatriques. Les courbes de niveau sérique peuvent être construites à partir des taux sériques de pic IV comme indiqué dans le tableau 1 par application de demi-vies d'élimination (voir Excrétion ).
Les taux sériques de clindamycine peuvent être maintenus au-dessus du in vitro Concentrations minimales inhibitrices pour la plupart des organismes indiqués par administration de clindamycine phosphate toutes les 8 à 12 heures chez l'adulte et toutes les 6 à 8 heures chez les patients pédiatriques ou par perfusion intraveineuse continue. Un état d'équilibre est atteint par la troisième dose.
Aucun niveau significatif de clindamycine n'est atteint dans le liquide céphalo-rachidien, même en présence de méninges enflammés.
Métabolisme
In vitro Des études sur le foie humain et les microsomes intestinaux ont indiqué que la clindamycine est principalement métabolisée par le cytochrome P450 3A4 (CYP3A4) avec une contribution mineure du CYP3A5 pour former du sulfoxyde de clindamycine et un métabolite mineur N-déméthylclindamynine.
Excrétion
Le phosphate de clindamycine biologiquement inactif disparaît rapidement du sérum; La demi-vie d'élimination moyenne est de 6 minutes; Cependant, la demi-vie de l'élimination sérique de la clindamycine active est d'environ 3 heures chez l'adulte et 2 heures chez les patients pédiatriques.
Populations spéciales
Troubles rénaux / hépatiques
La demi-vie d'élimination de la clindamycine est légèrement augmentée chez les patients présentant une fonction rénale ou hépatique nettement réduite. L'hémodialyse et la dialyse péritonéale ne sont pas efficaces pour éliminer la clindamycine du sérum. Les programmes posologiques n'ont pas besoin d'être modifiés en présence d'une maladie rénale ou hépatique légère ou modérée.
Utilisation chez les personnes âgées
Les études pharmacocinétiques chez les volontaires âgés (61-79 ans) et les jeunes adultes (18-39 ans) indiquent que l'âge seul ne modifie pas la pharmacocinétique de la clindamycine (élimination de la dédouanement du volume de distribution et de zone sous la courbe de concentration sérique) après l'administration IV de phosphate de clindamycine. Après l'administration orale de l'élimination du chlorhydrate de clindamycine, la demi-vie est augmentée à environ 4,0 heures (plage de 3,4 à 5,1 h) chez les personnes âgées, contre 3,2 heures (plage de 2,1 à 4,2 h) chez les jeunes adultes. L'étendue de l'absorption n'est cependant pas différente entre les groupes d'âge et aucune altération de dosage n'est nécessaire pour les personnes âgées avec une fonction hépatique normale et une fonction rénale normale (ajustée à l'âge) 1 .
Les tests sériques pour la clindamycine active nécessitent un inhibiteur pour éviter in vitro Hydrolyse du phosphate de clindamycine.
Tableau 1. Concentrations sériques moyennes de pic et de creux de clindamycine active après dosage avec du phosphate de clindamycine
| Dosage Regimen | Culminer MCG / ML | Creux MCG / ML |
| Hommes adultes en bonne santé (post-équilibre) | ||
| 10.9 | 2.0 | |
| 10.8 | 1.1 | |
| 14.1 | 1.7 | |
| 9 | ||
| Patients pédiatriques (première dose) * | ||
| 5-7 mg/kg IV in 1 hour | 10 | |
| 5-7 mg/kg IM | 8 | |
| 3-5 mg/kg IM | 4 | |
| * Données dans ce groupe des patients traités pour une infection. |
Microbiologie
Mécanisme d'action
La clindamycine inhibe la synthèse des protéines bactériennes en se liant à l'ARN 23S de la sous-unité des années 50 du ribosome. La clindamycine est bactériostatique.
La résistance à la résistance à la clindamycine est le plus souvent causée par la modification de bases spécifiques de l'ARN ribosomal 23S. La résistance croisée entre la clindamycine et la lincomycine est terminée. Étant donné que les sites de liaison de ces médicaments antibactériens se chevauchent une résistance croisée est parfois observé chez les macrolides de linosamides et la streptogramme inductible par la streptogramme du b. macrolide à la clindamycine se produit dans certains isolats de bactéries résistantes au macrolide. Les isolats résistants au macrolide de staphylocoques et de streptocoques bêta-hémolytiques doivent être dépistés pour l'induction de la résistance à la clindamycine à l'aide du test de la zone D.
Activité antimicrobienne
La clindamycine s'est avérée active contre la plupart des isolats des micro-organismes suivants in vitro et dans les infections cliniques comme décrit dans le Indications et utilisation section.
Bactéries à Gram positif
Staphylococcus aureus (souches sensibles à la méthicilline)
Streptococcus pneumoniae (souches sensibles à la pénicilline)
Streptococcus pyogenes
Bactéries anaérobies
Clostridium perfringens
Fusobacterium necrophorum
Fusobacterium nuleatum
Peptostreptococcus anaerobius
Prevotella melaninogenica
Au moins 90% des micro-organismes énumérés ci-dessous in vitro Les concentrations minimales inhibiteurs (MICS) inférieures ou égales au point de rupture du micro sensible à la clindamycine pour les organismes d'un type similaire à celles montrées dans le tableau 2. Cependant, l'efficacité de la clindamycine dans le traitement des infections cliniques en raison de ces micro-organismes n'a pas été établie dans des essais cliniques adéquats et bien comprimés.
Bactéries à Gram positif
Staphylococcus epidermidis (souches sensibles à la méthicilline)
Streptococcus agalactiae
Streptococcus dégoulinant
Streptococcus doux
Streptococcus oral
Bactéries anaérobies
Actinomyces israélii
Clostridium clostridioforme
Eggerthella Lenta
Finegoldia (peptostreptococcus) grand
Micromonas (peptostreptococcus) micros
Bivia Prevotella
Intermedia Previtella
Propionibacterium acnes
Méthodes de test de sensibilité
Lorsqu'il est disponible, le laboratoire de microbiologie clinique devrait fournir cumulatif in vitro Résultats des tests de sensibilité pour les médicaments antimicrobiens utilisés dans les hôpitaux locaux et les zones de pratique au médecin comme rapports périodiques qui décrivent le profil de sensibilité des agents pathogènes nosocomiaux et acquis à la communauté. Ces rapports devraient aider le médecin à sélectionner un médicament antibactérien pour le traitement.
Techniques de dilution
Des méthodes quantitatives sont utilisées pour déterminer les concentrations inhibiteurs minimums antimicrobiennes (CMI). Ces CMI fournissent des estimations de la sensibilité des bactéries aux composés antimicrobiens. Les micros doivent être déterminés à l'aide d'une méthode de test standardisée 23 (bouillon et / ou gélose). Les valeurs du CMI doivent être interprétées en fonction des critères fournis dans le tableau 2.
Diffusion Techniques
Les méthodes quantitatives qui nécessitent la mesure des diamètres de zone peuvent également fournir des estimations reproductibles de la sensibilité des bactéries aux composés antimicrobiens. La taille de la zone doit être déterminée à l'aide d'une méthode standardisée 25 . Cette procédure utilise des disques papier imprégnés de 2 mcg de clindamycine pour tester la sensibilité des bactéries à la clindamycine. Les points d'arrêt de diffusion du disque sont fournis dans le tableau 2.
Techniques anaérobies
Pour les bactéries anaérobies, la sensibilité à la clindamycine peut être déterminée par une méthode de test standardisée 24 . Les valeurs MIC obtenues doivent être interprétées en fonction des critères fournis dans le tableau 2.
Tableau 2. Critères d'interprétation des tests de sensibilité pour la clindamycine
| Pathogène | Critères d'interprétation de la sensibilité | |||||
| Concentrations inhibiteurs minimales (Micro dans MCG / ML) | Diffusion du disque (Diamètres de zone en mm) | |||||
| S | I | R | S | I | R | |
| Staphylococcus spp. | ≤0,5 | 1-2 | ≥4 | ≥21 | 15-20 | ≤14 |
| Streptococcus pneumoniae et d'autres Streptocoque spp. | ≤0,25 | 0.5 | ≥1 | ≥19 | 16-18 | ≤15 |
| Bactéries anaérobies | ≤2 | 4 | ≥8 | N / A | N / A | N / A |
| N / A=not applicable |
Un rapport de Susceptible (s) indique que le médicament antimicrobien est susceptible d'inhiber la croissance de l'agent pathogène si le médicament antimicrobien atteint la concentration généralement réalisable au site d'infection. Un rapport de Intermédiaire (i) indique que le résultat doit être considéré comme équivoque et si le micro-organisme n'est pas entièrement sensible aux alternatifs cliniquement réalisables, le test doit être répété. Cette catégorie implique une applicabilité clinique possible dans les sites corporels où le médicament est physiologiquement concentré ou dans des situations où une dose élevée de médicament peut être utilisée. Cette catégorie fournit également une zone tampon qui empêche de petits facteurs techniques incontrôlés de provoquer des écarts majeurs dans l'interprétation. Un rapport de Résistant (R) indique que le médicament antimicrobien est peu susceptible d'inhiber la croissance de l'agent pathogène si le médicament antimicrobien atteint la concentration généralement réalisable au site d'infection; Une autre thérapie doit être sélectionnée.
Contrôle de qualité
Les procédures de test de sensibilité standardisé nécessitent l'utilisation de contrôles de laboratoire pour surveiller et assurer la précision et la précision des fournitures et réactifs utilisés dans le test et les techniques des individus effectuant le test 2345 . La poudre de clindamycine standard devrait fournir les plages de micro dans le tableau 3. Pour la technique de diffusion du disque à l'aide du disque de clindamycine à 2 mcg, les critères fournis dans le tableau 2 doivent être obtenus.
Tableau 3. Gabrins de contrôle de la qualité acceptables pour la clindamycine
| Souche QC | GAMMES DE CONTRÔLE DE LA qualité acceptable | |
| Plage de concentration inhibitrice minimale (MCG / ML) | Diffusion du disque Range (Diamètres de zone en mm) | |
| Enterococcus faecalis 1 ATCC 29212 | 4-16 | N / A |
| Staphylococcus aureus ATCC 29213 | 06-0.25 | N / A |
| Staphylococcus aureus ATCC 25923 | N / A | 24-30 |
| Streptococcus pneumoniae ATCC 49619 | 0,03-0.12 | 19-25 |
| Bacteroides fragilis ATCC 25285 | 0,5-2 | N / A |
| Bacteroides thétaiotaomicron ATCC 29741 | 2-8 | N / A |
| Clostridium difficile 2 ATCC 700057 | 2-8 | N / A |
| Eggerthella Lenta ATCC 43055 | 06-0.25 | N / A |
| 1. Enterococcus faecalis a été inclus dans ce tableau à des fins de contrôle de la qualité uniquement. 2. Contrôle de la qualité pour C. difficile est effectué en utilisant la méthode de dilution d'agar, seuls tous les autres anaérobies obligatoires peuvent être testés par la microdilution du bouillon ou les méthodes de dilution d'agar. N / A=Not applicable ATCC ® est une marque déposée de la collection américaine de la culture de type |
Références
1. Smith RB Phillips JP: Évaluation du cleocine HCl et du phosphate de cléocine dans une population âgée. Upjohn Tr 8147-82-9122-021 décembre 1982.
2. ClSi. Normes de performance pour les tests de sensibilité aux antimicrobiens: 26 ème éd. CLSI Supplément M100S. Wayne PA: Institut des normes cliniques et de laboratoire; 2016.
3. ClSi. Méthodes de dilution Tests de sensibilité aux antimicrobiens pour les bactéries qui poussent aérobiement; Norme approuvée -Tent édition. Document CLSI M07-A10. Wayne PA: Institut des normes cliniques et de laboratoire; 2015.
4. ClSi. Méthodes de test de sensibilité aux antimicrobiens des bactéries anaérobies; Édition standard approuvée. Document CLSI M11-A8. Wayne PA: Institut des normes cliniques et de laboratoire; 2012.
5. ClSi. Normes de performance pour les tests de sensibilité aux disques antimicrobiens; Édition standard approuvée. Document CLSI M02-A12. Wayne PA: Institut des normes cliniques et de laboratoire; 2015.
Informations sur les patients pour Cléocine I.V.
Les patients doivent être informés que les médicaments antibactériens, y compris le phosphate de cléocine, ne doivent être utilisés que pour traiter les infections bactériennes. Ils ne traitent pas les infections virales (par exemple le rhume). Lorsque le phosphate de cléocine est prescrit pour traiter une infection bactérienne, il convient de dire que, bien qu'il soit courant de se sentir mieux au début du traitement, le médicament doit être pris exactement comme indiqué. Sauter les doses ou ne pas terminer le cours complet du traitement peut (1) diminuer l'efficacité du traitement immédiat et (2) augmenter la probabilité que les bactéries développent une résistance et ne seront pas traitées par la cléocine phosphate ou d'autres médicaments antibactériens à l'avenir.
La diarrhée est un problème courant causé par les antibiotiques qui se termine généralement lorsque l'antibiotique est interrompu. Parfois, après avoir commencé le traitement avec des antibiotiques, les patients peuvent développer des selles aqueuses et sanglantes (avec ou sans crampes d'estomac et fièvre) même aussi tard que deux mois ou plus après avoir pris la dernière dose de l'antibiotique. Si cela se produit, les patients doivent contacter leur médecin dès que possible.
Instructions pour une utilisation pour le système de surface complémentaire. Pour l'utilisation IV uniquement
Cléocine phosphate ®
Solution stérile de clindamycine pour l'injection USP
en avant-avant ® Ampoule
Pour ouvrir un conteneur diluant:
Peler l'écrasement du coin et retirer le récipient. Une certaine opacité du plastique due à l'absorption d'humidité pendant le processus de stérilisation peut être observée. Ceci est normal et n'affecte pas la qualité ou la sécurité de la solution. L'opacité diminuera progressivement.
Suprax Suspension nécessite quelle étiquette auxiliaire
Pour assembler le flacon et le récipient diluant flexible:
(Utilisez la technique aseptique)
- Retirez les couvercles de protection du haut du flacon et du port de flacon sur le récipient de diluant comme suit:
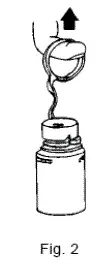
- Pour retirer le capuchon de flacon de rupture, balancez l'anneau de traction sur le haut du flacon et tirez suffisamment loin pour démarrer l'ouverture (voir figure 1.) Ensuite, tirez droit vers le haut pour retirer le capuchon. (Voir figure 2.) NOTE: Une fois que le capuchon de rupture a été supprimé N'accès pas à du flacon avec la seringue.
- Pour retirer le couvercle du port de flacon, saisissez l'onglet sur l'anneau de traction, tirez vers le haut pour casser les trois chaînes d'attache, puis retirez pour retirer le couvercle. (Voir figure 3.)

- Vissez le flacon dans le port du flacon jusqu'à ce qu'il n'ira pas plus loin. Le flacon doit être vissé étroitement pour assurer un joint. Cela se produit environ 1/2 tour (180 °) après le premier clic audible. (Voir Figure 4.) Le son de clic n'assure pas un sceau; Le flacon doit être tourné aussi loin qu'il ira. NOTE: Une fois le flacon assis, n'essayez pas de le retirer. (Voir figure 4.)
- Revérifiez le flacon pour vous assurer qu'il est serré en essayant de le retourner davantage dans le sens de l'assemblage.
- Étiqueter de manière appropriée.
 |
 |
Pour préparer le mélange:
- Pressez doucement le bas du récipient de diluant pour gonfler la partie du récipient entourant l'extrémité du flacon médicamenteux.
- Avec l'autre main, poussez le flacon de médicament dans le récipient télescopique des parois du récipient. Saisissez le capuchon intérieur du flacon à travers les parois du récipient. (Voir figure 5.)
- Tirez le capuchon intérieur du flacon médicamenteux. (Voir Figure 6.) Vérifiez que le bouchon en caoutchouc a été retiré permettant au médicament et au diluant de se mélanger.
- Mélanger soigneusement le contenu des conteneurs et utiliser dans le délai spécifié.
 |
 |
Préparation de l'administration: (Utilisez la technique aseptique)
- Confirmez l'activation et le mélange du contenu du flacon.
- Vérifiez fermement les fuites en serrant fermement. Si les fuites se trouvent l'unité de défausse car la stérilité peut être altérée.
- Closez la pince de contrôle de débit de l'ensemble d'administration.
- Retirez le couvercle du port de sortie en bas du conteneur.
- Insérez la broche de perçage de l'administration dans le port avec un mouvement de torsion jusqu'à ce que la broche soit fermement assise. Remarque: Voir les directions complètes sur le coffre d'administration.
- Soulevez l'extrémité libre de la boucle de cintre au bas du flacon brisant les deux cordes à cravate. Pliez la boucle vers l'extérieur pour le verrouiller en position verticale, puis suspendre le conteneur du cintre.
- Pressez et libérez la chambre à goutte pour établir un niveau de fluide approprié dans la chambre.
- Pince de commande de débit ouvrir et clair de l'air de l'ensemble. Close Clamp.
- Attachez le réglage sur le dispositif Venipuncture. Si l'appareil ne fait pas de séjour à Prime et ne fait pas la ponction veineuse.
- Réguler le taux d'administration avec une pince de contrôle de débit.
AVERTISSEMENT: Do not use flexible container in series connections.


