Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Dérivés d'ergotVraie vraie
Résumé
Qu'est-ce que Trudhesa?
Le spray nasal Trudhesa (mésylate de dihydroergotamine) est un dérivé d'ergotamine utilisé pour traiter la migraine avec ou sans aura chez l'adulte.
Quels sont les effets secondaires de Trudhesa?
Vraie vraie
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- rythme cardiaque lent ou rapide
- faiblesse des jambes
- Douleur musculaire dans les bras ou les jambes
- picotements ou engourdissement
- froideur dans les mains et les pieds
- doigts bleus et orteils
- douleur à l'estomac sévère
- mâchoire ou douleur au bras gauche
- douleur à la poitrine ou pression
- fatigue soudaine
- faiblesse d'un côté du corps
- Diagramme à parler
- changements de vision
- changements mentaux ou d'humeur
- confusion
- éruption cutanée
- démangeaisons et
- étourdissements sévères
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires de Trudhesa comprennent:
- nez qui coule
- nausée
- altéré sens de goût
- Réactions du site d'application
- vertiges
- vomissement
- somnolence
- mal de gorge et
- diarrhée.
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; Et des étourdissements soudains étourdissement ou s'évanouir;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Trudhesa
La dose recommandée de pulvérisation nasale de Trudhesa est de 1,45 mg (administrée comme un spray mètre de 0,725 mg dans chaque narine). La dose peut être répétée si nécessaire au moins 1 heure après la première dose.
Trudhesa chez les enfants
La sécurité et l'efficacité du spray nasal de Trudhesa sont chez les patients pédiatriques n'ont pas été établies.
Quelles substances ou suppléments de médicaments interagissent avec Trudhesa?
Le spray nasal de Trudhesa peut interagir avec d'autres médicaments tels que:
- bêta-bloquants
- nicotine
- inhibiteur sélectif de la recapture de la sérotonine ( Si ) antidépresseurs (par exemple, fluoxetine fluvoxamine paroxétine sertraline)
- Inhibiteurs de la protéase (par exemple Ritonavir Nelfinavir indinavir)
- macrolide Antibiotiques (par exemple érythromycine clarithromycine)
- antifongiques (par exemple le kétoconazole itraconazole)
- triptans et
- Vasoconstricteurs.
Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Trudhesa pendant la grossesse et l'allaitement
Dites à votre médecin si vous êtes enceinte ou prévoyez de tomber enceinte avant d'utiliser un spray nasal Trudhesa. Il peut augmenter le risque d'accouchement prématuré et peut nuire à un fœtus. On ne sait pas si le pulvérisation nasale de Trudhesa passe dans le lait maternel; Cependant, l'ergotamine, un médicament connexe est présent dans le lait maternel. En raison du potentiel de réduction de l'approvisionnement en lait et d'événements indésirables graves chez le nourrisson allaité, y compris la diarrhée, les vomissements faibles et l'allaitement maternel de la pression artérielle ne sont pas recommandés pendant le traitement avec un spray nasal Trudhesa et pendant 3 jours après la dernière dose. L'alimentation du lait maternel pendant cette période doit être pompée et jetée.
Informations Complémentaires
Notre Trudhesa (Mesylate de dihydroergotamine) Nasal Spray Effets Centre de médicaments fournit une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Ce n'est pas une liste complète des effets secondaires et d'autres peuvent survenir. Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Contre-indications
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Ischémie périphérique à la suite de la co-administration avec de forts inhibiteurs du CYP3A4
Une ischémie périphérique grave et / ou mortelle a été associée à la co-administration de dihydroergotamine avec de forts inhibiteurs du CYP3A4. Étant donné que l'inhibition du CYP3A4 augmente les taux sériques de dihydroergotamine, le risque de vasospasme conduisant à une ischémie cérébrale et / ou à une ischémie des extrémités est augmentée. Par conséquent, l'utilisation concomitante de Trudhesa avec de forts inhibiteurs du CYP3A4 est contre-indiqué [voir Contre-indications AVERTISSEMENTS AND PRECAUTIONS et Interactions médicamenteuses ].
Description de Trudhesa
Le spray nasal Trudhesa (mésylate de dihydroergotamine) est un produit combiné de médicament à dose unique contenant un constituant de médicament contre le mésylate de dihydroergotamine et un constituant de dispositif de pulvérisation nasal.
Le nom chimique du mésylate de dihydroergotamine est l'ergotaman-3 '6' 18-triron 910-dihydro- 12'-hydroxy-2'-méthyl-5'- (phénylméthyl) - (5'a) - monométhanesulfonate. Son poids moléculaire est de 679,78 et sa formule moléculaire est C 33 H 37 N 5 O 5 • ch 4 O 3 S.
La structure chimique est:
 |
Le constituant du médicament est une solution de mésylate de dihydroergotamine. Chaque millilitre (ml) de solution contient du mésylate de dihydroergotamine 4,0 mg (équivalent à 3,43 mg de dihydroergotamine) et les ingrédients inactifs suivants: de la caféine (NULL,0 mg) de dioxyde de carbone (q.s.) dextrose (NULL,0 mg) et d'eau (q.s. à 1,0 ml).
Spray nasal Trudhesa après assemblage et amorçage délivre 0,725 mg de mésylate de dihydroergotamine par pulvérisation. Une dose totale de 1,45 mg de mésylate de dihydroergotamine est délivrée dans 2 sprays. Le dispositif de pulvérisation nasal contient l'hydrofluoroalkane-134a (HFA) propulseur.
Utilisations pour Trudhesa
Trudhesa est indiqué pour le traitement aigu de la migraine avec ou sans aura chez l'adulte.
Limitations d'utilisation
Trudhesa n'est pas indiqué pour le traitement préventif de la migraine.
Trudhesa n'est pas indiqué pour la gestion de la migraine hémiplégique ou basilaire.
Dosage pour Trudhesa
Dossing Information
La dose recommandée de Trudhesa est de 1,45 mg administrée sous forme de deux vaporisateurs de compteurs dans le nez (un spray de 0,725 mg dans chaque narine).
La dose peut être répétée si nécessaire au moins 1 heure après la première dose. N'utilisez pas plus de 2 doses de Trudhesa dans une période de 24 heures ou 3 doses dans un délai de 7 jours.
Évaluation avant la première dose
Avant le début de Trudhesa, une évaluation cardiovasculaire est recommandée [voir AVERTISSEMENTS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Instructions d'administration importantes
Trudhesa est pour l'administration nasale uniquement et ne doit pas être injecté.
Trudhesa doit être assemblé avant l'utilisation (voir Instructions pour une utilisation ). Utilisez ou jetez Trudhesa dans les 8 heures une fois le flacon ouvert ou que le produit a été assemblé.
Amencez le Trudhesa assemblé avant l'utilisation initiale en libérant 4 sprays. Utilisez Trudhesa immédiatement après l'amorçage. Jetez Trudhesa immédiatement après utilisation. Ouvrez et préparez un nouveau Trudhesa si une dose supplémentaire est nécessaire.
Comment fourni
Formes et forces posologiques
Le spray nasal Trudhesa (mésylate de dihydroergotamine) est un produit combiné de médicament à dose unique contenant un flacon de mésylate de dihydroergotamine avec une solution claire et incolore à légèrement jaune et un dispositif d'administration intranasal. Chaque pulvérisation délivre 0,725 mg de mésylate de dihydroergotamine.
Trudhesa (mésylate de dihydroergotamine) Spray nasal (NULL,725 mg par pulvérisation) est fourni comme un ensemble de 4 unités à dose unique ( NDC 77530-725-04). Chaque unité à dose unique contient:
- Un flacon en verre ambre ( NDC 77530-725-01) contenant 4 mg de mésylate de dihydroergotamine dans une solution claire et incolore à 1 ml. Le bouchon n'est pas fait avec du latex en caoutchouc naturel.
- Un dispositif de pulvérisation nasal.
Stockage et manipulation
Conservez Trudhesa à température ambiante contrôlée de 20 ° C à 25 ° C (68 ° F à 77 ° F) avec des excursions autorisées entre 15 ° C à 30 ° C (59 ° F à 86 ° F). Ne réfrigérez ni ne congelez.
Fabriqué par: Mipharm S.P.A. Milano Italie. Révisé: septembre 2021
Effets secondaires for Trudhesa
Les effets indésirables cliniquement significatifs suivants sont décrits ailleurs dans l'étiquetage:
- Ischémie périphérique à la suite de la co-administration avec de forts inhibiteurs du CYP3A4 [voir Avertissement de boîte et AVERTISSEMENTS AND PRECAUTIONS ]
- Ischémie myocardique et / ou infarctus d'autres événements et décès cardiaques indésirables [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Réactions et décès indésirables cérébrovasculaires [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Autres réactions indésirables liées au vasospasme [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Augmentation de la pression artérielle [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Mélange de surutilisation des médicaments [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Travail prématuré [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Complications fibrotiques [voir AVERTISSEMENTS AND PRECAUTIONS ]
- Irritation locale [voir AVERTISSEMENTS AND PRECAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions de réaction indésirables très variables observées dans les essais cliniques d'un médicament ne peuvent pas être directement comparées aux taux dans les essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans la pratique.
Réactions indésirables dans les essais contrôlés par placebo avec pulvérisation nasale de mésylate de dihydroergotamine (DHE) [voir Études cliniques ]
Sur les 1796 patients et sujets traités avec des doses de pulvérisation nasale de DHE 2 mg ou moins dans les études cliniques américaines et étrangères 26 (NULL,4%) ont été interrompues en raison d'événements indésirables. Les événements indésirables associés à l'arrêt étaient dans l'ordre de fréquence diminué: la rhinite (13) étourdissements (2) œdème facial (2) et un patient en raison de sueurs froides traumatismes accidentels Dépression de la chirurgie élective Somnolence Allergie Vomitte d'hypotension et de paraesthésie.
L'augmentin et l'amoxicilline
Le tableau 1 résume les taux d'incidence des effets indésirables rapportés par au moins 1% des patients qui ont reçu un spray nasal DHE pour le traitement de la migraine pendant les études cliniques à doubleblide contrôlées par placebo et étaient plus fréquents que chez les patients recevant un placebo. Les effets indésirables les plus couramment rapportés (plus de 1% des patients qui ont reçu un pulvérisation nasale de DHE) étaient des réactions d'étourdissements altérés par la rhinite de la nausée des nausées de goûts. Dans la plupart des cas, ces événements ont été transitoires et autochtones et n'ont pas entraîné l'arrêt des patients d'une étude.
Tableau 1 Les effets indésirables rapportés par au moins 1% des patients traités par la pulvérisation nasale DHE et se sont produits plus fréquemment que dans le groupe placebo dans les essais contrôlés par le placebo migraine
| Et pulvérisation nasale N = 597 % | Placebo N = 631 % | |
| Système respiratoire | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Système gastro-intestinal | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Sens spéciaux autres | ||
| Altered Sense of Taste | 8 | 1 |
| Site de candidature | ||
| Site de candidature Reaction | 6 | 2 |
| Système nerveux central et périphérique | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Le corps dans son ensemble | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Système musculo-squelettique | ||
| Stiffness | 1 | <1 |
Réactions indésirables dans les études avec Trudhesa
Une étude ouverte chez les adultes (18 à 66 ans) a été menée pour évaluer la sécurité et la tolérabilité de l'utilisation répétée de Trudhesa de Trudhesa a été autorisée au cours de 6 à 12 mois. Au total, 354 patients atteints de migraine ont reçu au moins une dose de Trudhesa. Cent quatre-vingt-cinq patients traités en moyenne au moins deux migraines par mois pendant 6 mois et 55 patients traités en moyenne au moins deux migraines par mois pendant 12 mois. Parmi les patients qui ont reçu au moins une dose de Trudhesa 185 (NULL,3%), les patients ont présenté des symptômes irritatifs locaux. Parmi celles-ci, les symptômes irritatifs locaux les plus courants étaient la nasopharyngite rhinite l'inconfort nasal Produit goûté anormal / dysgéusie sinuste malaise test olfactif test anormal épistaxis pharyngite le changement de trouble muqueux nasal dans l'odorat inconfort et rhinorrhée [voir rhinorrhée [voir AVERTISSEMENTS AND PRECAUTIONS ].
Expérience de commercialisation de la poste
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de mésylate de dihydroergotamine. Parce que ces réactions sont signalées volontairement d'une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à l'exposition au médicament:
Vasospasme patesthésie hypertension étourdie anxiété anxiété dyspnée maux de tête rinçage diarrhée éruption cutanée de transpiration et de fibrose pleurale et rétropéritonéale après une utilisation à long terme de dihydroergotamine. Des cas d'infarctus du myocarde et d'un accident vasculaire cérébral ont été signalés à la suite de l'utilisation de mésylate de dihydroergotamine [voir AVERTISSEMENTS AND PRECAUTIONS ].
Interactions médicamenteuses for Trudhesa
Inhibiteurs du CYP3A4
Il y a eu de rares rapports d'événements indésirables graves en lien avec la co-administration d'administration intraveineuse de dihydroergotamine et de forts inhibiteurs du CYP3A4 tels que les inhibiteurs de protéase (par exemple les antibiotiques de macrolide de ritonavir nelfinavir) et les antifungales (par exemple la kezoonyne-anne à érythromycine) et les antifungales (e.gozoletoletoletoletoly itraconazole) entraînant un vasospasme qui a conduit à l'ischémie cérébrale et / ou à l'ischémie des extrémités [voir AVERTISSEMENTS AND PRECAUTIONS ]. The use of strong CYP3A4 inhibiteurs with dihydroergotamine is contraindicated [see Contre-indications ]. Administer moderate CYP3A4 inhibiteurs (e.g. saquinavir néfazodone fluconazole grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Triptans
Triptans (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm et its effect could be additive with TRUDHESA. Therefore triptans et TRUDHESA should not be taken within 24 heures of each other [see Contre-indications ].
Bêta-bloquants
Il a été rapporté que le propranolol peut potentialiser l'action vasoconstrictive de l'ergotamine en bloquant la propriété vasodilatante de l'épinéphrine.
Vasoconstricteurs
Trudhesa est contre-indiqué pour une utilisation avec des vasoconstricteurs périphériques et centraux car la combinaison peut provoquer une élévation synergique de la pression artérielle [voir AVERTISSEMENTS AND PRECAUTIONS ].
Nicotine
Nicotine may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see AVERTISSEMENTS AND PRECAUTIONS ].
Inhibiteurs sélectifs de la recapture de la sérotonine
Une faiblesse hyperréflexie et incoordination ont été rapportées rarement lorsque le 5-HT 1 Les agonistes ont été co-administrés avec des inhibiteurs sélectifs du recaptage de la sérotonine (par exemple, la fluvoxamine paroxétine de la fluoxétine paroxétine).
Abus de drogues et dépendance
Substance contrôlée
Trudhesa contient de la dihydroergotamine (comme le sel de mésylate) qui n'est pas une substance contrôlée.
Abus
Abus is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Dépendance
La dépendance physique est un état qui se développe à la suite d'une adaptation physiologique en réponse à une consommation répétée de drogues se manifestant par des signes de sevrage et des symptômes après un arrêt abrupte ou une réduction de dose significative d'un médicament. Les données actuellement disponibles n'ont pas démontré de dépendance physique ou psychologique avec la dihydroergotamine. Cependant, des cas de dépendance psychologique chez les patients concernant d'autres formes de thérapie par l'ergot ont été signalés.
Avertissements pour Trudhesa
Inclus dans le cadre du 'PRÉCAUTIONS' Section
Précautions pour Trudhesa
Ischémie périphérique à la suite de la co-administration avec de forts inhibiteurs du CYP3A4
L'ischémie périphérique grave et / ou mortelle a été associée à la co-administration de dihydroergotamine avec de forts inhibiteurs du CYP3A4, y compris des inhibiteurs de protéase, des antibiotiques macrolides et des antifongiques. Étant donné que l'inhibition du CYP3A4 augmente les taux sériques de dihydroergotamine, le risque de vasospasme conduisant à une ischémie cérébrale et / ou à une ischémie des extrémités est augmentée. Par conséquent, l'utilisation concomitante de Trudhesa avec de forts inhibiteurs du CYP3A4 est contre-indiqué [voir Contre-indications et Interactions médicamenteuses ].
Ischémie myocardique et / ou infarctus d'autres effets et décès cardiaques
Il existe le potentiel de réactions cardiaques indésirables avec le traitement à Trudhesa. Des événements cardiaques défavorables graves, dont certains qui ont été mortels, se sont produits après l'utilisation de mésylate de dihydroergotamine. Ces événements ont inclus l'infarctus aigu de l'infarctus du myocarde des perturbations du rythme cardiaque (par exemple la tachycardie ventriculaire et la fibrillation ventriculaire) artère coronarienne vasospasm et ischémie myocardique transitoire.
Avant l'initiation de Trudhesa, une évaluation cardiovasculaire est recommandée pour déterminer si le patient est exempt d'artère coronaire et d'une maladie myocardique ischémique ou d'une autre maladie cardiovasculaire sous-jacente importante. Si pendant l'évaluation cardiovasculaire, les antécédents médicaux du patient (y compris les facteurs de risque) ou les résultats de l'enquête électrocardiographique sont cohérents avec le vasospasme de l'artère coronarienne ou l'ischémie myocardique Trudhesa ne doit pas être administré [voir Contre-indications ].
Pour les patients présentant des facteurs de risque prédictifs de la maladie coronarienne (par exemple, l'hypertension Hypercholestérolémie fumeur diabète antécédents familiaux de la maladie coronarienne ou les hommes qui ont plus de 40 ans) qui sont déterminés qui ont une évaluation de cardiovasculaire satisfaisante. Trudhesa a lieu dans le cadre d'un établissement de santé équipé à moins que le patient ait déjà reçu du mésylate de dihydroergotamine. Pendant l'intervalle, immédiatement après la première utilisation de Trudhesa, un électrocardiogramme est recommandé chez les patients présentant des facteurs de risque car une ischémie peut se produire en l'absence de symptômes cliniques.
Réactions et décès indésirables cérébrovasculaires
Il existe le potentiel d'effets indésirables indésirables des effets indésirables cérébrovasculaires avec le traitement à Trudhesa. AVC d'hémorragie sous-arachnoïde de l'hémorragie cérébrale et d'autres événements cérébrovasculaires ont été signalés chez les patients traités par du mésylate de dihydroergotamine; Et certains ont entraîné des décès. Dans un certain nombre de cas, il semble possible que les événements cérébrovasculaires soient primaires, le mésylate de dihydroergotamine ayant été administré dans la croyance incorrecte que les symptômes ressentis étaient une conséquence de la migraine alors qu'ils ne l'ont pas été. Il convient de noter que les patients atteints de migraine peuvent courir un risque accru de certains événements cérébrovasculaires (par exemple, une attaque ischémique transitoire de l'hémorragie AVC). Arrêtez Trudhesa si un événement cérébrovasculaire est suspecté.
Autres réactions indésirables liées au vasospasme
Trudhesa comme d'autres alcaloïdes d'ergot peut provoquer des réactions vasospastiques autres que le vasospasme coronarien. Une ischémie vasculaire périphérique myocardique et colique a été signalée avec du mésylate de dihydroergotamine.
Les phénomènes vasospastiques associés au mésylate de dihydroergotamine peuvent également provoquer des douleurs musculaires engourdisseurs la pâleur et la cyanose des chiffres. Chez les patients atteints de circulation compromis, un vasospasme persistant peut entraîner une gangrène ou une mort. Trudhesa doit être interrompu immédiatement si les signes ou symptômes de vasoconstriction se développent.
Les patients qui éprouvent d'autres symptômes ou signes suggérant une diminution du flux artériel tel que le syndrome de l'intestin ischémique ou le syndrome de Raynaud après l'utilisation d'un agoniste 5-HT, y compris Trudhesa, doivent être évalués par un fournisseur de soins de santé.
Augmentation de la pression artérielle
Une élévation significative de la pression artérielle a été signalée à de rares occasions chez les patients atteints de mésylate de dihydroergotamine et sans antécédents d'hypertension avec du mésylate de dihydroergotamine. Trudhesa est contre-indiqué chez les patients souffrant d'hypertension non contrôlée [voir Contre-indications ].
Une augmentation de 18% de la pression moyenne de l'artère pulmonaire a été observée après l'administration avec un autre 5 ht 1 Agoniste dans une étude évaluant les sujets subissant un cathétérisme cardiaque.
Mélange de surutilisation des médicaments
La surutilisation des médicaments de migraine aiguë (par exemple les opioïdes ergotamines triptans ou une combinaison de ces médicaments pendant 10 jours ou plus par mois) peut entraîner une exacerbation des maux de tête (c'est-à-dire des maux de tête de surutilisation des médicaments). Les maux de tête de surutilisation des médicaments peuvent se présenter sous forme de maux de tête quotidiens de type migraine ou comme une augmentation marquée de la fréquence des attaques de migraine. La détoxification des patients, y compris le retrait des médicaments surutilisés et le traitement des symptômes de sevrage (qui comprend souvent une aggravation transitoire des maux de tête) peut être nécessaire.
Travail prématuré
Sur la base du mécanisme d'action de la dihydroergotamine et des résultats de la littérature publiée, Trudhesa peut provoquer un travail prématuré. Évitez l'utilisation de Trudhesa pendant la grossesse [voir Utiliser dans des populations spécifiques ]
Complications fibrotiques
Le potentiel de complications fibrotiques existe avec un traitement Trudhesa. Il y a eu des rapports de fibrose pleurale et rétropéritonéale chez les patients après une utilisation quotidienne prolongée de mésylate de dihydroergotamine. L'utilisation quotidienne rarement prolongée d'autres médicaments alcaloïdes Ergot a été associée à une fibrose valvulaire cardiaque. Des cas rares ont également été signalés en association avec l'utilisation du mésylate de dihydroergotamine; Cependant, dans ces cas, les patients ont également reçu des médicaments connus pour être associés à une fibrose valvulaire cardiaque.
L'administration de Trudhesa ne doit pas dépasser les directives de dosage et ne doit pas être utilisée pour l'administration quotidienne chronique [voir Posologie et administration ].
Irritation locale
Des symptômes irritatifs locaux ont été signalés chez 52% des patients traités avec au moins une dose de Trudhesa dans un essai ouvert qui a permis une utilisation répétée de Trudhesa sur 6 à 12 mois. Les symptômes irritatifs locaux locaux les plus courants (au moins 1% des patients) étaient la nasopharyngite (21%) en rhinite (19%) inconfort (7%) goûter à l'inconfort anormal / dysgeusie (6%) (5%) malfaisant (4%) Test olfactif annulant [défini basé sur un score à une odeur de pure-odex Test d'identification (UPSIT)] (4%) Epistaxis (3%) Pharyngite (3%) Trouble muqueux nasal (2%) Changement de l'inconfort de l'oreille (1%) (1%) et de la rhinorrhée (1%). Si un événement d'irritation local sévère se produit pour aucune autre raison attribuable, Trudhesa devrait être temporairement suspendu jusqu'à ce que l'événement se résout. Si l'événement ne se résout pas ou si elle se reproduit avec Re-Challenge, Trudhesa devrait être interrompu en permanence. L'administration de Trudhesa ne doit pas dépasser les directives de dosage et ne doit pas être utilisée pour l'administration quotidienne chronique [voir Posologie et administration ].
Le tissu nasal chez les animaux traités par le mésylate de dihydroergotamine quotidiennement a montré une légère irritation muqueuse caractérisée par des cellules muqueuses et une hyperplasie des cellules transitoires et une métaplasie squameuse des cellules. Les changements dans la muqueuse nasale de rat à 64 semaines étaient moins graves qu'à 13 semaines. Les effets locaux sur les tissus respiratoires après un dosage intranasal chronique chez les animaux n'ont pas été évalués.
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Guide des médicaments et Instructions pour une utilisation ).
À quoi servent les baies de genévrier pour
Réactions graves et / ou potentiellement mortelles avec la co-administration des inhibiteurs du CYP3A4
Informer les patients que l'ischémie périphérique grave et / ou potentiellement mortelle (ischémie cérébrale et / ou ischémie des extrémités) a été associée à la co-administration de mésylate de dihydroergotamine et de forts inhibiteurs du CYP3A4 tels que les antibiotiques macrolides et les inhibiteurs de la prot3 [ Contre-indications AVERTISSEMENTS AND PRECAUTIONS et Interactions médicamenteuses ].
Ischémie myocardique et / ou infarctus d'autres événements cardiaques événements et décès cérébrovasculaires
Informez les patients du risque d'événements cérébrasculaires cardiaques graves et autres événements liés au vasospasme. Conseiller aux patients de notifier leur fournisseur de soins de santé s'ils développent des facteurs de risque ou des symptômes tout en prenant Trudhesa. Informer les patients que la nicotine peut provoquer une vasoconstriction prédisposant à une plus grande réponse ischémique [voir AVERTISSEMENTS AND PRECAUTIONS ].
Mélange de surutilisation des médicaments
Informer les patients que l'utilisation de médicaments pour traiter les attaques de migraine pendant 10 jours ou plus par mois peut entraîner une exacerbation des maux de tête et encourager les patients à enregistrer la fréquence des maux de tête et la consommation de médicaments (par exemple en organisant un journal de maux de tête) [voir AVERTISSEMENTS AND PRECAUTIONS ].
Irritation locale
Conseiller aux patients de notifier leur fournisseur de soins de santé s'ils ont une irritation locale gênante [voir AVERTISSEMENTS AND PRECAUTIONS ].
Interactions médicamenteuses
Conseiller aux patients d'informer leurs prestataires de soins de santé s'ils prennent ou prévoient de prendre des médicaments sur ordonnance ou en vente libre car il existe un potentiel d'interactions [voir Interactions médicamenteuses ].
Grossesse
Conseiller les patients du risque d'accouchement prématuré. Conseiller aux femmes d'informer leur fournisseur de soins de santé si elles sont enceintes ou ont l'intention de devenir enceintes [voir AVERTISSEMENTS AND PRECAUTIONS Utiliser dans des populations spécifiques ]
Lactation
Conseiller aux patients de ne pas allaiter pendant le traitement avec Trudhesa [voir Utiliser dans des populations spécifiques ].
Instructions d'administration importantes
Conseillez les patients que Trudhesa doit être assemblé avant l'utilisation et qu'avant l'administration, le dispositif doit être amorcé (c'est-à-dire pompé 4 fois). Demandez aux patients d'utiliser ou de jeter Trudhesa dans les 8 heures une fois le flacon ouvert ou que le produit a été assemblé.
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
Cancérogenèse
L'évaluation du potentiel cancérigène du mésylate de dihydroergotamine chez la souris et le rat n'a pas été évaluée.
Mutagenèse
Le mésylate de dihydroergotamine était négatif dans un in vitro Dosage de mutagénicité (AMES) et positif in vitro Aberration chromosomique (V79 Chinese Hamster Cell Hamster Cell with Metabolic Activation and Human Péripheral Blood Lymphocyte). La dihydroergotamine était négative dans en vain Dosages de micronucléus chez la souris et le hamster.
Altération de la fertilité
Il n'y avait aucune preuve d'altération de la fertilité chez le rat étant donné des doses intranasales de mésylate de dihydroergotamine jusqu'à 1,6 mg / jour qui était associée à des expositions au plasma (ASC) environ 3 fois chez l'homme à la dose humaine maximale recommandée de 2,9 mg / jour.
Utiliser dans des populations spécifiques
Grossesse
Résumé des risques
Les données disponibles de la littérature publiée indiquent un risque accru de livraison prématurée avec une utilisation de Trudhesa pendant la grossesse. Évitez l'utilisation de Trudhesa pendant la grossesse [voir AVERTISSEMENTS AND PRECAUTIONS ]. Données collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
Dans les études animales, les effets néfastes sur le développement embryofétal ont été observés après l'administration de mésylate de dihydroergotamine pendant la grossesse (diminution du poids fœtal et / ou de l'ossification squelettique) chez les rats et les lapins ou pendant la grossesse et l'alctation chez les rats (diminution du poids corporel et altération de la fonction reproductrice et non associée à la maternité). Données ).
Le taux estimé des principaux malformations congénitales (NULL,2% à 2,9%) et une fausse couche (17%) parmi les accouchements aux femmes atteintes de migraine sont similaires aux taux signalés chez les femmes sans migraine. Toutes les grossesses présentent un risque de fond de perte de maltraitance natale ou d'autres résultats indésirables. Dans la population générale américaine, le risque de fond estimé de malformations congénitales et de fausses couches dans les grossesses cliniquement reconnues est respectivement de 2% à 4% et 15% à 20%.
Données
Données sur les animaux
L'administration intranasale de mésylate de dihydroergotamine à des rats enceintes tout au long de la période d'organogenèse a entraîné une diminution du poids corporel fœtal et / ou de l'ossification squelettique à des doses de 0,16 mg / jour (associées à des expositions plasmatiques [AUC] inférieures à celles chez l'homme à la dose humaine recommandée maximale [MRHD] de 2,9 mg) ou plus. Un niveau sans effet pour la toxicité embryofétale n'a pas été identifié chez le rat. L'administration intranasale de mésylate de dihydroergotamine à des lapins enceintes tout au long de l'organogenèse a entraîné une diminution de l'ossification squelettique à 3,6 mg / jour. À la dose de non-effet (NULL,2 mg / jour) pour les effets néfastes sur le développement embryofétal dans les expositions au plasma des lapins (AUC) étaient inférieures à celles chez l'homme au MRHD.
L'administration intranasale de mésylate de dihydroergotamine à des rats femelles tout au long de la grossesse et la lactation a entraîné une diminution du poids corporel et une fonction de reproduction altérée (diminution des indices d'accouplement) a été observé dans la progéniture à des doses de 0,16 Mg / jour ou plus. Une dose sans effet pour les effets de développement défavorable chez le rat n'a pas été établie.
Des effets sur le développement se sont produits à des doses inférieures à celles qui ont produit des preuves d'une toxicité maternelle significative dans ces études.
Le retard de croissance intra-utérine induit par la dihydroergotamine a été attribué à une baisse sanguine utéroplacentaire réduite résultant d'une vasoconstriction prolongée des vaisseaux utérins et / ou d'un ton myométrial accru.
Lactation
Résumé des risques
Il n'y a pas de données sur la présence de dihydroergotamine dans le lait maternel; Cependant, l'ergotamine, un médicament connexe est présent dans le lait maternel. Il y a des rapports de diarrhée qui vomissent un impulsion faible et de la pression artérielle instable chez les nourrissons allaités exposés à l'ergotamine. Trudhesa peut réduire l'apport de lait car il peut diminuer les niveaux de prolactine. En raison du potentiel de réduction de l'approvisionnement en lait et d'événements indésirables graves chez le nourrisson allaité, y compris la diarrhée vomissant un impulsion faible et la pression artérielle instable conseille aux patients de ne pas allaiter pendant le traitement par Trudhesa et pendant 3 jours après la dernière dose. L'alimentation du lait maternel pendant cette période doit être pompée et jetée.
Usage pédiatrique
La sécurité et l'efficacité des patients pédiatriques n'ont pas été établies.
Utilisation gériatrique
Les études cliniques sur les produits de mésylate de dihydroergotamine à Trudhesa et à dihydroergotamine n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s'ils réagissent différemment des sujets plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente qui commence généralement à l'extrémité inférieure de la plage de dosage reflétant la plus grande fréquence de diminution de la fonction rénale ou cardiaque hépatique et de maladie concomitante ou autre médicament.
Surdosage Information for Trudhesa
Symptômes
Des doses excessives de dihydroergotamine peuvent entraîner des signes périphériques et des symptômes de l'ergotisme. En général, les symptômes d'une surdose aiguë de Trudhesa sont similaires à ceux d'une surdose d'ergotamine bien qu'il puisse y avoir moins de nausées et de vomissements prononcés avec Trudhesa. Les symptômes d'une surdose d'ergotamine comprennent les éléments suivants: engourdissement de la douleur et de la cyanose des extrémités associées à des impulsions périphériques diminuées ou absentes; dépression respiratoire; une augmentation et / ou une diminution de la pression artérielle généralement dans cet ordre; Convulsions de délire de confusion et coma; et / ou un certain degré de nausées vomissements et douleurs abdominales.
Chez les animaux de laboratoire, la dihydroergotamine était mortelle lorsqu'il était administré à des doses intraveineuses de 44 mg / kg chez la souris 130 mg / kg chez le rat et 37 mg / kg chez le lapin.
Traitement
Traitement includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators et nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Contre-indications for Trudhesa
Trudhesa est contre-indiqué chez les patients:
sac à dos en Europe
- avec une utilisation concomitante de forts inhibiteurs du CYP3A4 tels que les inhibiteurs de protéase (par exemple les antibiotiques de macrolide de ritonavir (par ex. érythromycine ou clarithromycine) et antifongiques (kétoconazole ou itraconazole) [voir AVERTISSEMENTS AND PRECAUTIONS et Interactions médicamenteuses ]
- avec des maladies cardiaques ischémiques (antécédents d'angine de pectoralis d'infarctus du myocarde ou d'ischémie silencieuse documentée) ou des patients qui présentent des symptômes cliniques ou des résultats cohérents avec le vasospasme de l'artère coronarienne, y compris la variante de poitrine de Prinzmetal [ AVERTISSEMENTS AND PRECAUTIONS ]
- avec une hypertension incontrôlée [voir AVERTISSEMENTS AND PRECAUTIONS ]
- avec une maladie artérielle périphérique
- avec septicémie
- Après une chirurgie vasculaire
- avec une déficience hépatique sévère
- avec une sévère insuffisance rénale
- avec une hypersensibilité connue aux alcaloïdes ergot
- avec une utilisation récente (c'est-à-dire dans les 24 heures) des autres 5-HT 1 les agonistes (par exemple le sumatriptan) ou les médicaments contenant de l'ergotamine ou de type ergot [voir Interactions médicamenteuses ]
- avec une utilisation concomitante de vasoconstricteurs périphériques et centraux car la combinaison peut entraîner une élévation additive ou synergique de la pression artérielle [voir AVERTISSEMENTS AND PRECAUTIONS ]
Pharmacologie clinique for Trudhesa
Mécanisme d'action
La dihydroergotamine se lie à une affinité élevée au 5-HT 1da et 5-HT 1 dB récepteurs. L'activité thérapeutique de la dihydroergotamine dans la migraine est généralement attribuée aux effets agonistes à 5-HT 1D récepteurs.
Pharmacodynamique
Une élévation significative de la pression artérielle a été signalée chez les patients atteints et sans antécédents d'hypertension [voir AVERTISSEMENTS AND PRECAUTIONS ].
La dihydroergotamine possède des propriétés oxytociques [voir AVERTISSEMENTS AND PRECAUTIONS ].
Pharmacocinétique
Absorption
Le temps moyen entre le dosage à la concentration plasmatique maximale après l'administration de Trudhesa était d'environ 0,5 heure.
Distribution
Le mésylate de dihydroergotamine est à 93% lié aux protéines de plasma. Le volume de distribution apparent à l'état d'équilibre est d'environ 800 litres.
Élimination
Métabolisme
Quatre métabolites de mésylate de dihydroergotamine ont été identifiés dans le plasma humain après l'administration orale. Le principal métabolite 8'-ß-hydroxy dihydroergotamine présente une affinité équivalente à son parent pour les récepteurs adrénergiques et 5-HT et démontre une puissance équivalente dans plusieurs modèles d'activité venoconstrictor en vain et in vitro . Les autres métabolites, c'est-à-dire l'amide dihydrolysergique à l'acide dihydrolysergique et un métabolite formé par l'ouverture oxydative de l'anneau proline, sont d'une importance mineure. Après l'administration nasale, les métabolites totaux ne représentent que 20% à 30% de l'ASC plasmatique. La clairance systémique du mésylate de dihydroergotamine après l'administration intraveineuse et intramusculaire est de 1,5 L / min. La caractérisation pharmacocinétique quantitative des quatre métabolites n'a pas été réalisée.
Excrétion
La principale voie excrétoire de la dihydroergotamine est via la bile dans les excréments. La dégagement total du corps est de 1,5 L / min, ce qui reflète principalement la clairance hépatique. Seulement 6% à 7% de la dihydroergotamine inchangée est excrétée dans l'urine après injection intramusculaire. La clairance rénale (NULL,1 L / min) n'est pas affectée par la route de l'administration de dihydroergotamine.
La demi-vie apparente moyenne de l'administration nasale de Trudhesa chez des sujets sains est d'environ 12 heures.
Populations spécifiques
Aucune étude n'a été menée sur l'effet de l'ethnicité ou de la grossesse de la race ou de la grossesse sur la pharmacocinétique de dihydroergotamine [voir Contre-indications Utiliser dans des populations spécifiques ].
Études d'interaction médicamenteuse
Inhibiteurs du CYP3A4
Rare reports of ergotism have been obtained from patients treated with dihydroergotamine and macrolide antibiotics (e.g. clarithromycin erythromycin) and from patients treated with dihydroergotamine and protease inhibitors (e.g. ritonavir) presumably due to inhibition of CYP3A metabolism of ergotamine [see Contre-indications ].
Autres drogues
La pharmacocinétique de la dihydroergotamine ne semble pas être significativement affectée par l'utilisation concomitante d'un vasoconstricteur local.
Plusieurs doses orales de l'antagoniste β-adrénergateur propranolol utilisé pour la prophylaxie de la migraine n'ont eu aucune influence significative sur le CMAX Tmax ou l'AUC de doses de dihydroergotamine jusqu'à 4 mg. Cependant, le propranolol peut potentialiser l'action vasoconstrictive de l'ergotamine [voir Interactions médicamenteuses ].
L'effet des contraceptifs oraux sur la pharmacocinétique de Trudhesa n'a pas été étudié.
Études cliniques
L'efficacité de Trudhesa est basée sur la biodisponibilité relative du spray nasal Trudhesa par rapport au spray nasal de mésylate de dihydroergotamine chez des sujets sains.
Les études cliniques décrites ci-dessous ont été menées en utilisant un spray nasal de mésylate de dihydroergotamine.
L'efficacité du spray nasal de mésylate de dihydroergotamine pour le traitement aigu des maux de tête de migraine a été évaluée dans quatre études contrôlées par placebo en double aveugle randomisées aux États-Unis. La population de patients pour les essais était principalement des femmes (87%) et du Caucasien (95%) avec un âge moyen de 39 ans (plage de 18 à 65 ans). Les patients ont traité un seul mal de tête de migraine modéré à sévère avec une seule dose de médicament à l'étude et évalué la gravité de la douleur au cours des 24 heures suivant le traitement. La réponse des maux de tête a été déterminée 0,5 1 2 3 et 4 heures après le dosage et a été définie comme une réduction de la gravité des maux de tête à une douleur légère ou non. Dans les études 1 et 2, une échelle d'intensité de douleur à quatre points a été utilisée; Dans les études 3 et 4, une échelle à cinq points a été utilisée pour enregistrer la réponse à la douleur. Bien que les médicaments de sauvetage aient été autorisés dans les quatre études, les patients ont été invités à ne pas les utiliser pendant la période d'observation de quatre heures. Dans les études 3 et 4, une dose totale de 2 mg a été comparée au placebo. Dans les études 1 et 2, des doses de 2 et 3 mg ont été évaluées et n'ont montré aucun avantage de la dose plus élevée pour un seul traitement. In all studies patients received a regimen consisting of 0.5 mg in each nostril repeated in 15 minutes (and again in another 15 minutes for the 3 mg dose in studies 1 and 2).
Le pourcentage de patients atteignant une réponse des maux de tête 4 heures après le traitement était significativement plus élevé chez les patients recevant 2 mg de doses de spray nasal de mésylate de dihydroergotamine par rapport à celles recevant un placebo dans 3 des 4 études (voir tableau 2 et tableau 3 et figure 1 et figure 2).
Tableau 2 Études 1 et 2: pourcentage de patients avec réponse aux maux de tête a 2 et 4 heures après un seul traitement des médicaments d'étude (pulvérisation nasale mésylate de dihydroergotamine ou placebo)
| N | 2 heures | 4 heures | ||
| Étude 1 | Dihydroergotamine mésylate nasale | 105 | 61% ** | 70% ** |
| Placebo | 98 | 23% | 28% | |
| Différence par rapport au placebo | 37% | 42% | ||
| Étude 2 | Dihydroergotamine mésylate nasale | 103 | 47% | 56% * |
| Placebo | 102 | 33% | 35% | |
| Différence par rapport au placebo | 14% | 21% | ||
| a La réponse des maux de tête a été définie comme une réduction de la gravité des maux de tête à une douleur légère ou non. La réponse des maux de tête était basée sur l'intensité de la douleur comme interprété par le patient en utilisant une échelle d'intensité de douleur à quatre points. * Vale <0.01 ** Valeur P <0.001 |
Tableau 3 Études 3 et 4: pourcentage de patients avec réponse aux maux de tête a 2 et 4 heures après un seul traitement des médicaments d'étude (pulvérisation nasale mésylate de dihydroergotamine ou placebo)
| N | 2 heures | 4 heures | ||
| Étude 3 | Dihydroergotamine mésylate nasale | 50 | 32 | 48% * |
| Placebo | 50 | 20% | 22% | |
| Différence par rapport au placebo | 12% | 26% | ||
| Étude 4 | Dihydroergotamine mésylate nasale | 47 | 30% | 47% |
| Placebo | 50 | 20% | 30% | |
| Différence par rapport au placebo | 10% | 17% | ||
| a La réponse des maux de tête a été définie comme une réduction de la gravité des maux de tête à une douleur légère ou non. La réponse des maux de tête a été évaluée sur une échelle de cinq points qui comprenait une réponse à la douleur. * Vale <0.01 |
Les tracés de Kaplan-Meier ci-dessous (figure 1 et figure 2) fournissent une estimation de la probabilité qu'un patient ait répondu à une dose de 2 mg unique de dihydroergotamine mésylate nasale en fonction du temps depuis le début du traitement.
Figure 1 La probabilité estimée d'un patient répondant pendant les quatre heures suivant une seule dose de 2 mg de pulvérisation nasale de mésylate de dihydroergotamine en fonction du temps écoulé depuis le début du traitement *
| * La figure montre la probabilité au fil du temps d'obtenir une réponse après un traitement avec un pulvérisation nasale de mésylate de dihydroergotamine. La réponse des maux de tête était basée sur l'intensité de la douleur comme interprété par le patient en utilisant une échelle d'intensité de la douleur à quatre points. Les patients qui n'obtiennent pas de réponse dans les 4 heures ont été censurés à 4 heures. |
Figure 2 Probabilité estimée d'un patient répondant au spray nasal mésylat de dihydroergotamine pendant les quatre heures suivant le dosage *
| * La figure montre la probabilité au fil du temps d'obtenir une réponse après un traitement avec un pulvérisation nasale de mésylate de dihydroergotamine. La réponse des maux de tête a été évaluée sur une échelle de cinq points qui comprenait une réponse à la douleur. Les patients qui n'obtiennent pas de réponse dans les 4 heures ont été censurés à 4 heures. |
Pour les patients atteints de phonophobie et de phonophobie associées à la migraine, il y avait une incidence plus faible de ces symptômes à 2 et 4 heures après l'administration de pulvérisation nasale de mésylate de dihydroergotamine par rapport au placebo.
Les patients n'ont pas été autorisés à utiliser des traitements supplémentaires pendant 8 heures avant le dosage des médicaments de l'étude et pendant la période d'observation de 4 heures suivant le traitement de l'étude. Après la période d'observation de 4 heures, les patients ont été autorisés à utiliser des traitements supplémentaires. Pour toutes les études, la probabilité estimée de patients utilisant des traitements supplémentaires pour leurs migraines au cours des 24 heures suivant la dose de 2 mg de traitement à 2 mg est résumé sur la figure 3 ci-dessous.
Figure 3 Probabilité estimée d'un patient utilisant des traitements supplémentaires pour la migraine au cours des 24 heures suivant soit la dihydroergotamine mésylate nasale pulvérisation 2 mg (ou placebo) *
| * Graphique de Kaplan-Meier basé sur les données obtenues à partir de toutes les études avec des patients n'utilisant pas de traitements supplémentaires censurés à 24 heures. Tous les patients ont reçu un traitement unique des médicaments d'étude pour leur attaque de migraine. L'intrigue comprend également des patients qui n'ont eu aucune réponse à la dose initiale. |
Ni l'âge ni le sexe ne semblent affecter la réponse du patient au spray nasal de mésylate de dihydroergotamine. La répartition raciale des patients était insuffisante pour déterminer l'effet de la race sur l'efficacité du spray nasal de mésylate de dihydroergotamine.
Informations sur les patients pour Trudhesa
Trusta ™
(Trae - Deh - un)
(mésylate de dihydroergotamine)
Quelles sont les informations les plus importantes que je devrais connaître sur Trudhesa?
Trudhesa peut provoquer des effets secondaires graves, notamment:
- Problèmes graves avec la circulation sanguine aux jambes et aux pieds (ischémie périphérique). Trudhesa peut provoquer une ischémie périphérique lorsque vous le prenez avec certains médicaments appelés inhibiteurs du CYP3A4. L'ischémie périphérique peut entraîner un accident vasculaire cérébral et une mort. Arrêtez de prendre Trudhesa et obtenez une aide médicale d'urgence immédiatement si vous présentez l'un des symptômes suivants:
- Crampes et douleur dans vos jambes ou vos hanches
- sentiment de lourdeur ou de tension dans les muscles de vos jambes
- Douleur brûlante ou douloureuse dans vos pieds ou orteils tout en se reposant
- engourdissement picotement ou faiblesse dans vos jambes
- sensation à froid ou changements de couleur dans 1 ou les deux jambes ou pieds
- discours
- faiblesse
Ne prenez pas de médicaments appelés forts inhibiteurs du CYP3A4 tels que:
-
- Ritonavir
- érythromycine
- kétoconazole
- Netfinavir
- clarithromycine
- itraconazole
Ce ne sont pas tous les médicaments qui pourraient affecter le fonctionnement de Trudhesa. Votre professionnel de la santé peut vous dire s'il est sûr de prendre Trudhesa avec d'autres médicaments.
Qu'est-ce que Trudhesa?
Trudhesa est un médicament sur ordonnance utilisé pour le traitement aigu de la migraine avec ou sans aura chez l'adulte.
- Trudhesa n'est pas utilisé pour empêcher la migraine.
- Trudhesa n'est pas utilisé pour traiter d'autres types de maux de tête tels que l'hémiplégique (qui vous rend incapable de vous déplacer d'un côté de votre corps) ou de migraines basilaires (rare de migraine avec l'aura).
On ne sait pas si Trudhesa est sûr et efficace chez les enfants.
Ne prenez pas Trudhesa si vous:
- prennent des médicaments connus sous le nom de forts inhibiteurs du CYP3A4.
- avoir des problèmes cardiaques ou une histoire de problèmes cardiaques.
- ont une pression artérielle élevée incontrôlée.
- Ayez un rétrécissement des vaisseaux sanguins dans vos jambes, les armes ou les reins (maladie vasculaire périphérique).
- avoir une septicémie.
- ont subi une chirurgie vasculaire.
- avoir de graves problèmes hépatiques.
- avoir de graves problèmes rénaux.
- sont allergiques aux alcaloïdes de l'ergot mésylate de dihydroergotamine ou à tout ingrédients de Trudhesa. Voir la fin de ce guide de médicaments pour une liste complète des ingrédients.
- ont pris l'un des médicaments suivants au cours des dernières 24 heures:
- sumatriptan
- almotriptan
- étruptan
- frovatriptate
- naratriptan
- Rizatriptan
- médicaments de type ergotamine ou ergotamine
- ont pris des médicaments qui restreignent vos vaisseaux sanguins ou augmentent votre tension artérielle.
Demandez à votre fournisseur de soins de santé si vous ne savez pas si vous prenez l'un de ces médicaments. Votre professionnel de la santé peut vous dire s'il est sûr de prendre Trudhesa avec d'autres médicaments.
Avant de prendre Trudhesa, informez votre fournisseur de soins de santé de toutes vos conditions médicales, y compris si vous:
- ont une pression artérielle élevée.
- avoir des problèmes de foie.
- avoir des problèmes rénaux.
- fumée.
- sont enceintes ou prévoient de devenir enceintes. Trudhesa peut provoquer un travail prématuré. Trudhesa doit être évité pendant la grossesse. Parlez immédiatement à votre fournisseur de soins de santé si vous êtes enceinte ou si vous souhaitez devenir enceinte.
- allaitent ou prévoient d'allaiter. Trudhesa peut réduire l'approvisionnement en lait maternel et passer dans votre lait maternel. Trudhesa peut être nocif pour votre bébé. N'allaitez pas votre bébé en prenant Trudhesa et pendant 3 jours après avoir utilisé Trudhesa. Parlez avec votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé si vous prenez Trudhesa.
Parlez à votre fournisseur de soins de santé de tous les médicaments que vous prenez y compris les médicaments sur ordonnance et en vente libre des vitamines et des suppléments à base de plantes. Votre professionnel de la santé décidera si vous pouvez prendre Trudhesa avec vos autres médicaments.
Parlez surtout de votre fournisseur de soins de santé si vous prenez:
-
- sumatriptan
- fluconazole
- propranolol ou d'autres médicaments qui peuvent abaisser votre fréquence cardiaque
- Médecine de type ergot o jus de pamplemousse o tout médicament qui peut augmenter votre tension artérielle
- saquinavir o zileuton o sérotonine sélective réapprovisionnement inhibiteurs
- néfazodone
- nicotine
Ce ne sont pas tous les médicaments qui pourraient affecter le fonctionnement de Trudhesa. Votre professionnel de la santé peut vous dire s'il est sûr de prendre Trudhesa avec d'autres médicaments.
Comment devrais-je prendre Trudhesa?
- Certaines personnes devraient prendre leur première dose de Trudhesa dans le cabinet de leur médecin ou dans un autre milieu. Demandez à votre médecin si vous devez prendre votre première dose en milieu médical.
- Utilisez Trudhesa exactement comme votre fournisseur de soins de santé vous dit de l'utiliser. Lisez et suivez les instructions dans le Instructions pour une utilisation qui est fourni avec le package Trudhesa avant de l'utiliser.
- Vous devez utiliser Trudhesa dès que les symptômes de vos maux de tête commencent, mais il peut être donné à tout moment pendant une migraine.
- Après avoir assemblé Trudhesa et amorcé l'appareil pulvérisé 1 fois dans chaque narine (une dose complète).
- Si votre mal de tête revient après la première dose complète ou si vous obtenez seulement un soulagement de votre mal de tête, vous pouvez utiliser une deuxième dose 1 heure après la première dose complète. Utilisez un nouveau dispositif de pulvérisation nasal Trudhesa pour la deuxième dose.
- N'utilisez pas plus de 2 doses de Trudhesa dans une période de 24 heures ou 3 doses dans un délai de 7 jours.
- Si vous utilisez trop Trudhesa, appelez votre fournisseur de soins de santé ou allez immédiatement aux urgences de l'hôpital le plus proche.
- Prendre Trudhesa pendant 10 jours ou plus en 1 mois peut aggraver vos maux de tête. Vous devriez écrire lorsque vous avez des maux de tête et lorsque vous prenez Trudhesa afin que vous puissiez parler avec votre professionnel de la santé de la façon dont Trudhesa travaille pour vous.
Quels sont les effets secondaires possibles de Trudhesa?
Trudhesa peut provoquer des effets secondaires graves, notamment:
Voir «Quelles sont les informations les plus importantes que je devrais connaître sur Trudhesa?
- Crise cardiaque et autres problèmes cardiaques. Les problèmes cardiaques peuvent entraîner la mort. Arrêtez de prendre Trudhesa et obtenez une aide médicale d'urgence immédiatement si vous présentez l'un des symptômes suivants d'un crise cardiaque :
- inconfort au centre de votre poitrine qui dure plus de quelques minutes ou qui disparaît et revient
- Pression sévère de la douleur ou de la lourdeur dans le cou ou la mâchoire de la gorge de votre poitrine
- douleur ou inconfort dans vos bras arrière mâchoire ou estomac
- essoufflement avec ou sans inconfort thoracique
- Rompre dans une sueur froide
- nausée or vomissement
- se sentir étourdi
Trudhesa n'est pas pour les personnes présentant des facteurs de risque de maladie cardiaque à moins qu'un examen cardiaque ne soit effectué et ne montre aucun problème. Vous avez un risque plus élevé pour les maladies cardiaques si vous:
-
- avoir une pression artérielle élevée
- ont des taux élevés de cholestérol
- fumée
- sont en surpoids
- avoir le diabète
- avoir des antécédents familiaux de maladie cardiaque
- Accident vasculaire cérébral. Arrêtez de prendre Trudhesa et obtenez une aide médicale d'urgence immédiatement si vous présentez l'un des symptômes suivants d'un accident vasculaire cérébral:
- visage tombant
- faiblesse ou engourdissement inhabituel
- discours
- Changements de couleur ou de sensation dans vos doigts et orteils (syndrome de Raynaud).
- Problèmes d'estomac et d'intestin (événements ischémiques gastro-intestinaux et coliques). Les symptômes des événements ischémiques gastro-intestinaux et coliques comprennent:
- Douleurs soudaines ou sévères
- constipation ou diarrhée
- Douleurs d'estomac après les repas
- Diarrhée sanglante
- perte de poids
- fièvre
- nausée or vomissement
- Augmenter la pression artérielle.
- Médecine sur utilisation des maux de tête. Certaines personnes qui utilisent trop Trudhesa peuvent aggraver leurs maux de tête (médicaments sur utilisation des maux de tête). Si vos maux de tête s'aggravent, votre fournisseur de soins de santé peut décider d'arrêter votre traitement avec Trudhesa.
- Travail prématuré.
- Changements tissulaires (complications fibrotiques). La nflammation et les tissus de type fibre qui ne sont pas normaux (fibrose) peuvent se produire autour des poumons et de l'estomac.
- Brûler des sentiments dans la bouche et la gorge de votre nez et un goût anormal.
- nez qui coule
- Réactions du site d'application
- envie de dormir
- nausée
- vertiges
- mal de gorge
- goût anormal
- vomissement
- diarrhée
Ce ne sont pas tous les effets secondaires possibles Trudhesa.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Comment dois-je stocker Trudhesa?
Éloignez Trudhesa de la chaleur et de la lumière.
- Conservez Trudhesa à température ambiante entre 68 ° F à 77 ° F (20 ° C à 25 ° C).
- Ne réfrigérez ni ne congelez.
- Après l'ouverture d'un flacon de Trudhesa, il doit être jeté après 8 heures.
Gardez Trudhesa et tous les médicaments hors de portée des enfants.
Ne jetez pas Trudhesa dans le feu ou les incinérateurs car la cartouche à l'intérieur de l'appareil peut exploser.
Informations générales sur l'utilisation sûre et efficace de Trudhesa.
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide de médicaments. N'utilisez pas Trudhesa pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas Trudhesa à d'autres personnes même s'ils présentent les mêmes symptômes que vous. Cela peut leur faire du mal. Vous pouvez demander à votre pharmacien ou fournisseur de soins de santé pour des informations sur Trudhesa qui sont écrits pour les professionnels de la santé.
Ingrédient actif: Mésylate de dihydroergotamine
Ingrédients inactifs: Dextrose de dioxyde de carbone de caféine et d'eau. La cartouche de dispositif de pulvérisation nasal contient l'hydrofluoroalkane-134a (HFA) propulseur. Le bouchon du flacon n'est pas fait avec du latex en caoutchouc naturel. Trudhesa est une marque de fabrique d'Impel Neuropharma Inc.
Ce guide de médicaments a été approuvé par la Food and Drug Administration des États-Unis.
Instructions pour une utilisation
Trusta ™
(ROE-SA)
(mésylate de dihydroergotamine)
spray nasal
Pour une utilisation nasale uniquement
Introduction
Lisez ces instructions à utiliser avant de commencer à utiliser Trudhesa et chaque fois que vous obtenez une recharge de prescription. Il peut y avoir de nouvelles informations.
Ces informations ne prennent pas la place de parler avec votre fournisseur de soins de santé de votre état de santé ou de votre traitement. Vous et votre fournisseur de soins de santé devriez parler de Trudhesa lorsque vous commencez à le prendre et à des contrôles réguliers.
Il est important de suivre ces instructions avec précision afin de recevoir la bonne dose.Contactez votre fournisseur de soins de santé si vous avez des questions sur la façon d'utiliser ce produit.
 |
Pièces de dispositif de pulvérisation nasal
 |
Pièces de flacon de verre
 |
Informations importantes que vous devez savoir avant de doser avec Trudhesa
- Pour une utilisation nasale uniquement.
- Amennez toujours le dispositif de pulvérisation nasal avant de doser en pompant les poignées des doigts et le flacon en verre ensemble exactement 4 fois
- Le but de l'amorçage est d'amener le médicament à la pointe de la buse de pulvérisation. Vous pouvez voir ou non le liquide ou le spray sortir de la buse pendant chaque action d'amorçage.
- Pendant l'amorçage, assurez-vous de viser la buse de pulvérisation loin de votre visage et tout ce que vous ne voulez pas entrer en contact avec le spray de médicament.
- Une dose complète est de 2 sprays; 1 pulvérisation dans chaque narine.
- Ne pas Prenez plus de 2 doses dans un délai de 24 heures. Ne pas Prenez plus de 3 doses dans une période de 7 jours.
- Tenez toujours le dispositif de pulvérisation nasal parfaitement debout lors de l'amorçage et lors du dosage.
- Sniffing tandis que le dosage n'est pas nécessaire.
- Ce produit de dispositif de pulvérisation nasal est unique (pour une dose complète uniquement) et doit être jeté (jeté) après une utilisation. Vous aurez besoin d'un nouveau kit pour chaque dose.
- Gardez le produit dans le cas jusqu'à ce que ce soit prêt à l'emploi.
- Après un flacon de Trudhesa, il doit être jeté après 8 heures.
- Ne pas Ouvrez le flacon de verre et exposez à l'air jusqu'à ce qu'il soit prêt à l'emploi.
- Conservez à température ambiante dans une zone sèche propre.
- Ne pas Utilisez si le produit est endommagé.
- Ne pas Utilisez si le produit est expiré.
- Chaque flacon en verre et dispositif de pulvérisation nasal ne peut être utilisé qu'un temps. Jetez l'ensemble du dispositif de pulvérisation nasal après le dosage sans retirer le flacon de verre.
- Vous pouvez prendre une autre dose complète au moins 1 heure après votre première dose si vos symptômes persistent.
Stockage Trudhesa
- Conservez Trudhesa à température ambiante entre 68 ° F à 77 ° F (20 ° C à 25 ° C).
- Conservez Trudhesa dans l'emballage d'origine dans une zone Cleandry loin de la chaleur et de la lumière ( Figure A ).
- Gardez Trudhesa dans l'emballage d'origine jusqu'à ce que vous soyez prêt à l'emploi.
- Ne pas Réfrigérer ou congeler Trudhesa.
- Gardez Trudhesa et tous les médicaments hors de portée des enfants.
 |
Se préparer à la dose avec Trudhesa
Étape 1: Rassemblez et vérifiez les fournitures
 |
 |
- Vérifiez que vous utilisez le bon médicament pour votre migraine (voir Figure B ).
- Vérifiez que Trudhesa n'est pas expiré (EXP) (voir Figure C ).
- S'il est expiré, jetez et obtenez un nouveau flacon en verre.
- Vérifiez que le flacon en verre et le couvercle en plastique bleu ne semblent pas endommagés.
Étape 2: Retirez le papier couvert en plastique bleu et le bouchon en caoutchouc gris du flacon de verre
 |
 |
 |
- Retirer (remonter) le couvercle en plastique bleu du flacon en verre (voir Figure D ).
- Utilisez le couvercle en plastique bleu pour décoller lentement le papier d'aluminium métallique du bouchon de caoutchouc gris dans un mouvement circulaire (voir Figure E ).

- Tirez le bouchon en caoutchouc gris vers le haut et hors du flacon de verre ( Figure F et Figure G ).
- Jeter (jeter) couvrer le papier d'aluminium et un bouchon en caoutchouc gris dans la poubelle.
Étape 3: Retirez le couvercle en plastique transparent du dispositif de pulvérisation nasal
- Tenez le dispositif nasal SPPRAY debout.
- Tirez sur le couvercle en plastique transparent et retirez-le du dispositif de pulvérisation nasal ( Figure H ).
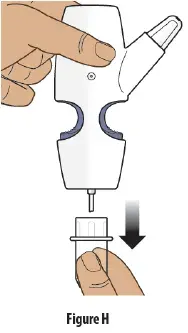
- Jetez la chère couverture en plastique.
Étape 4: Vissez le flacon de verre dans le dispositif de pulvérisation nasal
 |
 |
- Tenez le dispositif de pulvérisation nasal debout.
- Poussez doucement le flacon de verre dans le bas du dispositif nasal Sparay (voir Figure I ) et le visser jusqu'à ce qu'il soit sécurisé comme indiqué dans Figure J .
Étape 5: Prime le dispositif de pulvérisation nasal en pompant quatre fois avec des doigts et du pouce
 |
- Tenez le dispositif de pulvérisation nasal droit .
- Pointez la buse de pulvérisation loin de votre visage.
- Placez votre pouce sur le bas du flacon de verre et placez votre pointeur (index) et les doigts du milieu sur les poignées des doigts (voir Figure K ).
- Pomper le dispositif de pulvérisation nasal exactement 4 fois.
- Pour pomper le dispositif de pulvérisation nasal, appuyez fermement sur les poignées du doigt Dowm et appuyez sur le flacon de verre en même temps. Puis relâchez (voir Figure K )
- Vous pouvez voir un jet de médicament pendant l'amorçage. C'est normal. C'est bien si vous ne voyez pas de médicaments pulvériser sur les premières pompes.
Conseil important: Le but de l'amorçage est d'amener le médicament à la pointe de la buse de pulvérisation. Si vous n'amortissez pas le dispositif de pulvérisation nasal, vous n'obtiendrez pas votre dose de médecine correcte.
Aménager toujours le dispositif de pulvérisation nasal avant l'utilisation en pompant exactement 4 fois.
Pendant l'amorçage, assurez-vous de viser la buse loin de votre visage et tout ce que vous ne voulez pas entrer en contact avec le spray de médicament.
Utilisation de Trudhesa
Étape 6: Positionnez le dispositif de pulvérisation nasal
 |
- Tourner ou reprendre le dispositif nasal Sprey afin que la buse de pulvérisation vous soit affrontée.
- Assurez-vous que votre tête est droite et que le dispositif de pulvérisation nasal est droit.
- Insérez la buse Sparay dans votre première narine jusqu'à confort (voir Figure L ).
Étape 7: Vaporisez la première pulvérisation en 1 narine
- Appuyez fermement sur les poignées des doigts et appuyez sur le flacon de verre en même temps pour livrer le premier spray (voir Figure m ).Then release.
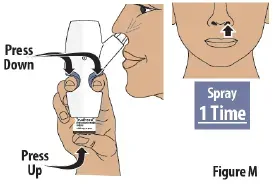
- Ne donnez que 1 pulvérisation dans cette narine.
Étape 8: Vaporisez le deuxième pulvérisation dans d'autres narines
- Déplacez la buse de pulvérisation dans votre autre narine.
- Appuyez fermement sur les poignées des doigts et appuyez sur le flacon de verre en même temps pour livrer le deuxième spray (voir Figure N ).Then release.
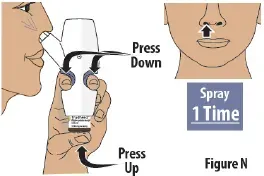
- Ne donnez que 1 pulvérisation dans cette narine.
Conseil important: Une dose complète est de 2 sprays; 1 pulvérisation dans chaque narine.
glucides / levo 25
Ne pas Prenez plus de 2 doses dans un délai de 24 heures. Ne pas Prenez plus de 3 doses dans une période de 7 jours.Please refer to the prescribing information for more information.
Sniffing tandis que ou après le dosage n'est pas nécessaire.
Questions importantes fréquemment posées (FAQ)
Question: Puis-je économiser des médicaments en sautant les 4 pompes dans «Étape 5: Prime le dispositif de pulvérisation nasal»?
Répondre: Aucune saut de 4 pompes pour amorcer le dispositif de pulvérisation nasal ne peut vous empêcher d'obtenir votre dose de médicament correcte.
Qestion: Quand j'ai pompé le dispositif de pulvérisation nasal pour la première fois, rien ne semblait se produire. Pourquoi?
Répondre: Le but de l'amorçage est d'amener le médicament à la pointe de la buse. Même si vous ne voyez ni ne voyez rien sur votre première pompe ou deux, l'action de pompage déplacera le médicament du flacon de verre à l'intérieur du dispositif de pulvérisation nasal et dans la buse.Vous devriez voir un pulvérisation par votre quatrième tentative de pompe.
Question: Puis-je réutiliser le dispositif de pulvérisation nasal avec un nouveau flacon en verre?
Répondre: Le dispositif de pulvérisation nasal nasal est pour une utilisation ponctuelle uniquement et doit être jeté après avoir fermé (1 pulvérisation dans chaque narine). C'est parce que le dispositif peut obstruer. Après avoir dossant le flacon de verre vissé sur le dispositif de pulvérisation nasal et jeter le dispositif de pulvérisation nasal assemblé dans la poubelle. Ne recyclez aucune partie du produit.
Question: Puis-je utiliser le médicament qui reste dans le flacon de verre pour une dose ultérieure?
Répondre: Bien qu'il soit nrmal que certains médicaments restent dans le flacon de verre, il ne peut pas être utilisé pour le dosage ultérieur. Toutes les restes de médecine deviendront inefficaces.
Question: Que se passe-t-il si je paraiss plus d'une fois dans la même narine?
Répondre: Une dose complète et correcte est une pulvérisation dans chaque narine. Ne faites pas de dose dans votre autre narine si vous avez déjà pulvérisé deux fois dans un narine.
Question: Combien de temps puis-je prendre une autre dose si je ne reçois pas de soulagement de ma migraine?
Répondre: Vous pouvez prendre une autre dose au moins 1 heure après la première dose de la première dose si vos symptômes persistent. Ne pas Prenez plus de 2 doses dans un délai de 24 heures. Ne pas Prenez plus de 3 doses dans une période de 7 jours.Please refer to the prescribing information for more information.
Ces instructions d'utilisation ont été approuvées par la Food et la Drug Administration des États-Unis.




