Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Corticostéroïdes, topiqueSpray kenalog
Résumé
Qu'est-ce que Kenalog Spray?
Le spray Kenalog (acétonide de triamcinolone) est un corticostéroïde topique indiqué pour le soulagement des démangeaisons en raison de l'irritation cutanée. Le spray Kenalog est disponible en tant que drogue générique .
Quels sont les effets secondaires du spray kenalog?
Les effets secondaires courants du spray Kenalog comprennent la brûlure des démangeaisons et de la sécheresse. Les effets secondaires graves du spray kenalog comprennent:
- éruption cutanée sévère
- essoufflement
- difficulté à avaler et
- infections cutanées
Dosage pour le spray kenalog
Le spray Kenalog est disponible en deux tailles, 63 et 100 mg peuvent en force de 0,147 mg par gramme. Des instructions pour l'utilisation du pulvérisation peuvent être fournies sur l'étiquette. Des sprays de kenalog peuvent être appliqués sur n'importe quelle zone du corps, bien que des soins soient prises pour voir que les yeux sont couverts et que l'inhalation du spray est évitée lorsqu'elle est pulvérisée autour du visage.
Quelles substances ou suppléments de médicaments interagissent avec le spray kenalog?
Le spray Kenalog peut interagir avec d'autres médicaments. Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Spray kenalog pendant la grossesse ou l'allaitement
Il n'y a pas d'études adéquates et bien contrôlées chez les femmes enceintes sur les effets tératogènes à partir de corticostéroïdes appliqués par voie topique comme le spray Kenalog. Par conséquent, les corticostéroïdes topiques ne doivent être utilisés pendant la grossesse que si le bénéfice potentiel justifie le risque potentiel pour le fœtus. Les corticostéroïdes appliqués par voie topique ne doivent pas être utilisés largement sur les patients enceintes en grande quantité ou pendant des périodes prolongées. On ne sait pas si l'utilisation du spray kenalog est détectable dans le lait maternel. La prudence doit être exercée lorsque des corticostéroïdes topiques sont administrés à une femme infirmière. Le spray kenalog doit être utilisé avec prudence chez les enfants en raison d'une plus grande surface de la peau à un rapport de poids corporel les rend plus sensibles à la suppression surrénalienne du syndrome de Cushing et à l'hypertension intracrânienne qui ont été signalées chez les enfants recevant des corticostéroïdes topiques.
Informations Complémentaires
Notre centre de médicaments secondaires Kenalog Spray Effets offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
Pour une utilisation dermatologique uniquement
Pas pour une utilisation ophtalmique
Description du spray kenalog
The topical corticosteroids constitute a class of primarily synthetic steroids used as anti-inflammatory and antipruritic agents. The steroids in this class include triamcinolone acetonide. Triamcinolone acetonide is designated chemically as 9-fluoro-11β 16α 17 21-tetrahydroxypregna-1 4-diene-3 20-dione cyclic 16 17-acetal with acetone. The structural formula is:
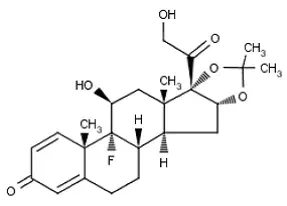 |
C 24 H 31 Foot 6
Une application de deux secondes qui couvre une zone approximativement la taille de la main offre une quantité d'acétonide de triamcinolone ne dépassant pas 0,2 mg. Après avoir pulvérisé le véhicule non volatile, le respect de la peau contient environ 0,2% d'acétonide de triamcinolone. Chaque gramme de pulvérisation fournit 0,147 mg d'acétonide de triamcinolone dans un véhicule d'alcool déshydraté de palmitate d'isopropyle (NULL,3%) et de propulseur isobutane.
petite pilule ovale bleue GG 258
Utilisations pour Kenalog Spray
Le spray kenalog (Aérosol topique de la triamcinolone USP) est indiqué pour le soulagement des manifestations inflammatoires et pruritiques des dermatoses sensibles aux corticostéroïdes.
Dosage pour le spray kenalog
Des instructions pour l'utilisation du pulvérisation peuvent être fournies sur l'étiquette. La préparation peut être appliquée sur n'importe quelle zone du corps, mais lorsqu'elle est pulvérisée, il faut prendre des soins faciaux pour voir que les yeux sont couverts et que l'inhalation du spray est évitée.
Le pulvérisation est inflammable; Évitez la flamme de chaleur ou fumez lorsque vous utilisez ce produit.
Trois ou quatre applications par jour de Kenalog Spray (aérosol topique de la triamcinolone acétonide) sont généralement adéquates.
Comment fourni
Kenalog Spray (Triamcinolone Acétonide Topical Aerosol USP)
63 g ( NDC 10631-093-62) Aérosol Can.
100 g ( NDC 10631-093-07) Aérosol Can.
Stockage et manipulation
Stocker à température ambiante; Évitez une chaleur excessive. Contenu sous pression; Ne percez pas et n'incitez pas. Restez hors de portée des enfants.
Pour signaler les effets indésirables suspects, contactez la FDA au 1-800-FDA-1088 ou www. FDA. Allez v / medwatch.
Ranbaxy Jacksonville FL 32257 USA. Révisé en juillet 2011
Effets secondaires pour le spray kenalog
Les réactions indésirables locales suivantes sont signalées rarement avec des corticostéroïdes topiques mais peuvent se produire plus fréquemment avec l'utilisation de pansements occlusifs (les réactions sont répertoriées dans un ordre approximatif de la baisse de la sécheresse d'irritation de l'irritation. striae et miliaria.
Interactions médicamenteuses pour Kenalog Spray
Aucune information fournie.
pulvérisation nasale atrovente en vente libre
Avertissements pour Kenalog Spray
Aucune information fournie.
Précautions pour le spray kenalog
Général
L'absorption systémique des corticostéroïdes topiques a produit des manifestations de suppression hypothalamique-hypophyso-surrénalienne (HPA) réversibles de l'hyperglycémie et de la glucosurie du syndrome de Gushing chez certains patients.
Les conditions qui augmentent l'absorption systémique incluent l'application des stéroïdes les plus puissants sur les grandes surfaces d'utilisation prolongée et l'ajout de pansements occlusifs.
Par conséquent, les patients recevant une grande dose de tout stéroïde topique puissant appliqué à une grande surface ou sous un pansement occlusif doivent être évalués périodiquement pour des preuves de suppression de HP A Axis en utilisant le cortisol libre urinaire et les tests de stimulation ACTH et pour une altération de l'homéostasie thermique. Si HP, une suppression ou une élévation de la température corporelle de l'axe, une tentative doit être faite pour retirer le médicament pour réduire la fréquence de substitut d'application un stéroïde moins puissant ou utiliser une approche séquentielle.
La récupération de la fonction HP A Axe et l'homéostasie thermique sont généralement promptes et complètes lors de l'arrêt du médicament. Des signes et des symptômes rarement de sevrage de stéroïdes peuvent survenir nécessitant des corticostéroïdes systémiques supplémentaires.
Les enfants peuvent absorber des quantités proportionnellement plus importantes de corticostéroïdes topiques et donc être plus sensible à la toxicité systémique (voir Précautions Utilisation pédiatrique ).
Qu'est-ce que le pantoprazole de 40 mg pour
Si l'irritation développe des corticostéroïdes topiques doit être interrompu et une thérapie appropriée instituée.
En présence d'infections dermatologiques, l'utilisation d'un agent antifongique ou antibactérien approprié doit être instituée. Si une réponse favorable ne se produit pas rapidement, le corticostéroïde doit être interrompu jusqu'à ce que l'infection ait été correctement contrôlée.
Tests de laboratoire
Un test urinaire de cortisol libre et un test de stimulation ACTH peut être utile pour évaluer la suppression de l'axe HPA.
Carcinogenèse Mutagenèse A trouble de la fertilité
Les études animales à long terme n'ont pas été réalisées pour évaluer le potentiel cancérigène ou l'effet sur la fertilité des corticostéroïdes topiques.
Des études pour déterminer la mutagénicité avec la prednisolone et l'hydrocortisone ont montré des résultats négatifs.
Grossesse: effets tératogènes
Category C. Corticosteroids are generally teratogenic in laboratory animals when administered systemically at relatively low dosage levels. The more potent corticosteroids have been shown to be teratogenic after dermal application in laboratory animals. There are no adequate and well-controlled studies in pregnant women on teratogenic effects from topically applied corticosteroids. Therefore topical corticosteroids should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus. Drugs of this class should not be used extensively on pregnant patients in large amounts or for prolonged periods of time.
Mères qui allaitent
On ne sait pas si l'administration topique de corticostéroïdes pourrait entraîner une absorption systémique suffisante pour produire des quantités détectables dans le lait maternel. Les corticostéroïdes systémiquement administrés sont sécrétés dans du lait maternel en quantités, peu susceptibles d'avoir un effet délétère sur le nourrisson. Néanmoins, la prudence doit être exercée lorsque des corticostéroïdes topiques sont administrés à une femme allaitée.
Usage pédiatrique
Les patients pédiatriques peuvent démontrer une plus grande sensibilité à la suppression topique de l'axe HPA induit par les corticostéroïdes et au syndrome de Cushing que les patients matures en raison d'une plus grande surface cutanée / rapport du poids corporel.
Le syndrome de Cushing de suppression de l'axe HPA et l'hypertension intracrânienne ont été signalés chez les enfants recevant des corticostéroïdes topiques. Les manifestations de la suppression surrénalienne chez les enfants comprennent le retard de croissance linéaire un gain de poids retardé à faible taux de cortisol plasmatique et l'absence de réponse à la stimulation de l'ACTH. Les manifestations de l'hypertension intracrânienne comprennent des maux de tête bombés et des maux de tête bilatéraux.
L'administration des corticostéroïdes topiques aux enfants doit être limitée au moins de montant compatible avec un régime thérapeutique efficace. La corticothérapie chronique peut interférer avec la croissance et le développement des enfants.
Informations sur la surdose pour Kenalog Spray
Les corticostéroïdes appliqués par voie topique peuvent être absorbés dans des quantités suffisantes pour produire des effets systémiques (voir PRÉCAUTIONS Général ).
Contre-indications pour le spray kenalog
Les corticostéroïdes topiques sont contre-indiqués chez les patients ayant des antécédents d'hypersensibilité à l'une des composantes des préparations.
Pharmacologie clinique for Kenalog Spray
Les corticostéroïdes topiques partagent des actions antipruritiques et vasoconstrictes anti-inflammatoires.
Le mécanisme de l'activité anti-inflammatoire des corticostéroïdes topiques n'est pas clair. Diverses méthodes de laboratoire, y compris des tests vasoconstricteurs, sont utilisées pour comparer et prédire les puissances et / ou les efficaces cliniques des corticostéroïdes topiques. Il existe des preuves suggérant qu'une corrélation reconnaissable existe entre la puissance vasoconstrictive et l'efficacité thérapeutique chez l'homme.
Quelle classification du médicament est le tramadol
Pharmacocinétique
L'étendue de l'absorption percutanée des corticostéroïdes topiques est déterminée par de nombreux facteurs, notamment le véhicule, l'intégrité de la barrière épidermique et l'utilisation de pansements occlusifs.
Les corticostéroïdes topiques peuvent être absorbés par la peau intacte normale. L'inflammation et / ou d'autres processus pathologiques de la peau augmentent l'absorption percutanée.
Une fois absorbée par la peau, les corticostéroïdes topiques sont manipulés par des voies pharmacocinétiques similaires aux corticostéroïdes administrés systémiquement. Les corticostéroïdes sont liés aux protéines plasmatiques à des degrés divers. Les corticostéroïdes sont métabolisés principalement dans le foie et sont ensuite excrétés par les reins. Certains des corticostéroïdes topiques et leurs métabolites sont également excrétés dans le même .
Informations sur les patients pour Kenalog Spray
Les patients utilisant le spray Kenalog devraient recevoir les informations et instructions suivantes:
- Ce médicament doit être utilisé comme indiqué par le médecin. Il est pour une utilisation externe uniquement; Évitez le contact avec les yeux et l'inhalation du spray.
- Les patients doivent être invités à ne pas utiliser ce médicament pour un trouble autre que pour lequel il a été prescrit.
- La zone cutanée traitée ne doit pas être bandée ou autrement couverte ou enveloppée de ce qui est occlusive à moins que le médecin ne soit dirigé par le médecin.
- Les patients doivent signaler tout signe de réactions indésirables locales.
- Les parents de patients pédiatriques doivent être invités à ne pas utiliser de couches serrées ou de pantalons en plastique sur un enfant traité dans la zone des couches car ces vêtements peuvent constituer des pansements occlusifs.
- N'utilisez pas de spray kenalog sur les aisselles ou les zones de l'aine sauf dirigés par votre médecin.
- Si aucune amélioration n'est observée dans les 2 semaines, contactez votre médecin.
- N'utilisez pas d'autres produits contenant des corticostéroïdes tout en utilisant un spray Kenalog sans d'abord consulter votre médecin.
- Le spray Kenalog est inflammable. Évitez les flammes thermiques ou fumez lors de l'application de spray kenalog.
