Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Inhibiteurs décarboxylasesStalevo
Résumé
Qu'est-ce que Stalevo?
Stalevo (Carbidopa Levodopa et Entacapone) est une combinaison de plusieurs médicaments utilisés pour traiter les symptômes de Parkinson tels que la rigidité musculaire tremble des spasmes et un mauvais contrôle musculaire. Levodopa est converti en un produit chimique appelé dopamine dans le cerveau. Symptômes Maladie de Parkinson Peut être causé par de faibles niveaux de dopamine dans le cerveau. La carbidopa aide à prévenir la ventilation de la lévodopa avant de pouvoir atteindre le cerveau et prendre effet. Lorsqu'il est utilisé avec la carbidopa et la lévodopa entacapone augmente les niveaux de lévodopa dans le corps.
Quels sont les effets secondaires de Stalevo?
Stalevo
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- Nouveau ou aggravant les spasmes musculaires
- Des yeux des yeux ou des contractions considérablement accrues
- évanouissement
- diarrhée
- changements de vision
- vision floue
- douleurs oculaires
- douleurs abdominales sévères
- tabourets noirs ou goudronneux
- Vomi qui ressemble à un marc de café
- sensibilité ou faiblesse de la douleur musculaire
- Changement de la quantité d'urine
- changements d'humeur
- confusion
- hallucinations
- Pensées de suicide
- persistant mal de gorge
- Saignement ou ecchymose facile
- fatigue inhabituelle
- picotement des mains ou des pieds
- Des pulsions fortes inhabituelles (augmentation des envies sexuelles de jeu)
- douleur thoracique
- fièvre
- raideur musculaire inhabituelle
- confusion sévère
- transpiration
- rythme cardiaque rapide ou irrégulier
- respiration rapide et
- étourdissements sévères
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires courants de Stalevo comprennent:
- diarrhée
- nausée
- vomissement
- mal de tête
- vertiges
- somnolence
- vision floue
- Douleurs d'estomac ou bouleversé
- perte d'appétit
- constipation
- bouche sèche
- changements dans votre sens du goût
- Rash ou démangeaisons de la peau
- Changements de peau inhabituels
- crampes musculaires
- maux de dos
- agitation
- anxiété
- difficulté à dormir (insomnie) ou
- étrange rêves .
Dites à votre médecin si vous avez des effets secondaires graves de Stalevo, notamment:
- involontaire Mouvements (en particulier les contractions de la paupière)
- évanouissement or falling
- difficulté à avaler
- Douleurs d'estomac / abdominal
- persistant diarrhée
- changements de vision (including vision floue)
- tabourets noirs / goudronneux
- douleur musculaire
- Changements dans la quantité d'urine
- Changements mentaux / d'humeur (comme la confusion hallucinations pensées de suicide)
- signes d'infection (par exemple
- Des pulsions fortes inhabituelles (comme l'augmentation du jeu ont augmenté les envies sexuelles).
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; Et des étourdissements soudains étourdissement ou s'évanouir;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Stalevo
La dose quotidienne optimale de Stalevo doit être déterminée pour chaque patient. La thérapie doit être individualisée et ajustée en fonction de la réponse thérapeutique souhaitée.
Quelles substances ou suppléments de médicaments interagissent avec Stalevo?
Stalevo peut interagir avec la cholestyramine d'apomorphine dobutamine épinéphrine isoniazide isoprotérenol méthyldopa métoclopramide papavérine phénytoïne probénécide antibiotique médicament contre la pression artérielle antidépresseurs médicaments pour traiter les troubles psychiatriques froids ou allergie Medicine Narcotics Sleaming Pills Muscle Mascle Médeures pour les convulsions ou les médicaments anti-anxiété. Dites à votre médecin tous les médicaments que vous prenez.
Stalevo pendant la grossesse et l'allaitement
Stalevo ne doit être utilisé que lorsqu'il est prescrit pendant la grossesse. Levodopa passe dans le lait maternel. On ne sait pas si la carbidopa ou l'entacapone passent dans le lait maternel. Consultez votre médecin avant l'allaitement.
Informations Complémentaires Notre centre de médicaments à effets secondaires de Stalevo (Carbidopa Levodopa et Entacapone) offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament. Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
/ H4> Description de Stalevo
Stalevo est une combinaison de Carbidopa levodopa et d'entacapone pour le traitement de la maladie de Parkinson.
Carbidopa Un inhibiteur de la décarboxylation des acides aminés aromatiques est un composé cristallin blanc légèrement soluble dans l'eau avec un poids moléculaire de 244,3. Il est désigné chimiquement comme (-) - L- (α-hydrazino- (α-méthyl-β- (34-dihydroxybenzène) monohydraté d'acide propanoïque. Sa formule empirique est C est C 10 H 14 N 2 O 4 · H 2 O et sa formule structurelle est:

La teneur en comprimés est exprimée en termes de carbidopa anhydre qui a un poids moléculaire de 226,3.
Levodopa Un acide aminé aromatique est un composé cristallin blanc légèrement soluble dans l'eau avec un poids moléculaire de 197,2. Il est désigné chimiquement comme (-) - L-α-amino-β- (34-dihydroxybenzène) acide propanoïque. Sa formule empirique est C 9 H 11 NON 4 Et sa formule structurelle est:

Entacapone Un inhibiteur du COMT est un composé structuré par nitro-catéchol avec un poids moléculaire de 305,3. Le nom chimique de l'entacapone est (E) -2-Cyano-3- (34-dihydroxy-5-nitrophényl) -NN-diéthyl-2-propénamide. Sa formule empirique est C 14 H 15 N 3 O 5 Et sa formule structurelle est:
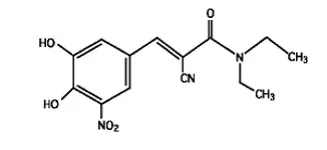
Stalevo est fourni sous forme de comprimés en 6 forces:
Stalevo 50: 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone
Stalevo 75: 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'Entacapone
Stalevo 100: 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone
Stalevo125: 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'Entacapone
Stalevo 150: 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'Entacapone
Stalevo 200: 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone
Ingrédients inactifs: Adon d'amidon de maïs croscarmellose de sodium glycérol 85% hypromellose magnésium stéarate de mannitol polysorbate 80 povidone saccharose oxyde de fer rouge et dioxyde de titane. Stalevo 50 Stalevo 100 et Stalevo 150 contiennent également de l'oxyde de fer jaune.
Utilisations pour Stalevo
Stalevo est indiqué pour le traitement de la maladie de Parkinson.
Stalevo peut être utilisé:
- Pour remplacer (par des résistances équivalentes de chacun des trois composantes), Carbidopa / Levodopa et Entacapone ont précédemment administré en tant que produits individuels.
- Pour remplacer la thérapie carbbidopa / lévodopa (sans entacapone) lorsque les patients éprouvent les signes et symptômes de la fin de la dose et lorsqu'ils ont pris une dose quotidienne totale de lévodopa de 600 mg ou moins et n'ont pas souffert de dyskinésies.
Dosage pour Stalevo
Stalevo doit être utilisé comme substitut des patients déjà stabilisés sur des doses équivalentes de carbidopa / lévodopa et d'entacapone. Cependant, certains patients qui ont été stabilisés sur une dose donnée de carbidopa / lévodopa peuvent être traités avec Stalevo si une décision a été prise pour ajouter l'entacapone (voir ci-dessous ). La thérapie doit être individualisée et ajustée en fonction de la réponse thérapeutique souhaitée.
Dossing Information
La dose quotidienne optimale de Stalevo doit être déterminée par un titrage minutieux chez chaque patient.
L'expérience clinique avec des doses quotidiennes supérieures à 1600 mg d'Entacapone est limitée. La dose quotidienne maximale recommandée de Stalevo dépend de la résistance utilisée. Le nombre maximum de comprimés à utiliser dans une période 24h / 24 est moindre avec la résistance la plus élevée (Stalevo 200) qu'avec des résistances inférieures (voir tableau 1). Des études montrent que la dopa décarboxylase périphérique est saturée par la carbidopa à environ 70 mg par jour à 100 mg par jour. Les patients recevant moins que cette quantité de carbidopa sont plus susceptibles de ressentir des nausées et des vomissements.
Tableau 1: Dose maximale recommandée de Stalevo dans une période de 24 heures
STALET DOSATION DE STALEVO Nombre maximum de comprimés dans une période de 24 heures Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 8 Stalevo 200 6
Convertir les patients de Carbidopa levodopa et entacapone en stalevo
Les patients actuellement traités avec Entacapone 200 mg avec chaque dose de comprimé carbidopa / lévodopa à libération non étendue peuvent passer à la force correspondante de Stalevo contenant les mêmes quantités de lévodopa et de carbidopa. Par exemple, les patients recevant un comprimé de carbidopa / lévodopa 25 mg / 100 mg et un comprimé d'Entacapone 200 mg à chaque administration peuvent passer à un seul comprimé Stalevo 100 (contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'Entacapone).
Conversion des patients des produits carbidopa et lévodopa en stalevo
Il n'y a aucune expérience dans le transfert de patients actuellement traités avec des formulations à libération prolongée de produits carbidopa / lévodopa ou carbidopa / lévodopa qui ne sont pas combinés dans un rapport 1: 4 de carbidopa à la lévodopa.
Les patients ayant des antécédents de dyskinésies modérés ou sévères ou de prendre plus de 600 mg de la composante Levodopa par jour nécessiteront probablement une réduction de leur dose de lévodopa quotidienne lorsque l'entacapone est ajouté. Étant donné que l'ajustement de la dose du composant de carbidopa ou de lévodopa individuel n'est pas possible avec des produits à dose fixe qui tirent initialement les patients à une dose qui est tolérée et qui répond à leur besoin thérapeutique individuel en utilisant un comprimé carbidopa / lévodopa séparé (rapport 1: 4) plus un comprimé Entacapone. Une fois que la dose individuelle du patient de dose de carbidopa / lévodopa plus entacapone a été établie à l'aide de deux comprimés distincts; Passez le patient à une tablette unique correspondante de Stalevo.
Lorsque moins de lévodopa est nécessaire, réduisez la dose quotidienne totale de carbidopa / lévodopa soit en diminuant la résistance de Stalevo à chaque administration, soit en diminuant la fréquence de l'administration en prolongeant le temps entre les doses.
Utilisation concomitante avec d'autres médicaments contre la maladie de l'anti-parkinson
Agents anticholinergiques dopamine Agonistes monoamine oxydase (MAO) - B inhibiteurs d'amantadine et autres médicaments standard pour la maladie de Parkinson peuvent être utilisés concomitamment pendant que Stalevo est administré; Cependant, les ajustements posologiques du médicament concomitant ou de la stalevo peuvent être nécessaires.
Diminuer ou interruption du dosage
Évitez l'interruption du dosage de Stalevo car l'hyperpyrexie a été signalée chez des patients qui interrompent soudainement ou réduisent leur utilisation de la lévodopa [voir Avertissements et précautions ].
Instructions d'administration importantes
Ne divisons pas les comprimés d'écrasement ou de mâcher les comprimés Stalevo. Administrer une seule tablette à chaque intervalle de dosage. Toutes les forces de Stalevo contiennent 200 mg d'entacapone. La combinaison de plusieurs comprimés ou parties de comprimés pour obtenir une dose de lévodopa plus élevée peut entraîner une surdose d'entacapone.
Administrer Stalevo avec ou sans nourriture. Cependant, un repas élevé en calories élevé peut retarder l'absorption de la lévodopa d'environ 2 heures [voir Pharmacologie clinique ].
Comment fourni
Formes et forces posologiques
Chaque comprimé Stalevo fourni dans 6 résistances à dose unique contient des carbidopa et des lévodopa dans un rapport 1: 4 et une dose de 200 mg d'entacapone. Stalevo (Carbidopa Levodopa et Entacapone) est fourni sous forme de comprimés enrobés de film pour l'administration orale dans les 6 points forts suivants:
Stalevo 50 comprimés enduits de film contenant 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone. Les comprimés ronds en forme de bi-convex sont le LCE 50 brunâtre ou grisâtre non scoré et en relief d'un côté.
Stalevo 75 comprimés enrobés de film contenant 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'entacapone. Les comprimés à calcul ovale sont rouges brunâtres légers et en relief avec du code LCE 75 d'un côté.
Stalevo 100 comprimés enrobés de film contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone. Les comprimés en forme d'oval sont brunâtres ou grisâtre non scorés et en relief 100 d'un côté.
Stalevo 125 comprimés enrobés de film contenant 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'entacapone. Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 125 d'un côté.
Stalevo 150 comprimés enrobés de film contenant 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'entacapone. Les comprimés en forme d'ellipse allongés sont le LCE 150 brunâtre ou rouge grisâtre ou en relief d'un côté.
Stalevo 200 comprimés enrobés de film contenant 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone. Les comprimés de forme ovale sont le rouge brunâtre foncé non scoré et le LCE 200 en relief d'un côté.
Stockage et manipulation
Stalevo (Carbidopa Levodopa et Entacapone) est fourni sous forme de comprimés enrobés de film pour l'administration orale dans les six forces suivantes:
Stalevo 50 film-coated tablets contenant 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone.
Les comprimés ronds en forme de bi-convex sont le LCE 50 brunâtre ou grisâtre non scoré et en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-805-01
Stalevo 75 film-coated tablets contenant 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 75 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-809-01
Stalevo 100 film-coated tablets contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont un lce 100 brunâtre ou grisâtre ou en relief de 100 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-816-01
Stalevo 125 film-coated tablets contenant 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 125 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-827-01
Stalevo 150 film-coated tablets contenant 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'entacapone.
Les comprimés en forme d'ellipse allongés sont le LCE 150 brunâtre ou rouge grisâtre ou en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-834-01
Stalevo 200 film-coated tablets contenant 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont le rouge brunâtre foncé non scoré et le LCE 200 en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-842-01
Stocker à 25 ° C (77 ° F); Excursions autorisées à 15 ° C à 30 ° C (59 ° F à 86 ° F).
[Voir Température ambiante contrôlée par l'USP .]
Dispenser dans un récipient serré (USP).
Fabriqué par: Orion Corporation Orion Pharma Orionintie 1 FI-02200 ESPOO FINLAND. Distribué par: Almatica Pharma LLC Morristown NJ 07960 USA. Révisé: mai 2020
Effets secondaires for Stalevo
Les effets indésirables suivants sont discutés plus en détail dans les sections des avertissements et précautions d'étiquetage:
- S'endormir pendant les activités de la vie quotidienne et de la somnolence [voir Avertissements et précautions ]
- Hypotension / Hypotension orthostatique et syncope [voir Avertissements et précautions ]
- Dyskinésie [voir Avertissements et précautions ]
- Dépression et suicidalité [voir Avertissements et précautions ]
- Hallucinations / comportement psychotique [voir Avertissements et précautions ]
- Contrôle des impulsions et / ou comportements compulsifs [voir Avertissements et précautions ]
- Hyperpyrexie et confusion émergentes du retrait [voir Avertissements et précautions ]
- Diarrhée et colite [voir Avertissements et précautions ]
- Rhabdomyolyse [voir Avertissements et précautions ]
- Maladie de l'ulcère gastroduoque [voir Avertissements et précautions ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, l'incidence des effets indésirables (nombre de patients uniques subissant une réaction indésirable associée au traitement / nombre total de patients traités) observés dans les essais cliniques d'un médicament ne peut pas être directement comparé à l'incidence des réactions indésirables dans les essais cliniques d'un autre médicament et ne peut pas refléter l'incidence des réactions indésirables observées dans la pratique clinique.
Entacapone
Les réactions indésirables les plus couramment observées (incidence au moins 3% supérieure à l'incidence du placebo) dans les essais à double aveugle carbibidopa-levodopa-placebo sur l'entacapone (n = 1003 patients) associés à l'utilisation de carbidopalevodopa-entacapone seuls et non vus à une fréquence équivalente parmi les patients traités par placement: dyskinesia dia-naiseAia-traited les hyperkines. Douleur vomir la bouche sèche et la décoloration de l'urine.
L'incidence de la différence de traitement pour l'arrêt prématuré de l'étude pour l'entacapone avec l'inhibiteur de la lévodopa et de la dopa décarboxylase dans les essais contrôlés par placebo en double aveugle était de 5%. L'incidence de la différence de traitement pour les causes les plus fréquentes de l'arrêt de l'étude était de 2% pour la diarrhée et 1% pour d'autres effets indésirables spécifiques, y compris les raisons psychiatriques, la dyskinésie / hyperkinésie nausée ou les douleurs abdominales.
Incidence de réaction indésirable dans les études cliniques contrôlées de l'entacapone
Le tableau 2 énumère le traitement des effets indésirables émergents qui se sont produits chez au moins 1% des patients traités par carbidopa / lévodopa et 200 mg d'entacapone qui ont participé aux études contrôlées par placebo en double aveugle et qui étaient numériquement plus fréquentes dans ce groupe que dans le groupe carbidopa / levodopa plus placebo. Dans ces études, l'entacapone ou le placebo ont été ajoutés à la carbidopa / lévodopa (ou bensérazide / lévodopa).
Tableau 2: Résumé des patients ayant des effets indésirables après le début de l'essai Administration du médicament au moins 1% dans le groupe Entacapone et supérieur au placebo
Réaction indésirable de la classe d'organes du système Carbidopa / lévodopa plus entacapone
(n = 603)% des patients Carbidopa / lévodopa plus placebo
(n = 400)% des patients Troubles de la peau et des appendices La transpiration a augmenté 2 1 Troubles du système musculo-squelettique Maux de dos 5 3 Troubles du système nerveux central et périphérique Dyskinésie 25 15 Hyperkinésie 10 5 Hypokinésie 9 8 Vertiges 8 6 Sens spéciaux d'autres troubles Perversion de goût 1 0 Troubles psychiatriques Anxiété 2 1 Somnolence 2 0 Agitation 1 0 Troubles du système gastro-intestinal Nausée 14 8 Diarrhée 10 4 Douleurs abdominales 8 4 Constipation 6 4 Vomissement 4 1 Séchée à la bouche 3 0 Dyspepsie 2 1 Flatulence 2 0 Gastrite 1 0 Troubles gastro-intestinaux nos 1 0 Troubles du système respiratoire Dyspnée 3 1 Saignement plaquettaire et coagulation Troubles Purpura 2 1 Troubles du système urinaire Décoloration de l'urine 10 0 Le corps comme troubles généraux Fatigue 6 4 Asthénie 2 1 Troubles du mécanisme de résistance Infection bactérienne 1 0
Expérience de commercialisation de la poste
Les rapports spontanés suivants d'événements indésirables associés temporairement à Entacapone ou à Stalevo ont été identifiés depuis l'introduction du marché et ne sont pas répertoriés dans le tableau 2. Parce que ces réactions sont signalées volontairement d'une population de taille inconnue, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à Entacone ou à l'exposition de Stalevo.
Une hépatite avec des caractéristiques principalement cholestatiques a été signalée.
Effets du sexe et de l'âge sur les effets indésirables
Aucune différence n'a été notée dans la vitesse des effets indésirables attribuables à l'entacapone seul par âge ou sexe.
Interactions médicamenteuses for Stalevo
Inhibiteurs du MAO
Les patients recevant des inhibiteurs de MAO non sélectifs et de la carbidopa levodopa et l'entacapone peuvent être à risque d'une augmentation du ton adrénergique. Par conséquent, l'utilisation de Stalevo est contre-indiquée chez les patients recevant des inhibiteurs non sélectifs de MAO [voir Contre-indications ].
Médicaments métabolisés par catéchol-o-méthyltransférase (COMT)
Les médicaments connus pour être métabolisés par COMT tels que l'isoprotérenol épinéphrine noradrénaline dopamine dobutamine alpha-méthyldopa apomorphine isoétherine et le bitoltérol doivent être administrés avec la prudence chez les patients recevant l'entacapone, indépendamment de la voie d'administration (y compris l'inclusion) car leur interaction peut entraîner une augmentation des rythmes car [voir Avertissements et précautions ].
Agents antihypertenseurs
Symptomatique hypotension posturale s'est produit lorsque des carbidopa / lévodopa ont été ajoutés au traitement des patients recevant des médicaments antihypertenseurs. Lors du démarrage du traitement avec une dose de stalevo, un ajustement de médicament antihypertenseur peut être nécessaire.
Antidépresseurs tricycliques
Il y a eu des rapports d'effets indésirables, notamment l'hypertension et la dyskinésie résultant de l'utilisation concomitante du tricyclique antidépresseurs et Carbidopa / Levodopa.
Antagonistes des récepteurs de la dopamine D2
Les antagonistes des récepteurs de la dopamine D2 (par exemple les phénothiazines de métoclopramide butyrophénones rispéridone) peuvent réduire les effets thérapeutiques de la lévodopa.
Isoniazide
Isoniazide may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Lable
Les effets bénéfiques de la lévodopa dans la maladie de Parkinson auraient été inversés par la phénytoïne. Les patients prenant de la phénytoïne avec du carbidopa / levodopa doivent être soigneusement observés pour la perte de réponse thérapeutique. La dose de Stalevo doit être augmentée comme nécessaire cliniquement chez les patients recevant de la phénytoïne.
Papaverne
Les effets bénéfiques de la lévodopa dans la maladie de Parkinson auraient été inversés par la papavérine. Les patients prenant de la papavérine avec une carbidopa / lévodopa doivent être soigneusement observés pour la perte de réponse thérapeutique. La dose de Stalevo doit être augmentée comme nécessaire cliniquement chez les patients recevant de la papavérine.
Sels de fer
Les sels de fer ou multi-vitamines contenant des sels de fer doivent être co-administrés avec prudence. Les sels de fer peuvent former des chélates avec la lévodopa carbidopa et l'entacapone et, par conséquent, la biodisponibilité de Levodopa carbidopa et de l'entacapone.
Médicaments connus pour interférer avec la glucuronidation de l'excrétion biliaire et la bêta-glucuronidase intestinale
Comme la plupart de l'excrétion entacapone est via le même La prudence doit être exercée lorsque les médicaments connus pour interférer avec la glucuronidation de l'excrétion biliaire et la bêta-glucuronidase intestinale sont donnés simultanément avec l'entacapone. Il s'agit notamment de la cholestyramine probénide et de certains antibiotiques (par exemple, érythromycine rifampicine ampicilline et chloramphénicol).
Médicaments métabolisés via CYP2C9 (par ex. Coumadin)
La posologie de Stalevo doit être ajustée comme nécessaire cliniquement chez les patients utilisant d'autres médicaments métabolisés via le CYP2C9. Une étude d'interaction chez des volontaires sains entacapone a augmenté l'ASC de R-warfarine en moyenne de 18% et les valeurs INR en moyenne de 13%. Des cas d'INR accrus chez les patients en utilisant concomitante la warfarine ont été signalés lors de l'utilisation post-approbation de l'entacapone. Ainsi, la surveillance de l'INR est recommandée lorsque le traitement de Stalevo est initié pour les patients recevant de la warfarine.
Avertissements pour Stalevo
Inclus dans le cadre du PRÉCAUTIONS section.
Précautions pour Stalevo
Les effets indésirables suivants décrits dans cette section sont liés à au moins l'une des composantes de Stalevo (c'est-à-dire Levodopa carbidopa et / ou entacapone) sur la base de l'expérience de sécurité dans les essais cliniques (en particulier des essais pivots) ou dans les rapports post-commercialisation.
S'endormir pendant les activités de la vie quotidienne et de la somnolence
Les patients atteints de la maladie de Parkinson traités avec Stalevo ou d'autres produits Carbidopa / Levodopa ont été soudainement endormis sans avertissement préalable de somnolence tout en se livrant à des activités de vie quotidienne (y compris l'exploitation des véhicules à moteur). Certains de ces épisodes ont abouti à des accidents. Bien que bon nombre de ces patients aient signalé une somnolence lors de la prise de l'entacapone, certains n'ont pas perçu des signes avant-coureurs tels que la somnolence excessive et pensaient qu'ils étaient alertes immédiatement avant l'événement. Certains de ces événements auraient eu lieu jusqu'à un an après le début du traitement.
Somnolence was reported in 2% of patients taking entacapone et 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for somnolence or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge somnolence or sleepiness until directly questioned about somnolence or sleepiness during specific activities. Patients who have already experienced somnolence et/or an episode of sudden sleep onset should not participate in these activities during treatment with Stalevo.
Avant de lancer un traitement avec Stalevo, conseille aux patients du potentiel de développer la somnolence et de poser des questions spécifiquement sur les facteurs qui peuvent augmenter ce risque tels que l'utilisation de médicaments sédatifs concomitants et la présence de troubles du sommeil. Si un patient développe une somnolence diurne ou des épisodes de s'endormir pendant les activités qui nécessitent une participation active (par exemple, les conversations alimentaires, etc.) Stalevo devrait généralement être interrompu [voir Posologie et administration et Avertissements et précautions ]. If the decision is made to continue Stalevo patients should be advised not to drive et to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Hypotension Orthostatic Hypotension And Syncope
Les rapports de syncope étaient généralement plus fréquents chez les patients des deux groupes de traitement qui avaient eu un épisode antérieur d'hypotension documentée (bien que les épisodes de syncope obtenus par l'histoire n'étaient pas eux-mêmes documentés avec une mesure vitale des signes). Hypotension L'hypotension et la syncope orthostatiques sont observées chez les patients traités avec des médicaments qui augmentent le ton dopaminergique central, y compris le stalevo.
Dyskinésie
Dyskinésie (involontaire movements) may occur or be exacerbated at lower dosages et sooner with Stalevo than with preparations containing only carbidopa et levodopa. The occurrence of dyskinesias may require dosage reduction.
Dans les essais pivots, l'incidence de la différence de traitement de la dyskinésie était de 10% et pour la carbidopa-levodopa plus 200 mg d'entacapone. Bien que la diminution de la dose de lévodopa puisse améliorer cet effet secondaire, de nombreux patients dans des essais contrôlés ont continué à ressentir des dyskinésies fréquentes malgré une réduction de leur dose de lévodopa. L'incidence de la différence de traitement du retrait de l'étude pour la dyskinésie était de 1% pour la carbidopa-levodopa-entacapone.
Dépression et suicidalité
Tous les patients doivent être observés avec soin pour le développement de la dépression avec des tendances suicidaires concomitantes. Les patients atteints de psychoses passées ou actuels doivent être traités avec prudence.
Hallucinations et / ou comportement psychotique
Le traitement dopaminergique chez les patients atteints de la maladie de Parkinson a été associé à des hallucinations. Les hallucinations ont conduit à l'arrêt des médicaments et au retrait prématuré des essais cliniques chez 0,8% et 0% des patients traités avec Carbidopa levodopa entacapone et Carbidopa levodopa respectivement. Les hallucinations ont conduit à l'hospitalisation chez 1,0% et 0,3% des patients des groupes Carbidopa Levodopa Entacapone et Carbidopa Levodopa respectivement. L'agitation s'est produite chez 1% des patients traités par Carbidopa levodopa entacapone et 0% traités par Carbidopa levodopa.
Contrôle des impulsions et / ou comportements compulsifs
Les rapports de commercialisation suggèrent que les patients traités par des médicaments anti-parkinson peuvent ressentir des envies intenses à jouer des envies sexuelles accrues à dépenser de l'argent incontrôlable et d'autres envies intenses. Les patients peuvent être incapables de contrôler ces envies tout en prenant un ou plusieurs des médicaments généralement utilisés pour le traitement de la maladie de Parkinson et qui augmentent le ton dopaminergique central, y compris l'entacapone prise avec la lévodopa et la carbidopa. Dans certains cas, bien que toutes ces envies n'étaient pas censées s'être arrêtées lorsque la dose de médicaments anti-parkinson a été réduite ou interrompue. Étant donné que les patients peuvent ne pas reconnaître ces comportements comme anormaux, il est important pour les prescripteurs de demander spécifiquement aux patients ou à leurs soignants sur le développement d'une augmentation des envies de jeu, les envies sexuelles dépensent des dépenses non contrôlées ou d'autres pulsions tout en étant traitées avec Entacapone. Les médecins devraient envisager la réduction de la dose ou l'arrêt de Stalevo si un patient développe de telles envies tout en prenant Stalevo [voir Posologie et administration Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Des cas d'hyperpyrexie et de confusion ressemblant au syndrome malin neuroleptique (NMS) ont été signalés en association avec la réduction de la dose ou le retrait du traitement avec la carbidopa levodopa et l'entacapone. Cependant, dans certains cas, l'hyperpyrexie et la confusion ont été signalées après le début du traitement par entacapone. L'hyperpyrexie et la confusion sont rares, mais elles peuvent être mortelles avec une variété de caractéristiques, notamment l'hyperpyrexie / la fièvre / l'hyperthermie rigidité musculaire Mouvements involontaires altérés conscience / l'état mental changent de la dysfonction autonome de la tachycardie Tachypnea Terming Hyper ou l'hypotension du laboratoire annoral (e.g.g. Créine Phosphinase Labation du lesicodase de la créatine (e.g.gosphokinase-likocinas licedosise le labotage annoral. myoglobinurie et augmentation de la myoglobine sérique).
Si un patient doit interrompre ou réduire sa dose quotidienne de Stalevo, la dose doit être diminuée lentement avec la supervision d'un fournisseur de soins de santé [voir Posologie et administration ]. Specific methods for tapering entacapone have not been systematically evaluated.
Diarrhée And Colitis
Dans les essais cliniques de diarrhée d'entacapone développés chez 60 sur 603 (NULL,0%) et 16 sur 400 (NULL,0%) des patients traités avec 200 mg d'entacapone ou de placebo en combinaison avec le lévodopa et l'inhibiteur de DOPA décarboxylase respectivement. Chez les patients traités par entacapone, la diarrhée était généralement légère à modérée en gravité (NULL,6%) mais était considérée comme sévère dans 1,3%. La diarrhée a entraîné un retrait chez 10 des 603 (NULL,7%) patients 7 (NULL,2%) avec une diarrhée légère et modérée et 3 (NULL,5%) avec une diarrhée sévère. La diarrhée a généralement résolu après l'arrêt de l'entacapone. Deux patients atteints de diarrhée ont été hospitalisés. Généralement, la diarrhée se présente dans les 4 à 12 semaines après le début de l'entacapone, mais elle peut apparaître dès la première semaine et aussi tard autant de mois après le début du traitement. La diarrhée peut être associée à une déshydratation de perte de poids et à une hypokaliémie.
L'expérience de la post-commercialisation a montré que la diarrhée peut être un signe de colite microscopique induite par le médicament principalement la colite lymphocytaire. Dans ces cas, la diarrhée a généralement été modérée à sévère aqueuse et sans folie parfois associée à la déshydratation de la perte de poids de douleur abdominale et à une hypokaliémie. Dans la majorité des cas, la diarrhée et d'autres symptômes liés à la colite ont résolu ou significativement amélioré lorsque le traitement à l'entacapone a été arrêté. Chez certains patients atteints de biopsie, la diarrhée a confirmé que la diarrhée s'était résolue ou significativement améliorée après l'arrêt de l'entacapone mais a été recourbé après le retraitement avec Entacapone.
Si une diarrhée prolongée est soupçonnée d'être liée à Stalevo, le médicament doit être interrompu et un traitement médical approprié considéré. Si la cause de la diarrhée prolongée reste claire ou se poursuit après l'arrêt de l'entacapone, des enquêtes diagnostiques supplémentaires, y compris la coloscopie et les biopsies, doivent être prises en compte.
Rhabdomyolyse
Des cas de rhabdomyolyse sévère ont été signalés avec Entacapone lorsqu'ils sont utilisés en combinaison avec la carbidopa et la lévodopa. Une activité motrice sévère prolongée, y compris la dyskinésie, peut éventuellement expliquer la rhabdomyolyse. La plupart des cas se sont manifestés par la myalgie et les valeurs accrues de la créatine phosphokinase (CPK) et de la myoglobine. Certaines réactions comprenaient également de la fièvre et / ou une altération de la conscience. Il est également possible que la rhabdomyolyse puisse être le résultat du syndrome décrit dans l'hyperpyrexie et la confusion émergentes du sevrage [voir [voir Avertissements et précautions ].
Interaction avec les médicaments métabolisés par comt
Les médicaments connus pour être métabolisés par le COMT tels que l'isoprotérénol épinéphrine norréphrine dopamine dopamine dobutamine alpha-méthyldopa apomorphine isoétherine et le bitoltérol doivent être administrés avec la prudence chez les patients qui réceptent l'entacapone, indépendamment de la voie d'administration (y compris une augmentation de la pression de l'homme) car leur interaction peut entraîner une augmentation du rythme car
Complications fibrotiques
Des cas d'infiltrats pulmonaires de la fibrose rétropéritonéale ont été signalés chez certains patients traités par des agents dopaminergiques dérivés d'ergot. Ces complications peuvent se résoudre lorsque le médicament est interrompu, mais une résolution complète ne se produit pas toujours. Bien que ces effets indésirables puissent être liés à la structure de l'ergoline de ces composés, un rôle causal possible des médicaments dérivés non ERGOT (par exemple l'entacapone levodopa) qui augmentent l'activité dopaminergique a également été pris en compte. L'incidence attendue de complications fibrotiques est si faible que même si l'entacapone provoquait ces complications à des taux similaires à ceux attribuables à d'autres thérapies dopaminergiques, il est peu probable qu'elle ait été détectée dans une cohorte de la taille exposée à l'entacapone pendant son développement clinique. Quatre cas de fibrose pulmonaire ont été signalés lors du développement clinique de l'entacapone; 3 de ces patients ont également été traités avec du pergolide et 1 avec de la bromocriptine. La durée du traitement avec Entacapone variait de 7 mois à 17 mois.
Maladie de l'ulcère gadin
Comme pour le traitement de la lévodopa avec Stalevo, peut augmenter la possibilité d'hémorragie gastro-intestinale supérieure chez les patients ayant des antécédents d'ulcère gastro-duodénal.
Trouble hépatique
Les patients souffrant de troubles hépatiques doivent être traités avec prudence [voir Pharmacologie clinique ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Tests de laboratoire
Des anomalies dans les tests de laboratoire peuvent inclure des élévations de tests de fonction hépatique tels que la phosphatase alcaline SGOT (AST) SGPT (ALT) déshydrogénase et bilirubine. Anomalies dans le sang urée Un test d'azote et de coombes positifs a également été signalé. Les niveaux couramment des niveaux d'azote de l'urée sanguine et de l'acide urique sont plus faibles pendant l'administration de Stalevo qu'avec levodopa.
Stalevo may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
La prudence doit être exercée lors de l'interprétation des taux plasmatiques et d'urine de catécholamines et de leurs métabolites chez les patients sous traitement carbidopa / lévodopa.
Informations de conseil des patients S'endormir pendant les activités de la vie quotidienne et de la somnolence
Conseillez les patients sur le potentiel d'effets sédatifs associés à Stalevo, y compris la somnolence et sur la possibilité de s'endormir tout en se livrant à des activités de vie quotidienne. Parce que la somnolence peut être une réaction indésirable fréquente avec des conséquences potentiellement graves, les patients ne devraient pas conduire un véhicule à moteur à faire fonctionner des machines lourdes ou s'engager dans d'autres activités potentiellement dangereuses jusqu'à ce qu'elles aient acquis une expérience suffisante avec STALEVO pour déterminer si cela affecte ou non leurs performances mentales et / ou motrices [voir adversation [voir Avertissements et précautions ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Conseiller aux patients de parler avec leur prescripteur de soins de santé avant de prendre des médicaments en séduisant ou d'autres dépresseurs du SNC (par exemple les antidépresseurs antipsychotiques benzodiazépines, etc.) en raison des effets additifs possibles en combinaison avec Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Informer les patients qu'ils peuvent développer une hypotension symptomatique (ou asymptomatique) posturale (orthostatique) ou une hypotension non orthostatique lors de la prise de Stalevo. L'hypotension / hypotension orthostatique peut se produire plus fréquemment pendant le traitement initial. Les patients ne devraient pas augmenter rapidement après s'asseoir ou se coucher, surtout s'ils l'ont fait pendant des périodes prolongées et surtout lors de l'initiation du traitement avec Stalevo.
Conseillez les patients sur le potentiel de syncope chez les patients utilisant des agonistes de dopamine. Pour cette raison, informer les patients de la possibilité de syncope tout en prenant Stalevo [voir Avertissements et précautions ].
Dyskinésies
Informer les patients que Stalevo peut provoquer et / ou exacerber les dyskinésies préexistantes [voir Avertissements et précautions ].
Hallucinations et / ou comportement psychotique
Informer les patients que les hallucinations et autres comportements de type psychotique peuvent se produire lors de la prise de Stalevo [voir Avertissements et précautions ].
Contrôle des impulsions et / ou comportements compulsifs
Informer les patients qu'ils peuvent ressentir des comportements de contrôle des impulsions et / ou compulsifs tout en prenant un ou plusieurs médicaments utilisés pour le traitement de la maladie de Parkinson, y compris Stalevo. Demandez aux patients sur le développement des envies de jeu nouvelles ou accrues les envies sexuelles les envies de dépenses incontrôlées ou d'autres envies intenses tout en étant traitées avec Stalevo. Conseiller aux patients d'informer leur médecin ou leur fournisseur de soins de santé s'ils connaissent des envies de jeu nouvelles ou accrues accrues les envies sexuelles ou d'autres envies intenses tout en prenant Stalevo. Les médecins devraient envisager la réduction de la dose ou l'arrêt du médicament si un patient développe de telles envies tout en prenant Stalevo [voir Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Informer les patients qu'ils peuvent développer de la fièvre et de la confusion dans le cadre d'un syndrome ressemblant à la NMS et éventuellement avec d'autres caractéristiques cliniques (par exemple, la rigidité musculaire dysfonctionnement hyper ou hypotension, etc.). Ce syndrome de fièvre et de confusion peut se produire particulièrement avec des réductions de dose ou un retrait de Stalevo mais peut également se développer après le début du traitement. Conseiller aux patients de contacter leur fournisseur de soins de santé s'ils souhaitent interrompre ou diminuer la dose de Stalevo et contacter un fournisseur de soins de santé s'ils développent de la fièvre et de la confusion [voir Avertissements et précautions ].
Diarrhée And Colitis
Informez les patients que la diarrhée peut se produire avec Stalevo et qu'il peut avoir un début retardé. Parfois, la diarrhée prolongée peut être causée par la colite (inflammation du gros intestin). Les patients atteints de diarrhée doivent boire des liquides pour maintenir une hydratation adéquate et surveiller la perte de poids. Si la diarrhée associée à STALEVO est prolongée, ce qui devrait entraîner la résolution. Si la diarrhée se poursuit après avoir arrêté des enquêtes de diagnostic à Stalevo peut être nécessaire. Dans certains cas, la diarrhée peut être associée à la colite [voir Avertissements et précautions ].
Rhabdomyolyse
Informer les patients qu'ils peuvent développer une rhabdomyolyse et une myalgie s'ils éprouvent une activité motrice prolongée, y compris la dyskinésie. Cet événement peut également être associé à la fièvre et à la confusion [voir Avertissements et précautions ].
Nausée And Vomissement
Informer les patients que Stalevo peut provoquer des nausées et des vomissements peuvent survenir plus fréquemment pendant le traitement initial et peuvent nécessiter un ajustement de la dose.
Instructions pour une utilisation
Demandez aux patients de prendre Stalevo uniquement comme prescrit. Demandez aux patients de ne prendre qu'un seul comprimé de Stalevo à chaque intervalle de dosage. Demandez aux patients de ne pas prendre plusieurs comprimés ou des portions supplémentaires de comprimés pour obtenir une dose plus élevée de lévodopa. Conseiller aux patients de ne pas séparer l'écrasement ou de mâcher Stalevo.
Informez le patient que Stalevo est une formulation de carbidopa / lévodopa combinée à l'entacapone conçu pour commencer la libération d'ingrédients dans les 30 minutes suivant l'ingestion. Il est important que Stalevo soit pris à intervalles réguliers selon le calendrier décrit par le médecin. ATTENTION Le patient de ne pas modifier le schéma posologique prescrit et de ne pas ajouter de médicaments antiparkinsoniens supplémentaires, y compris d'autres préparations carbidopa / lévodopa sans consulter d'abord le médecin.
Conseillez les patients que les épisodes interdits (le port de l'effet du médicament) se produisent à la fin de l'intervalle de dosage, mais des épisodes hors de terre imprévisibles peuvent se produire à tout moment. Conseillez au patient d'informer un fournisseur de soins de santé pour d'éventuels ajustements de traitement si une telle réponse pose un problème à la vie quotidienne du patient.
Conseillez les patients que la coloration foncée (brun rouge ou noir) peut apparaître dans l'urine ou la sueur de la salive après avoir pris Stalevo. Bien que la couleur semble être cliniquement insignifiante que les vêtements peuvent être décolorés.
Conseiller les patients qu'un changement de régime alimentaire en aliments riches en protéines peut retarder l'absorption de la lévodopa. Une acidité excessive retarde également la vidange de l'estomac, retardant ainsi l'absorption de la lévodopa. Les sels de fer (comme dans les comprimés multi-vitamines) peuvent également réduire l'efficacité de Stalevo.
Grossesse
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant la thérapie [voir Utiliser dans des populations spécifiques ].
Lactation
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils ont l'intention d'allaiter ou d'allaiter un nourrisson [voir Utiliser dans des populations spécifiques ].
Toxicologie non clinique Carcinogenèse Mutagenèse A trouble de la fertilité Cancérogenèse
Chez le rat, l'administration orale de carbidopa-levodopa pendant 2 ans n'a entraîné aucune preuve de cancérogénicité à des doses d'environ 2 fois (carbidopa) -4 fois (levodopa), la dose humaine maximale recommandée (MRHD).
Des études de cancérogénicité de deux ans de l'entacapone ont été menées chez des souris et des rats. Chez la souris, aucune augmentation des tumeurs n'a été observée à des doses orales de 100 200 et 400 mg / kg / jour. À la dose la plus élevée, les expositions au plasma (ASC) étaient 4 fois plus élevées que celles chez l'homme à la dose quotidienne maximale recommandée (MRDD) de 1600 mg. Chez le rat, des doses orales administrées de 20 90 ou 400 mg / kg / jour, une incidence accrue d'adénomes et de carcinomes tubulaires rénaux a été observée chez les hommes à la dose la plus élevée testée. Les AUC plasmatiques à la dose plus élevée non associée à une augmentation des tumeurs rénales (90 mg / kg / jour) étaient environ 5 fois chez l'homme au MRDD d'Entacapone.
Le potentiel cancérigène de l'entacapone administré en combinaison avec la carbidopa-levodopa n'a pas été évalué.
Mutagenèse
La carbidopa était mutagène dans le test de mutation inverse bactérienne in vitro (AME) en présence et en absence d'activation métabolique et dans le test de lymphome de souris in vitro (TK) en l'absence d'activation métabolique. La carbidopa était négative dans le test de micronucléus de souris in vivo.
Entacapone was mutagenic et clastogenic in the in vitro mouse lymphoma tk assay in the presence et absence of metabolic activation et was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapone either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus et in the Ames assays.
Altération de la fertilité
Dans les études de reproduction, aucun effet sur la fertilité n'a été trouvé chez le rat recevant la carbidopa-levodopa à des doses d'environ 2 fois (carbidopa) -4 fois (lévodopa) le MRHD.
Chez le rat traité par voie orale avec de l'entacapone (jusqu'à 700 mg / kg / jour), aucun effet sur la fertilité ou les performances de reproduction générale n'a été observée. Les expositions au plasma (ASC) à la dose la plus élevée testée étaient environ 30 fois chez l'homme au MRHD d'Entacapone. L'accouplement retardé était évident chez les femmes à la dose la plus élevée testée.
Utiliser dans des populations spécifiques Grossesse Résumé des risques
Il n'y a pas de données adéquates sur le risque de développement associé à l'utilisation de Stalevo chez les femmes enceintes. Chez les animaux, l'administration de carbidopa-levodopa ou d'entacapone pendant la grossesse était associée à une toxicité du développement, notamment des incidents accrus de malformations fœtales (voir Données ). Le risque de fond estimé de malformations congénitales et de fausse couche dans la population indiquée est inconnue. Dans la population générale américaine, les risques de fond estimés des principaux malformations congénitales et une fausse couche dans les grossesses cliniquement reconnues sont respectivement de 2 à 4% et 15 à 20%.
Données
Données sur les animaux
Dans les études non cliniques dans lesquelles une carbidopa-levodopa a été administrée à des animaux enceintes, des incidents accrus de malformations viscéraux et squelettiques ont été observés chez les lapins à toutes les doses et les rapports de carbidopa-levodopa testés qui variaient de 10 fois (carbidopa) -5 fois (levodopa) à 20 fois (carbidopa) - 10 fois de 1600 mg / jour. Chez le rat, il y a eu une diminution du nombre de chiots vivants délivrés par les barrages recevant environ deux fois (carbidopa) -five Times (Levodopa) le MRHD tout au long de l'organogenèse. Aucun effet sur les fréquences de malformation n'a été observé chez les souris recevant jusqu'à 20 fois le MRHD de Carbidopa-Levodopa.
Dans le développement des embryons-foetal, des études sur les animaux enceintes de l'entacapone ont reçu des doses allant jusqu'à 1000 mg / kg / jour (rats) ou 300 mg / kg / jour (lapins) tout au long de l'organogenèse. Une incidence accrue de variations fœtales était évidente dans les portées des rats traités avec la dose la plus élevée en l'absence de signes manifestes de toxicité maternelle. L'exposition à l'entacapone plasmatique maternelle (ASC) associée à cette dose était d'environ 34 fois celle chez l'homme au MRHD. Des fréquences accrues d'avortements et de résorption tardive / totale et une diminution des poids fœtaux ont été observés dans les portées de lapins traités avec des doses toxiques maternellement toxiques de 100 mg / kg / jour (AUC plasma inférieur à celle chez l'homme au MRHD) ou plus. Il n'y a eu aucune augmentation des taux de malformation dans ces études.
Lorsque l'entacapone a été administré à des rats femelles avant l'accouplement et pendant la gestation précoce, une incidence accrue d'anomalies oculaires fœtales (Macrophthalmia Microphthalmia anophtalmia) a été observée dans les portées des barrages traités avec des doses de 160 mg / kg / jour (plasma Aucs sept fois dans l'humain à la MRHD) ou plus dans l'absence de l'absence maternelle. Administration jusqu'à 700 mg / kg / jour (AUC plasma 28 fois chez l'homme au MRHD) aux rats pendant la dernière partie de la gestation et tout au long de la lactation n'a produit aucune preuve de déficience du développement chez la progéniture.
Lactation Résumé des risques
La lévodopa a été détectée dans le lait maternel après l'administration de Carbidopa-Levodopa. Il n'y a pas de données sur la présence d'entacapone ou de carbidopa dans le lait maternel les effets de la lévodopa carbidopa ou de l'entacapone sur le nourrisson allaité ou des effets sur la production de lait. Cependant, l'inhibition de la lactation peut se produire car la lévodopa diminue la sécrétion de prolactine [voir Pharmacologie clinique ]. Carbidopa et entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone et/or metabolites in milk up to 2 to 3 times that in plasma. The developmental et health benefits of breastfeeding should be considered along with the mother's clinical need for Stalevo et any potential adverse effects on the breastfed infant from Stalevo or from the underlying maternal condition.
Usage pédiatrique
La sécurité et l'efficacité des patients pédiatriques n'ont pas été établies.
Utilisation gériatrique
Sur le nombre total de sujets dans les études cliniques de Stalevo, 43,8% étaient âgés de 65 ans et plus, tandis que 7,2% avaient 75 ans et plus. Aucune différence globale de sécurité ou d'efficacité n'a été observée entre ces sujets et les sujets plus jeunes et d'autres expériences cliniques signalées n'ont pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes; Cependant, une plus grande sensibilité de certaines personnes âgées ne peut pas être exclue.
Stalevo tablets have not been studied in Maladie de Parkinson patients or in healthy volunteers older than 75 years [see Pharmacologie clinique ].
Trouble rénal
La déficience rénale n'affecte pas la pharmacocinétique de l'entacapone. Il n'y a pas d'études sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles rénaux [voir Pharmacologie clinique ].
Trouble hépatique Or Biliary Obstruction
Il n'y a pas d'études sur la pharmacocinétique de la carbidopa et de la lévodopa chez les patients souffrant de troubles hépatiques. Stalevo devrait être administré avec prudence aux patients présentant une obstruction biliaire ou une maladie hépatique, car l'excrétion biliaire semble être la principale voie d'excrétion de l'entacapone et de la déficience hépatique a eu un effet significatif sur la pharmacocinétique de l'entacapone lorsque 200 mg d'entacapone ont été administrés seuls [voir Pharmacologie clinique ].
Informations sur la surdose pour Stalevo
Signes et symptômes de surdosage
Il y a très peu de cas de surdose avec la lévodopa signalés dans la littérature publiée. Sur la base des informations disponibles, les symptômes aigus de la surdose de l'inhibiteur de la lévodopa et de la dopa décarboxylase devraient résulter d'une surstimulation dopaminergique. Les doses de quelques grammes peuvent entraîner des perturbations du SNC avec une probabilité croissante de perturbation cardiovasculaire (par exemple, une tachycardie d'hypotension) et des problèmes psychiatriques plus graves à des doses plus élevées. Un rapport isolé de la rhabdomyolyse et une autre d'insuffisance rénale transitoire suggèrent que la surdose de la lévodopa peut donner lieu à des complications systémiques secondaires à une surstimulation dopaminergique.
L'inhibition du COMT par le traitement à l'entacapone dépend de la dose. Une surdose massive d'entacapone peut théoriquement produire une inhibition à 100% de l'enzyme COMT chez les personnes empêchant ainsi l'O-méthylation de catéchols endogènes et exogènes.
Dans les essais cliniques, la dose unique d'entacapone la plus élevée administrée à l'homme était de 800 mg, ce qui a entraîné une concentration plasmatique de 14,1 mcg par ml. La dose quotidienne la plus élevée donnée aux humains était de 2400 mg administrée dans une étude à 400 mg six fois par jour avec une carbidopa / lévodopa pendant 14 jours chez 15 patients atteints de la maladie de Parkinson et dans une autre étude comme 800 mg trois fois par jour pendant 7 jours chez 8 volontaires sains. À cette dose quotidienne, les concentrations plasmatiques maximales d'Entacapone ont été en moyenne de 2,0 mcg par ml (à 45 min contre 1,0 mcg par ml et 1,2 mcg par ml avec 200 mg d'entacapone à 45 min.). Les douleurs abdominales et les selles lâches ont été les événements indésirables les plus couramment observés au cours de cette étude. Des doses quotidiennes pouvant atteindre 2000 mg d'entacapone ont été administrées comme 200 mg 10 fois par jour avec des carbidopa / lévodopa ou du bensérazide / lévodopa pendant au moins 1 an chez 10 patients pendant au moins 2 ans chez 8 patients et pendant au moins 3 ans chez 7 patients. Dans l'ensemble, cependant, l'expérience clinique avec des doses quotidiennes supérieures à 1600 mg est limitée.
Gestion de la surdosage
L'hospitalisation est conseillée et des mesures générales de soutien doivent être utilisées ainsi qu'un lavage gastrique immédiat et des doses répétées de charbon de bois au fil du temps. Cela peut accélérer l'élimination de l'entacapone en particulier en diminuant son absorption et sa réabsorption du tractus gastro-intestinal. Les liquides intraveineux doivent être administrés judicieusement et une voie aérienne adéquate.
La fonction circulatoire et rénale respiratoire doit être surveillée et les mesures de soutien appropriées utilisées. La surveillance électrocardiographique doit être instituée et le patient a soigneusement observé pour le développement d'arythmies; Si nécessaire, un traitement antiarythmique approprié doit être donné. La possibilité que le patient ait pris d'autres médicaments augmentant le risque d'interactions médicamenteuses (en particulier les médicaments structurés au catéchol) devrait être pris en considération. À ce jour, aucune expérience n'a été signalée avec dialyse; Par conséquent, sa valeur de surdosage n'est pas connue. Il est peu probable que l'hémodialyse ou l'héperfusion réduise les niveaux d'entacapone en raison de sa liaison élevée aux protéines plasmatiques. La pyridoxine n'est pas efficace pour inverser les actions de Stalevo.
Contre-indications pour Stalevo
Stalevo is contraindicated in patients:
- Prendre des inhibiteurs non sélectifs de la monoamine oxydase (MAO) (par exemple la phénelzine et la tranylcypromine). Ces inhibiteurs non sélectifs du MAO doivent être interrompus au moins deux semaines avant le début du traitement avec Stalevo.
- Avec un angle étroit glaucome .
Pharmacologie clinique for Stalevo
Mécanisme d'action Levodopa
Les preuves actuelles indiquent que les symptômes de la maladie de Parkinson sont liés à l'épuisement de la dopamine dans le corpus striatum. L'administration de dopamine est inefficace dans le traitement de la maladie de Parkinson car elle ne traverse pas la barrière hémato-encéphalique. Cependant, la lévodopa Le précurseur métabolique de la dopamine traverse la barrière hémato-encéphalique et est vraisemblablement converti en dopamine dans le cerveau. On pense que c'est le mécanisme par lequel Levodopa soulage les symptômes de la maladie de Parkinson.
Carbidopa
Lorsque la lévodopa est administrée par voie orale, elle est rapidement décarboxylée à la dopamine dans les tissus extracerébraux afin que seule une petite partie d'une dose donnée soit transportée inchangée vers le système nerveux central. La carbidopa inhibe la décarboxylation de la lévodopa périphérique rendant plus de lévodopa disponible pour l'accouchement au cerveau.
Entacapone
Entacapone is a selective et reversible inhibitor of catechol-O-methyltransferase (COMT).
COMT catalyse le transfert du groupe méthyle de S-adénosyl-l-méthionine vers le groupe phénolique de substrats qui contiennent une structure de catéchol. Les substrats physiologiques du COMT comprennent les dopa catécholamines (dopamine norcéréphrine et épinéphrine) et leurs métabolites hydroxylés. Lorsque la décarboxylation de la lévodopa est empêchée par la carbidopa comt devient l'enzyme métabolisante principale pour la lévodopa catalysant son métabolisme en 3-méthoxy-4-hydroxy-l-phénylalanine (3-OMD).
Pharmacocinétique
La pharmacocinétique des comprimés Stalevo a été étudiée chez des sujets sains (45 ans à 75 ans). Dans l'ensemble, la suite de l'administration de doses correspondantes de Levodopa carbidopa et de l'entacapone comme Stalevo ou en tant que produit carbidopa et lévodopa plus comprimés comtan (entacapone) Les concentrations plasmatiques moyennes de Levodopa carbidopa et de l'entacapone sont comparables.
Absorption et distribution
Levodopa et l'entacapone sont rapidement absorbés et éliminés et leur volume de distribution est modérément petit. La carbidopa est absorbée et éliminée légèrement plus lentement par rapport à la lévodopa et à l'entacapone. Il existe des variations inter et intra-individuelles substantielles dans l'absorption de Levodopa carbidopa et de l'entacapone en particulier concernant son CMAX.
L'effet alimentaire sur le comprimé Stalevo n'a pas été évalué. Parce que la lévodopa rivalise avec certains acides aminés pour le transport à travers la paroi intestinale, l'absorption de la lévodopa peut être altérée chez certains patients après avoir mangé un repas riche en protéines. Les repas riches en grands acides aminés neutres peuvent retarder et réduire l'absorption de la lévodopa [voir Informations de conseil des patients ].
Levodopa
Les propriétés pharmacocinétiques de la lévodopa après l'administration de comprimés de stalevo à dose unique (Carbidopa levodopa et entacapone) sont résumées dans le tableau 3.
Tableau 3: Caractéristiques pharmacocinétiques de la lévodopa avec différentes forces de comprimés de Stalevo (moyenne ± ET)
Résistance à la tablette AUC0 -∞ (nanogramme • H via ML) CMAX (nanogramme par ml) Tmax (h) 12,5 mg par 50 mg par 200 mg 1040 ± 314 470 ± 154 1,1 ± 0,5 25 mg par 100 mg par 200 mg 2910 ± 715 975 ± 247 1,4 ± 0,6 37,5 mg par 150 mg par 200 mg 3770 ± 1120 1270 ± 329 1,5 ± 0,9 50 mg par 200 mg par 200 mg 6115 ± 1536 1859 ± 455 1,76 ± 0,7
Levodopa is bound to plasma protein only to a minor extent (about 10% to 30%).
Carbidopa
Après l'administration de Stalevo en tant que dose unique pour des sujets mâles et féminins en bonne santé, la concentration maximale de carbidopa a été atteinte dans les 2,5 heures à 3,4 heures en moyenne. Le CMAX moyen variait d'environ 40 nanogrammes par ml à 225 nanogrammes par ml et l'ASC moyen de 170 nanogrammes • H par ml à 1200 nanogrammes • H par ml avec différentes résistances stalevo fournissant 12,5 mg 25 mg 37,5 mg ou 50 mg de carbidopa.
Carbidopa is approximately 36% bound to plasma protein.
Entacapone
Après l'administration de Stalevo en tant que dose unique pour des sujets mâles et féminins en bonne santé, la concentration maximale d'entacapone dans le plasma a été atteinte dans une heure à 1,2 heure en moyenne. Le CMAX moyen de l'entacapone était d'environ 1200 nanogrammes par ml à 1500 nanogrammes par ml et le nanogramme AUC 1250 • H par ml à 1750 nanagram • H par ml après l'administration de différentes résistances Stalevo fournissant tous 200 mg d'Entacapone.
La liaison à la protéine plasmatique de l'entacapone est de 98% sur la plage de concentration de 0,4 mcg par ml à 50 mcg par ml. Entacapone se lie principalement à l'albumine sérique.
Métabolisme et élimination
Levodopa
La demi-vie d'élimination de la lévodopa La fraction active de l'activité antiparkinsonienne était de 1,7 heures (intervalle de 1,1 heures à 3,2 heures).
Levodopa is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) et O-methylation by COMT.
Carbidopa
La demi-vie d'élimination de la carbidopa était en moyenne de 1,6 heures à 2 heures (intervalle de 0,7 à 4,0 heures).
Carbidopa is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid et α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapone
La demi-vie d'élimination de l'entacapone était en moyenne de 0,8 heure à 1 heure (NULL,3 heure à 4,5 heures).
Entacapone is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapone et the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent et 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 La dose marquée en C d'Entacapone 10% des parents et métabolites marqués est excrété dans l'urine et 90% dans les excréments.
En raison de la courte élimination, aucune véritable accumulation de lévodopa ou d'entacapone ne se produit lorsqu'elles sont administrées à plusieurs reprises.
Trouble rénal
Entacapone
La pharmacocinétique de l'entacapone a été étudiée après une seule dose d'entacapone de 200 mg chez des sujets avec des fonctions rénales normales modérées et gravement altérées sans la lévodopa et la coadmination de l'inhibiteur de la DOPA décarboxylase. Aucun effet significatif de la fonction rénale sur la pharmacocinétique de l'entacapone n'a été trouvé.
Levodopa And carbidopa
Aucune étude sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles rénaux.
Trouble hépatique
Entacapone
Les troubles hépatiques ont eu un effet significatif sur la pharmacocinétique de l'entacapone lorsque 200 mg d'entacapone ont été administrés seuls. Une seule dose de 200 mg d'entacapone sans levodopa et la co-administration de l'inhibiteur de la DOPA décarboxylase a montré des valeurs AUC et CMAX d'environ 2 fois plus élevées chez les patients ayant des antécédents d'alcoolisme et de déficience hépatique (n = 10) par rapport aux sujets normaux (n = 10). Tous les patients avaient une cirrhose hépatique prouvée par la biopsie causée par l'alcool. Selon Child-Pugh, 7 patients atteints d'une maladie du foie ont eu une déficience hépatique légère et 3 patients avaient une déficience hépatique modérée. Comme seulement environ 10% de la dose d'entacapone est excrété dans l'urine en tant que composé parent et excrétion biliaire du glucuronide conjugué semble être la principale voie d'excrétion de ce médicament. Stalevo doit être administré avec soin aux patients présentant une obstruction biliaire ou une maladie hépatique.
Levodopa And Carbidopa
Il n'y a pas d'études sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles hépatiques.
Utilisation gériatrique
Dans les études de pharmacocinétique menées chez des volontaires sains après une seule dose de carbidopa- lévodopa- et entacapone (comme stalevo ou en tant que comprimés de carbidopa / lévodopa et de comtan):
Levodopa
L'AUC de Levodopa est significativement (en moyenne 10% à 20%) plus élevée chez les personnes âgées (60 ans à 75 ans) que les sujets plus jeunes (45 ans à 60 ans). Il n'y a pas de différence significative dans le CMAX de la lévodopa entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 à 75 ans).
Carbidopa
Il n'y a pas de différence significative dans le CMAX et l'ASUC de la carbidopa entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 ans à 75 ans).
Entacapone
L'AUC de l'entacapone est significativement (en moyenne 15%) plus élevée chez les personnes âgées (60 ans à 75 ans) que les sujets plus jeunes (45 à 60 ans). Il n'y a pas de différence significative dans le CMAX de l'entacapone entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 à 75 ans).
Genre
Pharmacocinétique following a single dose of carbidopa levodopa et entacapone together either as Stalevo or as separate carbidopa/levodopa et Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Levodopa
L'exposition au plasma (AUC et CMAX) de la lévodopa est significativement plus élevée chez les femmes que les hommes (en moyenne 40% pour l'ASC et 30% pour CMAX). Ces différences s'expliquent principalement par le poids corporel. Une autre littérature publiée a montré un effet de genre significatif (concentrations plus élevées chez les femmes) même après correction du poids corporel.
Carbidopa
Il n'y a pas de différence entre les sexes dans la pharmacocinétique de la carbidopa.
Entacapone
Il n'y a pas de différence entre les sexes dans la pharmacocinétique de l'entacapone.
Études d'interaction médicamenteuse Médicament métabolisé par comt
Lorsqu'une seule dose d'entacapone de 400 mg a été donnée avec une isoprénaline intraveineuse (isoprotérénol) et une épinéphrine sans inhibiteur de la lévodopa et de la dopa décarboxylase coadmins, les changements maximaux moyens de la fréquence cardiaque pendant la perfusion étaient respectivement environ 50% et 80% plus élevés que le placebo pour l'isoprénaline et l'épinéphrine respectivement.
Les médicaments connus pour être métabolisés par COMT doivent être administrés avec prudence chez les patients recevant de l'entacapone quelle que soit la voie d'administration [voir Interactions médicamenteuses ].
Médicaments métabolisés via CYP2C9
En raison de son affinité avec le CYP2C9 in vitro, l'entacapone peut potentiellement interférer avec les médicaments avec le métabolisme dépendant de cette isoenzyme. Dans une étude d'interaction chez des volontaires sains, Entacapone a augmenté l'ASC de R-warfarine en moyenne de 18% et les valeurs INR ont augmenté en moyenne de 13% [voir Interactions médicamenteuses ].
Niveaux hormonaux
Des ingrédients de Stalevo Levodopa est connu pour déprimer la sécrétion de prolactine et augmenter hormone de croissance niveaux.
Études cliniques
L'efficacité de l'entacapone en complément de la lévodopa dans le traitement de la maladie de Parkinson a été établie dans trois études multicentriques multicentriques de 24 semaines en double aveugle à double aveugle chez les patients atteints de la maladie de Parkinson. Dans 2 de ces études (études 1 et 2), la maladie des patients fluctuait, c'est-à-dire, a été caractérisée par des périodes documentées de (périodes de fonctionnement relativement bon) et désactivées (périodes de fonctionnement relativement médiocre) malgré une thérapie par levodopa optimale. Il y a également eu une période de retrait après 6 mois de traitement. Dans le troisième essai, les patients n'étaient pas tenus de subir des fluctuations. Avant la partie contrôlée de ces études, les patients ont été stabilisés sur la lévodopa pendant 2 semaines à 4 semaines.
Il existe une expérience limitée en utilisant l'entacapone chez les patients qui ne souffrent pas de fluctuations.
Dans les études 1 et 2, les patients ont été randomisés pour recevoir un placebo ou un entacapone 200 mg administré en concomitance avec chaque dose de carbidopa / lévodopa (jusqu'à 10 fois par jour, mais les patients ont en moyenne 4 doses à 6 doses par jour). La partie en double aveugle des deux études a duré 6 mois. Les patients ont périodiquement enregistré le temps passé dans les états de marche et de désactivation dans les journaux intimes pendant toute la durée de l'essai. Dans une étude menée dans les pays nordiques, la principale mesure des résultats a été le temps moyen passé à l'état à l'état pendant un jour enregistré de 18 heures (6 h à minuit). Dans l'autre étude, la principale mesure des résultats était la proportion de temps éveillé passé plus de 24 heures à l'état.
En plus de la mesure principale des résultats, le temps passé à l'état hors de l'état a été évalué et les patients ont également été évalués par les sous-parties de l'échelle de notation de la maladie de Parkinson unifiée (UPDR) Une échelle d'évaluation multi-éléments fréquemment utilisée destiné à évaluer les activités de la thérapie (partie I) de la vie quotidienne (partie II) (partie V et VI); L'évaluation globale d'un enquêteur et du patient de l'état clinique, une échelle subjective de 7 points conçue pour évaluer le fonctionnement global de la maladie de Parkinson; et le changement de dose quotidienne de carbidopa / lévodopa.
rispéridone d'autres médicaments dans la même classe
Dans l'étude 1 171, les patients ont été randomisés dans 16 centres en Finlande, Norvège, la Suède et le Danemark (étude 1) qui ont tous reçu un inhibiteur concomitant de la lévodopa plus dopa décarboxylase (soit carbidopa / lévodopa ou bensérazide / lévodopa). Dans l'étude 2, 205 patients ont été randomisés dans 17 centres en Amérique du Nord (États-Unis et Canada); Tous les patients ont reçu une carbidopa / lévodopa concomitante.
Les tableaux suivants (tableau 4 et tableau 5) affichent les résultats de ces deux études:
Tableau 4: Résultats de l'efficacité de l'étude 1
Mesure primaire du journal intime (à partir d'une journée du journal de 18 heures) Base de base Changement par rapport à la ligne de base au mois 6 * valeur p contre placebo Heures de temps éveillé Placebo 9.2 0.1 - Entacapone 9.3 1.5 Moins de 0,001 Durée de l'heure après la dose de première am (HRS) Placebo 2.2 0.0 - Entacapone 2.1 0,2 Moins de 0,05 Mesures secondaires du journal intime (à partir d'une journée du journal de 18 heures) † Heures de congé Placebo 5.3 0.0 - Entacapone 5.5 -1.3 Moins de 0,001 Proportion de temps éveillé sur ‡ (%) Placebo 63.8 0.6 - Entacapone 62.7 9.3 Moins de 0,001 Levodopa Total Daily Dose (mg) Placebo 705 14 - Entacapone 701 -87 Moins de 0,001 Fréquence des apports quotidiens de la lévodopa Placebo 6.1 0.1 - Entacapone 6.2 - 0,4 Moins de 0,001 Autres mesures secondaires Base de base Changement par rapport à la ligne de base au mois 6 valeur p contre placebo Global (global) de l'enquêteur a amélioré§ § Placebo - 28 - Entacapone - 56 Moins de 0,01 Global (global) du patient a amélioré§ Placebo - 22 - Entacapone - 39 N.s.¶ UPDRS TOTAL Placebo 37.4 -1.1 - Entacapone 38.5 -4.8 Moins de 0,01 Moteur de monte Placebo 24.6 -0.7 - Entacapone 25.5 -3.3 Moins de 0,05 UPDRS ADL Placebo 11.0 -0.4 - Entacapone 11.2 -1.8 Moins de 0,05 *Signifier; Les valeurs du mois 6 représentent la moyenne des semaines 8 16 et 24 par mesure des résultats définis par le protocole.
† Les valeurs P pour les mesures secondaires sont des valeurs P nominales sans aucun ajustement pour la multiplicité.
‡ Pas un critère de terminaison pour cette étude mais un critère d'évaluation principal dans l'étude nord-américaine.
§ Au moins d'une catégorie change au point de terminaison.
¶S pas significatif.
Tableau 5: Résultats de l'efficacité de l'étude 2
Mesure primaire du journal intime (pour une journée de journal 24h / 24) Base de base Changement par rapport à la ligne de base au mois 6 * valeur p contre placebo Pour cent de temps éveillé Placebo 60.8 2.0 - Entacapone 60.0 6.7 Moins de 0,05 Mesures secondaires du journal intime (pour une journée du journal 24h / 24) † Heures de congé Placebo 6.6 -0.3 - Entacapone 6.8 -1.2 Moins de 0,01 Heures de temps éveillé Placebo 10.3 0.4 - Entacapone 10.2 1.0 N.S. ‡ Levodopa Total Daily Dose (mg) Placebo 758 19 - Entacapone 804 -93 Moins de 0,001 Fréquence des apports quotidiens de la lévodopa Placebo 6.0 0,2 - Entacapone 6.2 0.0 N.S. ‡ Autres mesures secondaires† Base de base Changement par rapport à la ligne de base au mois 6 valeur p contre placebo Global (global) de l'enquêteur a amélioré§ § Placebo - 21 - Entacapone - 34 Moins de 0,05 Global (global) du patient a amélioré§ Placebo - 20 - Entacapone - 31 Moins de 0,05 UPDRS TOTAL¶ Placebo 35.6 2.8 - Entacapone 35.1 -0.6 Moins de 0,05 Moteur de monte ¶ Placebo 22.6 1.2 - Entacapone 22.0 -0.9 Moins de 0,05 UPDRS ADL¶ Placebo 11.7 1.1 - Entacapone 11.9 0.0 Moins de 0,05 *Signifier; Les valeurs du mois 6 représentent la moyenne des semaines 8 16 et 24 par mesure des résultats définis par le protocole.
† Les valeurs P pour les mesures secondaires sont des valeurs P nominales sans aucun ajustement pour la multiplicité.
‡ Pas significatif.
§ Au moins d'une catégorie change au point de terminaison.
¶Score Change à un point final similaire à l'étude nordique.
Les effets sur le temps ne différaient pas par l'âge de poids sexuel La gravité de la maladie à la dose de lévodopa de base et un traitement simultané avec des agonistes de dopamine ou de la sélégiline.
Retrait de l'entacapone
Dans l'étude 2, un retrait brusque de l'entacapone sans altération de la dose de carbidopa / lévodopa a entraîné une aggravation significative des fluctuations par rapport au placebo. Dans certains cas, les symptômes étaient légèrement pires qu'au départ, mais sont revenus à une gravité approximativement de base dans les 2 semaines suivant l'augmentation de la dose de levodopa en moyenne de 80 mg. Dans l'étude 1, une aggravation significative des symptômes parkinsoniens a été observée après le retrait de l'entacapone, comme évalué 2 semaines après le retrait du médicament. À cette phase, les symptômes étaient approximativement à la gravité de base après l'augmentation de la dose de levodopa d'environ 50 mg.
Dans le troisième essai contrôlé par placebo (étude 3), un total de 301 patients ont été randomisés dans 32 centres en Allemagne et en Autriche. Dans cet essai, comme dans les 2 autres études, Entacapone 200 mg a été administré avec chaque dose d'inhibiteur de la lévodopa et de la dopa décarboxylase (jusqu'à 10 fois par jour) et les parties II et III totales et iii et le total au temps étaient les principales mesures de l'efficacité. Les résultats des mesures primaires ainsi que pour certaines mesures secondaires sont présentés dans le tableau 6.
Tableau 6: Résultats de l'efficacité de l'étude 3
Mesures primaires Base de base Changement par rapport à la ligne de base au mois 6 valeur p contre placebo (LOCF) UPDRSADL * Placebo 12.0 0,5 - Entacapone 12.4 -0.4 Moins de 0,05 Moteur de monte* Placebo 24.1 0.1 - Entacapone 24.9 -2.5 Moins de 0,05 Heures de temps éveillé (Home Diary)† Placebo 10.1 0,5 - Entacapone 10.2 1.1 N.S. ‡ Mesures secondaires§ Base de base Changement par rapport à la ligne de base au mois 6 valeur p contre placebo UPDRS TOTAL * Placebo 37.7 0.6 - Entacapone 39.0 -3.4 Moins de 0,05 Pour cent de temps éveillé (Home Diary) ** Placebo 59.8 3.5 - Entacapone 62.0 6.5 N.S. ‡ Heures de congé (Home Diary) Placebo 6.8 -0.6 - Entacapone 6.3 -1.2 0.07 Levodopa Total Daily Dose (mg)* Placebo 572 4 - Entacapone 566 -35 N.S. Fréquence de l'apport quotidien de la lévodopa * Placebo 5.6 0,2 - Entacapone 5.4 0.0 Moins de 0,01 Global (global)% amélioréoit Placebo - 34 - Entacapone - 38 N.S. ‡ * Population totale; changement de score au point de terminaison.
† fluctuant de la population avec 5 doses à 10 doses; changement de score au point de terminaison.
‡ Pas significatif.
Les valeurs §p pour les mesures secondaires sont des valeurs p nominales sans aucun ajustement pour la multiplicité.
¶Population totale; Au moins une catégorie change au point final.
Informations sur les patients pour Stalevo
S'endormir pendant les activités de la vie quotidienne et de la somnolence
Conseillez les patients sur le potentiel d'effets sédatifs associés à Stalevo, y compris la somnolence et sur la possibilité de s'endormir tout en se livrant à des activités de vie quotidienne. Parce que la somnolence peut être une réaction indésirable fréquente avec des conséquences potentiellement graves, les patients ne devraient pas conduire un véhicule à moteur à faire fonctionner des machines lourdes ou s'engager dans d'autres activités potentiellement dangereuses jusqu'à ce qu'elles aient acquis une expérience suffisante avec STALEVO pour déterminer si cela affecte ou non leurs performances mentales et / ou motrices [voir adversation [voir Avertissements et précautions ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Conseiller aux patients de parler avec leur prescripteur de soins de santé avant de prendre des médicaments en séduisant ou d'autres dépresseurs du SNC (par exemple les antidépresseurs antipsychotiques benzodiazépines, etc.) en raison des effets additifs possibles en combinaison avec Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Informer les patients qu'ils peuvent développer une hypotension symptomatique (ou asymptomatique) posturale (orthostatique) ou une hypotension non orthostatique lors de la prise de Stalevo. L'hypotension / hypotension orthostatique peut se produire plus fréquemment pendant le traitement initial. Les patients ne devraient pas augmenter rapidement après s'asseoir ou se coucher, surtout s'ils l'ont fait pendant des périodes prolongées et surtout lors de l'initiation du traitement avec Stalevo.
Conseillez les patients sur le potentiel de syncope chez les patients utilisant des agonistes de dopamine. Pour cette raison, informer les patients de la possibilité de syncope tout en prenant Stalevo [voir Avertissements et précautions ].
Dyskinésies
Informer les patients que Stalevo peut provoquer et / ou exacerber les dyskinésies préexistantes [voir Avertissements et précautions ].
Hallucinations et / ou comportement psychotique
Informer les patients que les hallucinations et autres comportements de type psychotique peuvent se produire lors de la prise de Stalevo [voir Avertissements et précautions ].
Contrôle des impulsions et / ou comportements compulsifs
Informer les patients qu'ils peuvent ressentir des comportements de contrôle des impulsions et / ou compulsifs tout en prenant un ou plusieurs médicaments utilisés pour le traitement de la maladie de Parkinson, y compris Stalevo. Demandez aux patients sur le développement des envies de jeu nouvelles ou accrues les envies sexuelles les envies de dépenses incontrôlées ou d'autres envies intenses tout en étant traitées avec Stalevo. Conseiller aux patients d'informer leur médecin ou leur fournisseur de soins de santé s'ils connaissent des envies de jeu nouvelles ou accrues accrues les envies sexuelles ou d'autres envies intenses tout en prenant Stalevo. Les médecins devraient envisager la réduction de la dose ou l'arrêt du médicament si un patient développe de telles envies tout en prenant Stalevo [voir Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Informer les patients qu'ils peuvent développer de la fièvre et de la confusion dans le cadre d'un syndrome ressemblant à la NMS et éventuellement avec d'autres caractéristiques cliniques (par exemple, la rigidité musculaire dysfonctionnement hyper ou hypotension, etc.). Ce syndrome de fièvre et de confusion peut se produire particulièrement avec des réductions de dose ou un retrait de Stalevo mais peut également se développer après le début du traitement. Conseiller aux patients de contacter leur fournisseur de soins de santé s'ils souhaitent interrompre ou diminuer la dose de Stalevo et contacter un fournisseur de soins de santé s'ils développent de la fièvre et de la confusion [voir Avertissements et précautions ].
Diarrhée And Colitis
Informez les patients que la diarrhée peut se produire avec Stalevo et qu'il peut avoir un début retardé. Parfois, la diarrhée prolongée peut être causée par la colite (inflammation du gros intestin). Les patients atteints de diarrhée doivent boire des liquides pour maintenir une hydratation adéquate et surveiller la perte de poids. Si la diarrhée associée à STALEVO est prolongée, ce qui devrait entraîner la résolution. Si la diarrhée se poursuit après avoir arrêté des enquêtes de diagnostic à Stalevo peut être nécessaire. Dans certains cas, la diarrhée peut être associée à la colite [voir Avertissements et précautions ].
Rhabdomyolyse
Informer les patients qu'ils peuvent développer une rhabdomyolyse et une myalgie s'ils éprouvent une activité motrice prolongée, y compris la dyskinésie. Cet événement peut également être associé à la fièvre et à la confusion [voir Avertissements et précautions ].
Nausée And Vomissement
Informer les patients que Stalevo peut provoquer des nausées et des vomissements peuvent survenir plus fréquemment pendant le traitement initial et peuvent nécessiter un ajustement de la dose.
Instructions pour une utilisation
Demandez aux patients de prendre Stalevo uniquement comme prescrit. Demandez aux patients de ne prendre qu'un seul comprimé de Stalevo à chaque intervalle de dosage. Demandez aux patients de ne pas prendre plusieurs comprimés ou des portions supplémentaires de comprimés pour obtenir une dose plus élevée de lévodopa. Conseiller aux patients de ne pas séparer l'écrasement ou de mâcher Stalevo.
Informez le patient que Stalevo est une formulation de carbidopa / lévodopa combinée à l'entacapone conçu pour commencer la libération d'ingrédients dans les 30 minutes suivant l'ingestion. Il est important que Stalevo soit pris à intervalles réguliers selon le calendrier décrit par le médecin. ATTENTION Le patient de ne pas modifier le schéma posologique prescrit et de ne pas ajouter de médicaments antiparkinsoniens supplémentaires, y compris d'autres préparations carbidopa / lévodopa sans consulter d'abord le médecin.
Conseillez les patients que les épisodes interdits (le port de l'effet du médicament) se produisent à la fin de l'intervalle de dosage, mais des épisodes hors de terre imprévisibles peuvent se produire à tout moment. Conseillez au patient d'informer un fournisseur de soins de santé pour d'éventuels ajustements de traitement si une telle réponse pose un problème à la vie quotidienne du patient.
Conseillez les patients que la coloration foncée (brun rouge ou noir) peut apparaître dans l'urine ou la sueur de la salive après avoir pris Stalevo. Bien que la couleur semble être cliniquement insignifiante que les vêtements peuvent être décolorés.
Conseiller les patients qu'un changement de régime alimentaire en aliments riches en protéines peut retarder l'absorption de la lévodopa. Une acidité excessive retarde également la vidange de l'estomac, retardant ainsi l'absorption de la lévodopa. Les sels de fer (comme dans les comprimés multi-vitamines) peuvent également réduire l'efficacité de Stalevo.
Grossesse
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant la thérapie [voir Utiliser dans des populations spécifiques ].
Lactation
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils ont l'intention d'allaiter ou d'allaiter un nourrisson [voir Utiliser dans des populations spécifiques ].
Description de Stalevo
Stalevo est une combinaison de Carbidopa levodopa et d'entacapone pour le traitement de la maladie de Parkinson.
Carbidopa Un inhibiteur de la décarboxylation des acides aminés aromatiques est un composé cristallin blanc légèrement soluble dans l'eau avec un poids moléculaire de 244,3. Il est désigné chimiquement comme (-) - L- (α-hydrazino- (α-méthyl-β- (34-dihydroxybenzène) monohydraté d'acide propanoïque. Sa formule empirique est C est C 10 H 14 N 2 O 4 · H 2 O et sa formule structurelle est:
 |
La teneur en comprimés est exprimée en termes de carbidopa anhydre qui a un poids moléculaire de 226,3.
Levodopa Un acide aminé aromatique est un composé cristallin blanc légèrement soluble dans l'eau avec un poids moléculaire de 197,2. Il est désigné chimiquement comme (-) - L-α-amino-β- (34-dihydroxybenzène) acide propanoïque. Sa formule empirique est C 9 H 11 NON 4 Et sa formule structurelle est:
 |
Entacapone Un inhibiteur du COMT est un composé structuré par nitro-catéchol avec un poids moléculaire de 305,3. Le nom chimique de l'entacapone est (E) -2-Cyano-3- (34-dihydroxy-5-nitrophényl) -NN-diéthyl-2-propénamide. Sa formule empirique est C 14 H 15 N 3 O 5 Et sa formule structurelle est:
 |
Stalevo est fourni sous forme de comprimés en 6 forces:
Stalevo 50: 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone
Stalevo 75: 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'Entacapone
Stalevo 100: 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone
Stalevo125: 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'Entacapone
Stalevo 150: 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'Entacapone
Stalevo 200: 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone
Ingrédients inactifs: Adon d'amidon de maïs croscarmellose de sodium glycérol 85% hypromellose magnésium stéarate de mannitol polysorbate 80 povidone saccharose oxyde de fer rouge et dioxyde de titane. Stalevo 50 Stalevo 100 et Stalevo 150 contiennent également de l'oxyde de fer jaune.
Utilisations pour Stalevo
Stalevo est indiqué pour le traitement de la maladie de Parkinson.
Stalevo peut être utilisé:
- Pour remplacer (par des résistances équivalentes de chacun des trois composantes), Carbidopa / Levodopa et Entacapone ont précédemment administré en tant que produits individuels.
- Pour remplacer la thérapie carbbidopa / lévodopa (sans entacapone) lorsque les patients éprouvent les signes et symptômes de la fin de la dose et lorsqu'ils ont pris une dose quotidienne totale de lévodopa de 600 mg ou moins et n'ont pas souffert de dyskinésies.
Dosage pour Stalevo
Stalevo doit être utilisé comme substitut des patients déjà stabilisés sur des doses équivalentes de carbidopa / lévodopa et d'entacapone. Cependant, certains patients qui ont été stabilisés sur une dose donnée de carbidopa / lévodopa peuvent être traités avec Stalevo si une décision a été prise pour ajouter l'entacapone (voir ci-dessous ). La thérapie doit être individualisée et ajustée en fonction de la réponse thérapeutique souhaitée.
Dossing Information
La dose quotidienne optimale de Stalevo doit être déterminée par un titrage minutieux chez chaque patient.
L'expérience clinique avec des doses quotidiennes supérieures à 1600 mg d'Entacapone est limitée. La dose quotidienne maximale recommandée de Stalevo dépend de la résistance utilisée. Le nombre maximum de comprimés à utiliser dans une période 24h / 24 est moindre avec la résistance la plus élevée (Stalevo 200) qu'avec des résistances inférieures (voir tableau 1). Des études montrent que la dopa décarboxylase périphérique est saturée par la carbidopa à environ 70 mg par jour à 100 mg par jour. Les patients recevant moins que cette quantité de carbidopa sont plus susceptibles de ressentir des nausées et des vomissements.
Tableau 1: Dose maximale recommandée de Stalevo dans une période de 24 heures
| STALET DOSATION DE STALEVO | Nombre maximum de comprimés dans une période de 24 heures |
| Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 | 8 |
| Stalevo 200 | 6 |
Convertir les patients de Carbidopa levodopa et entacapone en stalevo
Les patients actuellement traités avec Entacapone 200 mg avec chaque dose de comprimé carbidopa / lévodopa à libération non étendue peuvent passer à la force correspondante de Stalevo contenant les mêmes quantités de lévodopa et de carbidopa. Par exemple, les patients recevant un comprimé de carbidopa / lévodopa 25 mg / 100 mg et un comprimé d'Entacapone 200 mg à chaque administration peuvent passer à un seul comprimé Stalevo 100 (contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'Entacapone).
Conversion des patients des produits carbidopa et lévodopa en stalevo
Il n'y a aucune expérience dans le transfert de patients actuellement traités avec des formulations à libération prolongée de produits carbidopa / lévodopa ou carbidopa / lévodopa qui ne sont pas combinés dans un rapport 1: 4 de carbidopa à la lévodopa.
Les patients ayant des antécédents de dyskinésies modérés ou sévères ou de prendre plus de 600 mg de la composante Levodopa par jour nécessiteront probablement une réduction de leur dose de lévodopa quotidienne lorsque l'entacapone est ajouté. Étant donné que l'ajustement de la dose du composant de carbidopa ou de lévodopa individuel n'est pas possible avec des produits à dose fixe qui tirent initialement les patients à une dose qui est tolérée et qui répond à leur besoin thérapeutique individuel en utilisant un comprimé carbidopa / lévodopa séparé (rapport 1: 4) plus un comprimé Entacapone. Une fois que la dose individuelle du patient de dose de carbidopa / lévodopa plus entacapone a été établie à l'aide de deux comprimés distincts; Passez le patient à une tablette unique correspondante de Stalevo.
Lorsque moins de lévodopa est nécessaire, réduisez la dose quotidienne totale de carbidopa / lévodopa soit en diminuant la résistance de Stalevo à chaque administration, soit en diminuant la fréquence de l'administration en prolongeant le temps entre les doses.
Utilisation concomitante avec d'autres médicaments contre la maladie de l'anti-parkinson
Agents anticholinergiques dopamine Agonistes monoamine oxydase (MAO) - B inhibiteurs d'amantadine et autres médicaments standard pour la maladie de Parkinson peuvent être utilisés concomitamment pendant que Stalevo est administré; Cependant, les ajustements posologiques du médicament concomitant ou de la stalevo peuvent être nécessaires.
Diminuer ou interruption du dosage
Évitez l'interruption du dosage de Stalevo car l'hyperpyrexie a été signalée chez des patients qui interrompent soudainement ou réduisent leur utilisation de la lévodopa [voir Avertissements et précautions ].
Instructions d'administration importantes
Ne divisons pas les comprimés d'écrasement ou de mâcher les comprimés Stalevo. Administrer une seule tablette à chaque intervalle de dosage. Toutes les forces de Stalevo contiennent 200 mg d'entacapone. La combinaison de plusieurs comprimés ou parties de comprimés pour obtenir une dose de lévodopa plus élevée peut entraîner une surdose d'entacapone.
Administrer Stalevo avec ou sans nourriture. Cependant, un repas élevé en calories élevé peut retarder l'absorption de la lévodopa d'environ 2 heures [voir Pharmacologie clinique ].
Comment fourni
Formes et forces posologiques
Chaque comprimé Stalevo fourni dans 6 résistances à dose unique contient des carbidopa et des lévodopa dans un rapport 1: 4 et une dose de 200 mg d'entacapone. Stalevo (Carbidopa Levodopa et Entacapone) est fourni sous forme de comprimés enrobés de film pour l'administration orale dans les 6 points forts suivants:
Stalevo 50 comprimés enduits de film contenant 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone. Les comprimés ronds en forme de bi-convex sont le LCE 50 brunâtre ou grisâtre non scoré et en relief d'un côté.
Stalevo 75 comprimés enrobés de film contenant 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'entacapone. Les comprimés à calcul ovale sont rouges brunâtres légers et en relief avec du code LCE 75 d'un côté.
Stalevo 100 comprimés enrobés de film contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone. Les comprimés en forme d'oval sont brunâtres ou grisâtre non scorés et en relief 100 d'un côté.
Stalevo 125 comprimés enrobés de film contenant 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'entacapone. Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 125 d'un côté.
Stalevo 150 comprimés enrobés de film contenant 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'entacapone. Les comprimés en forme d'ellipse allongés sont le LCE 150 brunâtre ou rouge grisâtre ou en relief d'un côté.
Stalevo 200 comprimés enrobés de film contenant 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone. Les comprimés de forme ovale sont le rouge brunâtre foncé non scoré et le LCE 200 en relief d'un côté.
Stockage et manipulation
Stalevo (Carbidopa Levodopa et Entacapone) est fourni sous forme de comprimés enrobés de film pour l'administration orale dans les six forces suivantes:
Stalevo 50 film-coated tablets contenant 12,5 mg de carbidopa 50 mg de lévodopa et 200 mg d'entacapone.
Les comprimés ronds en forme de bi-convex sont le LCE 50 brunâtre ou grisâtre non scoré et en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-805-01
Stalevo 75 film-coated tablets contenant 18,75 mg de carbidopa 75 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 75 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-809-01
Stalevo 100 film-coated tablets contenant 25 mg de carbidopa 100 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont un lce 100 brunâtre ou grisâtre ou en relief de 100 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-816-01
Stalevo 125 film-coated tablets contenant 31,25 mg de carbidopa 125 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont rouges brunâtres légers et en relief avec le code LCE 125 d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-827-01
Stalevo 150 film-coated tablets contenant 37,5 mg de carbidopa 150 mg de lévodopa et 200 mg d'entacapone.
Les comprimés en forme d'ellipse allongés sont le LCE 150 brunâtre ou rouge grisâtre ou en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-834-01
Stalevo 200 film-coated tablets contenant 50 mg de carbidopa 200 mg de lévodopa et 200 mg d'entacapone.
Les comprimés de forme ovale sont le rouge brunâtre foncé non scoré et le LCE 200 en relief d'un côté.
Bouteille HDPE de 100 comprimés NDC 52427-842-01
Stocker à 25 ° C (77 ° F); Excursions autorisées à 15 ° C à 30 ° C (59 ° F à 86 ° F).
[Voir Température ambiante contrôlée par l'USP .]
Dispenser dans un récipient serré (USP).
Fabriqué par: Orion Corporation Orion Pharma Orionintie 1 FI-02200 ESPOO FINLAND. Distribué par: Almatica Pharma LLC Morristown NJ 07960 USA. Révisé: mai 2020
Effets secondaires for Stalevo
Les effets indésirables suivants sont discutés plus en détail dans les sections des avertissements et précautions d'étiquetage:
- S'endormir pendant les activités de la vie quotidienne et de la somnolence [voir Avertissements et précautions ]
- Hypotension / Hypotension orthostatique et syncope [voir Avertissements et précautions ]
- Dyskinésie [voir Avertissements et précautions ]
- Dépression et suicidalité [voir Avertissements et précautions ]
- Hallucinations / comportement psychotique [voir Avertissements et précautions ]
- Contrôle des impulsions et / ou comportements compulsifs [voir Avertissements et précautions ]
- Hyperpyrexie et confusion émergentes du retrait [voir Avertissements et précautions ]
- Diarrhée et colite [voir Avertissements et précautions ]
- Rhabdomyolyse [voir Avertissements et précautions ]
- Maladie de l'ulcère gastroduoque [voir Avertissements et précautions ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions très variables, l'incidence des effets indésirables (nombre de patients uniques subissant une réaction indésirable associée au traitement / nombre total de patients traités) observés dans les essais cliniques d'un médicament ne peut pas être directement comparé à l'incidence des réactions indésirables dans les essais cliniques d'un autre médicament et ne peut pas refléter l'incidence des réactions indésirables observées dans la pratique clinique.
Entacapone
Les réactions indésirables les plus couramment observées (incidence au moins 3% supérieure à l'incidence du placebo) dans les essais à double aveugle carbibidopa-levodopa-placebo sur l'entacapone (n = 1003 patients) associés à l'utilisation de carbidopalevodopa-entacapone seuls et non vus à une fréquence équivalente parmi les patients traités par placement: dyskinesia dia-naiseAia-traited les hyperkines. Douleur vomir la bouche sèche et la décoloration de l'urine.
L'incidence de la différence de traitement pour l'arrêt prématuré de l'étude pour l'entacapone avec l'inhibiteur de la lévodopa et de la dopa décarboxylase dans les essais contrôlés par placebo en double aveugle était de 5%. L'incidence de la différence de traitement pour les causes les plus fréquentes de l'arrêt de l'étude était de 2% pour la diarrhée et 1% pour d'autres effets indésirables spécifiques, y compris les raisons psychiatriques, la dyskinésie / hyperkinésie nausée ou les douleurs abdominales.
Incidence de réaction indésirable dans les études cliniques contrôlées de l'entacapone
Le tableau 2 énumère le traitement des effets indésirables émergents qui se sont produits chez au moins 1% des patients traités par carbidopa / lévodopa et 200 mg d'entacapone qui ont participé aux études contrôlées par placebo en double aveugle et qui étaient numériquement plus fréquentes dans ce groupe que dans le groupe carbidopa / levodopa plus placebo. Dans ces études, l'entacapone ou le placebo ont été ajoutés à la carbidopa / lévodopa (ou bensérazide / lévodopa).
Tableau 2: Résumé des patients ayant des effets indésirables après le début de l'essai Administration du médicament au moins 1% dans le groupe Entacapone et supérieur au placebo
| Réaction indésirable de la classe d'organes du système | Carbidopa / lévodopa plus entacapone (n = 603)% des patients | Carbidopa / lévodopa plus placebo (n = 400)% des patients |
| Troubles de la peau et des appendices | ||
| La transpiration a augmenté | 2 | 1 |
| Troubles du système musculo-squelettique | ||
| Maux de dos | 5 | 3 |
| Troubles du système nerveux central et périphérique | ||
| Dyskinésie | 25 | 15 |
| Hyperkinésie | 10 | 5 |
| Hypokinésie | 9 | 8 |
| Vertiges | 8 | 6 |
| Sens spéciaux d'autres troubles | ||
| Perversion de goût | 1 | 0 |
| Troubles psychiatriques | ||
| Anxiété | 2 | 1 |
| Somnolence | 2 | 0 |
| Agitation | 1 | 0 |
| Troubles du système gastro-intestinal | ||
| Nausée | 14 | 8 |
| Diarrhée | 10 | 4 |
| Douleurs abdominales | 8 | 4 |
| Constipation | 6 | 4 |
| Vomissement | 4 | 1 |
| Séchée à la bouche | 3 | 0 |
| Dyspepsie | 2 | 1 |
| Flatulence | 2 | 0 |
| Gastrite | 1 | 0 |
| Troubles gastro-intestinaux nos | 1 | 0 |
| Troubles du système respiratoire | ||
| Dyspnée | 3 | 1 |
| Saignement plaquettaire et coagulation Troubles | ||
| Purpura | 2 | 1 |
| Troubles du système urinaire | ||
| Décoloration de l'urine | 10 | 0 |
| Le corps comme troubles généraux | ||
| Fatigue | 6 | 4 |
| Asthénie | 2 | 1 |
| Troubles du mécanisme de résistance | ||
| Infection bactérienne | 1 | 0 |
Expérience de commercialisation de la poste
Les rapports spontanés suivants d'événements indésirables associés temporairement à Entacapone ou à Stalevo ont été identifiés depuis l'introduction du marché et ne sont pas répertoriés dans le tableau 2. Parce que ces réactions sont signalées volontairement d'une population de taille inconnue, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à Entacone ou à l'exposition de Stalevo.
Une hépatite avec des caractéristiques principalement cholestatiques a été signalée.
Effets du sexe et de l'âge sur les effets indésirables
Aucune différence n'a été notée dans la vitesse des effets indésirables attribuables à l'entacapone seul par âge ou sexe.
Interactions médicamenteuses for Stalevo
Inhibiteurs du MAO
Les patients recevant des inhibiteurs de MAO non sélectifs et de la carbidopa levodopa et l'entacapone peuvent être à risque d'une augmentation du ton adrénergique. Par conséquent, l'utilisation de Stalevo est contre-indiquée chez les patients recevant des inhibiteurs non sélectifs de MAO [voir Contre-indications ].
Médicaments métabolisés par catéchol-o-méthyltransférase (COMT)
Les médicaments connus pour être métabolisés par COMT tels que l'isoprotérenol épinéphrine noradrénaline dopamine dobutamine alpha-méthyldopa apomorphine isoétherine et le bitoltérol doivent être administrés avec la prudence chez les patients recevant l'entacapone, indépendamment de la voie d'administration (y compris l'inclusion) car leur interaction peut entraîner une augmentation des rythmes car [voir Avertissements et précautions ].
Agents antihypertenseurs
Symptomatique hypotension posturale s'est produit lorsque des carbidopa / lévodopa ont été ajoutés au traitement des patients recevant des médicaments antihypertenseurs. Lors du démarrage du traitement avec une dose de stalevo, un ajustement de médicament antihypertenseur peut être nécessaire.
Antidépresseurs tricycliques
Il y a eu des rapports d'effets indésirables, notamment l'hypertension et la dyskinésie résultant de l'utilisation concomitante du tricyclique antidépresseurs et Carbidopa / Levodopa.
Antagonistes des récepteurs de la dopamine D2
Les antagonistes des récepteurs de la dopamine D2 (par exemple les phénothiazines de métoclopramide butyrophénones rispéridone) peuvent réduire les effets thérapeutiques de la lévodopa.
Isoniazide
Isoniazide may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Lable
Les effets bénéfiques de la lévodopa dans la maladie de Parkinson auraient été inversés par la phénytoïne. Les patients prenant de la phénytoïne avec du carbidopa / levodopa doivent être soigneusement observés pour la perte de réponse thérapeutique. La dose de Stalevo doit être augmentée comme nécessaire cliniquement chez les patients recevant de la phénytoïne.
Papaverne
Les effets bénéfiques de la lévodopa dans la maladie de Parkinson auraient été inversés par la papavérine. Les patients prenant de la papavérine avec une carbidopa / lévodopa doivent être soigneusement observés pour la perte de réponse thérapeutique. La dose de Stalevo doit être augmentée comme nécessaire cliniquement chez les patients recevant de la papavérine.
Sels de fer
Les sels de fer ou multi-vitamines contenant des sels de fer doivent être co-administrés avec prudence. Les sels de fer peuvent former des chélates avec la lévodopa carbidopa et l'entacapone et, par conséquent, la biodisponibilité de Levodopa carbidopa et de l'entacapone.
Médicaments connus pour interférer avec la glucuronidation de l'excrétion biliaire et la bêta-glucuronidase intestinale
Comme la plupart de l'excrétion entacapone est via le même La prudence doit être exercée lorsque les médicaments connus pour interférer avec la glucuronidation de l'excrétion biliaire et la bêta-glucuronidase intestinale sont donnés simultanément avec l'entacapone. Il s'agit notamment de la cholestyramine probénide et de certains antibiotiques (par exemple, érythromycine rifampicine ampicilline et chloramphénicol).
Médicaments métabolisés via CYP2C9 (par ex. Coumadin)
La posologie de Stalevo doit être ajustée comme nécessaire cliniquement chez les patients utilisant d'autres médicaments métabolisés via le CYP2C9. Une étude d'interaction chez des volontaires sains entacapone a augmenté l'ASC de R-warfarine en moyenne de 18% et les valeurs INR en moyenne de 13%. Des cas d'INR accrus chez les patients en utilisant concomitante la warfarine ont été signalés lors de l'utilisation post-approbation de l'entacapone. Ainsi, la surveillance de l'INR est recommandée lorsque le traitement de Stalevo est initié pour les patients recevant de la warfarine.
Avertissements pour Stalevo
Inclus dans le cadre du PRÉCAUTIONS section.
Précautions pour Stalevo
Les effets indésirables suivants décrits dans cette section sont liés à au moins l'une des composantes de Stalevo (c'est-à-dire Levodopa carbidopa et / ou entacapone) sur la base de l'expérience de sécurité dans les essais cliniques (en particulier des essais pivots) ou dans les rapports post-commercialisation.
S'endormir pendant les activités de la vie quotidienne et de la somnolence
Les patients atteints de la maladie de Parkinson traités avec Stalevo ou d'autres produits Carbidopa / Levodopa ont été soudainement endormis sans avertissement préalable de somnolence tout en se livrant à des activités de vie quotidienne (y compris l'exploitation des véhicules à moteur). Certains de ces épisodes ont abouti à des accidents. Bien que bon nombre de ces patients aient signalé une somnolence lors de la prise de l'entacapone, certains n'ont pas perçu des signes avant-coureurs tels que la somnolence excessive et pensaient qu'ils étaient alertes immédiatement avant l'événement. Certains de ces événements auraient eu lieu jusqu'à un an après le début du traitement.
Somnolence was reported in 2% of patients taking entacapone et 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for somnolence or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge somnolence or sleepiness until directly questioned about somnolence or sleepiness during specific activities. Patients who have already experienced somnolence et/or an episode of sudden sleep onset should not participate in these activities during treatment with Stalevo.
Avant de lancer un traitement avec Stalevo, conseille aux patients du potentiel de développer la somnolence et de poser des questions spécifiquement sur les facteurs qui peuvent augmenter ce risque tels que l'utilisation de médicaments sédatifs concomitants et la présence de troubles du sommeil. Si un patient développe une somnolence diurne ou des épisodes de s'endormir pendant les activités qui nécessitent une participation active (par exemple, les conversations alimentaires, etc.) Stalevo devrait généralement être interrompu [voir Posologie et administration et Avertissements et précautions ]. If the decision is made to continue Stalevo patients should be advised not to drive et to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Hypotension Orthostatic Hypotension And Syncope
Les rapports de syncope étaient généralement plus fréquents chez les patients des deux groupes de traitement qui avaient eu un épisode antérieur d'hypotension documentée (bien que les épisodes de syncope obtenus par l'histoire n'étaient pas eux-mêmes documentés avec une mesure vitale des signes). Hypotension L'hypotension et la syncope orthostatiques sont observées chez les patients traités avec des médicaments qui augmentent le ton dopaminergique central, y compris le stalevo.
Dyskinésie
Dyskinésie (involontaire movements) may occur or be exacerbated at lower dosages et sooner with Stalevo than with preparations containing only carbidopa et levodopa. The occurrence of dyskinesias may require dosage reduction.
Dans les essais pivots, l'incidence de la différence de traitement de la dyskinésie était de 10% et pour la carbidopa-levodopa plus 200 mg d'entacapone. Bien que la diminution de la dose de lévodopa puisse améliorer cet effet secondaire, de nombreux patients dans des essais contrôlés ont continué à ressentir des dyskinésies fréquentes malgré une réduction de leur dose de lévodopa. L'incidence de la différence de traitement du retrait de l'étude pour la dyskinésie était de 1% pour la carbidopa-levodopa-entacapone.
Dépression et suicidalité
Tous les patients doivent être observés avec soin pour le développement de la dépression avec des tendances suicidaires concomitantes. Les patients atteints de psychoses passées ou actuels doivent être traités avec prudence.
Hallucinations et / ou comportement psychotique
Le traitement dopaminergique chez les patients atteints de la maladie de Parkinson a été associé à des hallucinations. Les hallucinations ont conduit à l'arrêt des médicaments et au retrait prématuré des essais cliniques chez 0,8% et 0% des patients traités avec Carbidopa levodopa entacapone et Carbidopa levodopa respectivement. Les hallucinations ont conduit à l'hospitalisation chez 1,0% et 0,3% des patients des groupes Carbidopa Levodopa Entacapone et Carbidopa Levodopa respectivement. L'agitation s'est produite chez 1% des patients traités par Carbidopa levodopa entacapone et 0% traités par Carbidopa levodopa.
Contrôle des impulsions et / ou comportements compulsifs
Les rapports de commercialisation suggèrent que les patients traités par des médicaments anti-parkinson peuvent ressentir des envies intenses à jouer des envies sexuelles accrues à dépenser de l'argent incontrôlable et d'autres envies intenses. Les patients peuvent être incapables de contrôler ces envies tout en prenant un ou plusieurs des médicaments généralement utilisés pour le traitement de la maladie de Parkinson et qui augmentent le ton dopaminergique central, y compris l'entacapone prise avec la lévodopa et la carbidopa. Dans certains cas, bien que toutes ces envies n'étaient pas censées s'être arrêtées lorsque la dose de médicaments anti-parkinson a été réduite ou interrompue. Étant donné que les patients peuvent ne pas reconnaître ces comportements comme anormaux, il est important pour les prescripteurs de demander spécifiquement aux patients ou à leurs soignants sur le développement d'une augmentation des envies de jeu, les envies sexuelles dépensent des dépenses non contrôlées ou d'autres pulsions tout en étant traitées avec Entacapone. Les médecins devraient envisager la réduction de la dose ou l'arrêt de Stalevo si un patient développe de telles envies tout en prenant Stalevo [voir Posologie et administration Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Des cas d'hyperpyrexie et de confusion ressemblant au syndrome malin neuroleptique (NMS) ont été signalés en association avec la réduction de la dose ou le retrait du traitement avec la carbidopa levodopa et l'entacapone. Cependant, dans certains cas, l'hyperpyrexie et la confusion ont été signalées après le début du traitement par entacapone. L'hyperpyrexie et la confusion sont rares, mais elles peuvent être mortelles avec une variété de caractéristiques, notamment l'hyperpyrexie / la fièvre / l'hyperthermie rigidité musculaire Mouvements involontaires altérés conscience / l'état mental changent de la dysfonction autonome de la tachycardie Tachypnea Terming Hyper ou l'hypotension du laboratoire annoral (e.g.g. Créine Phosphinase Labation du lesicodase de la créatine (e.g.gosphokinase-likocinas licedosise le labotage annoral. myoglobinurie et augmentation de la myoglobine sérique).
Si un patient doit interrompre ou réduire sa dose quotidienne de Stalevo, la dose doit être diminuée lentement avec la supervision d'un fournisseur de soins de santé [voir Posologie et administration ]. Specific methods for tapering entacapone have not been systematically evaluated.
Diarrhée And Colitis
Dans les essais cliniques de diarrhée d'entacapone développés chez 60 sur 603 (NULL,0%) et 16 sur 400 (NULL,0%) des patients traités avec 200 mg d'entacapone ou de placebo en combinaison avec le lévodopa et l'inhibiteur de DOPA décarboxylase respectivement. Chez les patients traités par entacapone, la diarrhée était généralement légère à modérée en gravité (NULL,6%) mais était considérée comme sévère dans 1,3%. La diarrhée a entraîné un retrait chez 10 des 603 (NULL,7%) patients 7 (NULL,2%) avec une diarrhée légère et modérée et 3 (NULL,5%) avec une diarrhée sévère. La diarrhée a généralement résolu après l'arrêt de l'entacapone. Deux patients atteints de diarrhée ont été hospitalisés. Généralement, la diarrhée se présente dans les 4 à 12 semaines après le début de l'entacapone, mais elle peut apparaître dès la première semaine et aussi tard autant de mois après le début du traitement. La diarrhée peut être associée à une déshydratation de perte de poids et à une hypokaliémie.
L'expérience de la post-commercialisation a montré que la diarrhée peut être un signe de colite microscopique induite par le médicament principalement la colite lymphocytaire. Dans ces cas, la diarrhée a généralement été modérée à sévère aqueuse et sans folie parfois associée à la déshydratation de la perte de poids de douleur abdominale et à une hypokaliémie. Dans la majorité des cas, la diarrhée et d'autres symptômes liés à la colite ont résolu ou significativement amélioré lorsque le traitement à l'entacapone a été arrêté. Chez certains patients atteints de biopsie, la diarrhée a confirmé que la diarrhée s'était résolue ou significativement améliorée après l'arrêt de l'entacapone mais a été recourbé après le retraitement avec Entacapone.
Si une diarrhée prolongée est soupçonnée d'être liée à Stalevo, le médicament doit être interrompu et un traitement médical approprié considéré. Si la cause de la diarrhée prolongée reste claire ou se poursuit après l'arrêt de l'entacapone, des enquêtes diagnostiques supplémentaires, y compris la coloscopie et les biopsies, doivent être prises en compte.
Rhabdomyolyse
Des cas de rhabdomyolyse sévère ont été signalés avec Entacapone lorsqu'ils sont utilisés en combinaison avec la carbidopa et la lévodopa. Une activité motrice sévère prolongée, y compris la dyskinésie, peut éventuellement expliquer la rhabdomyolyse. La plupart des cas se sont manifestés par la myalgie et les valeurs accrues de la créatine phosphokinase (CPK) et de la myoglobine. Certaines réactions comprenaient également de la fièvre et / ou une altération de la conscience. Il est également possible que la rhabdomyolyse puisse être le résultat du syndrome décrit dans l'hyperpyrexie et la confusion émergentes du sevrage [voir [voir Avertissements et précautions ].
Interaction avec les médicaments métabolisés par comt
Les médicaments connus pour être métabolisés par le COMT tels que l'isoprotérénol épinéphrine norréphrine dopamine dopamine dobutamine alpha-méthyldopa apomorphine isoétherine et le bitoltérol doivent être administrés avec la prudence chez les patients qui réceptent l'entacapone, indépendamment de la voie d'administration (y compris une augmentation de la pression de l'homme) car leur interaction peut entraîner une augmentation du rythme car
Complications fibrotiques
Des cas d'infiltrats pulmonaires de la fibrose rétropéritonéale ont été signalés chez certains patients traités par des agents dopaminergiques dérivés d'ergot. Ces complications peuvent se résoudre lorsque le médicament est interrompu, mais une résolution complète ne se produit pas toujours. Bien que ces effets indésirables puissent être liés à la structure de l'ergoline de ces composés, un rôle causal possible des médicaments dérivés non ERGOT (par exemple l'entacapone levodopa) qui augmentent l'activité dopaminergique a également été pris en compte. L'incidence attendue de complications fibrotiques est si faible que même si l'entacapone provoquait ces complications à des taux similaires à ceux attribuables à d'autres thérapies dopaminergiques, il est peu probable qu'elle ait été détectée dans une cohorte de la taille exposée à l'entacapone pendant son développement clinique. Quatre cas de fibrose pulmonaire ont été signalés lors du développement clinique de l'entacapone; 3 de ces patients ont également été traités avec du pergolide et 1 avec de la bromocriptine. La durée du traitement avec Entacapone variait de 7 mois à 17 mois.
Maladie de l'ulcère gadin
Comme pour le traitement de la lévodopa avec Stalevo, peut augmenter la possibilité d'hémorragie gastro-intestinale supérieure chez les patients ayant des antécédents d'ulcère gastro-duodénal.
Trouble hépatique
Les patients souffrant de troubles hépatiques doivent être traités avec prudence [voir Pharmacologie clinique ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Tests de laboratoire
Des anomalies dans les tests de laboratoire peuvent inclure des élévations de tests de fonction hépatique tels que la phosphatase alcaline SGOT (AST) SGPT (ALT) déshydrogénase et bilirubine. Anomalies dans le sang urée Un test d'azote et de coombes positifs a également été signalé. Les niveaux couramment des niveaux d'azote de l'urée sanguine et de l'acide urique sont plus faibles pendant l'administration de Stalevo qu'avec levodopa.
Stalevo may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
La prudence doit être exercée lors de l'interprétation des taux plasmatiques et d'urine de catécholamines et de leurs métabolites chez les patients sous traitement carbidopa / lévodopa.
Informations de conseil des patients S'endormir pendant les activités de la vie quotidienne et de la somnolence
Conseillez les patients sur le potentiel d'effets sédatifs associés à Stalevo, y compris la somnolence et sur la possibilité de s'endormir tout en se livrant à des activités de vie quotidienne. Parce que la somnolence peut être une réaction indésirable fréquente avec des conséquences potentiellement graves, les patients ne devraient pas conduire un véhicule à moteur à faire fonctionner des machines lourdes ou s'engager dans d'autres activités potentiellement dangereuses jusqu'à ce qu'elles aient acquis une expérience suffisante avec STALEVO pour déterminer si cela affecte ou non leurs performances mentales et / ou motrices [voir adversation [voir Avertissements et précautions ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Conseiller aux patients de parler avec leur prescripteur de soins de santé avant de prendre des médicaments en séduisant ou d'autres dépresseurs du SNC (par exemple les antidépresseurs antipsychotiques benzodiazépines, etc.) en raison des effets additifs possibles en combinaison avec Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Informer les patients qu'ils peuvent développer une hypotension symptomatique (ou asymptomatique) posturale (orthostatique) ou une hypotension non orthostatique lors de la prise de Stalevo. L'hypotension / hypotension orthostatique peut se produire plus fréquemment pendant le traitement initial. Les patients ne devraient pas augmenter rapidement après s'asseoir ou se coucher, surtout s'ils l'ont fait pendant des périodes prolongées et surtout lors de l'initiation du traitement avec Stalevo.
Conseillez les patients sur le potentiel de syncope chez les patients utilisant des agonistes de dopamine. Pour cette raison, informer les patients de la possibilité de syncope tout en prenant Stalevo [voir Avertissements et précautions ].
Dyskinésies
Informer les patients que Stalevo peut provoquer et / ou exacerber les dyskinésies préexistantes [voir Avertissements et précautions ].
Hallucinations et / ou comportement psychotique
Informer les patients que les hallucinations et autres comportements de type psychotique peuvent se produire lors de la prise de Stalevo [voir Avertissements et précautions ].
Contrôle des impulsions et / ou comportements compulsifs
Informer les patients qu'ils peuvent ressentir des comportements de contrôle des impulsions et / ou compulsifs tout en prenant un ou plusieurs médicaments utilisés pour le traitement de la maladie de Parkinson, y compris Stalevo. Demandez aux patients sur le développement des envies de jeu nouvelles ou accrues les envies sexuelles les envies de dépenses incontrôlées ou d'autres envies intenses tout en étant traitées avec Stalevo. Conseiller aux patients d'informer leur médecin ou leur fournisseur de soins de santé s'ils connaissent des envies de jeu nouvelles ou accrues accrues les envies sexuelles ou d'autres envies intenses tout en prenant Stalevo. Les médecins devraient envisager la réduction de la dose ou l'arrêt du médicament si un patient développe de telles envies tout en prenant Stalevo [voir Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Informer les patients qu'ils peuvent développer de la fièvre et de la confusion dans le cadre d'un syndrome ressemblant à la NMS et éventuellement avec d'autres caractéristiques cliniques (par exemple, la rigidité musculaire dysfonctionnement hyper ou hypotension, etc.). Ce syndrome de fièvre et de confusion peut se produire particulièrement avec des réductions de dose ou un retrait de Stalevo mais peut également se développer après le début du traitement. Conseiller aux patients de contacter leur fournisseur de soins de santé s'ils souhaitent interrompre ou diminuer la dose de Stalevo et contacter un fournisseur de soins de santé s'ils développent de la fièvre et de la confusion [voir Avertissements et précautions ].
Diarrhée And Colitis
Informez les patients que la diarrhée peut se produire avec Stalevo et qu'il peut avoir un début retardé. Parfois, la diarrhée prolongée peut être causée par la colite (inflammation du gros intestin). Les patients atteints de diarrhée doivent boire des liquides pour maintenir une hydratation adéquate et surveiller la perte de poids. Si la diarrhée associée à STALEVO est prolongée, ce qui devrait entraîner la résolution. Si la diarrhée se poursuit après avoir arrêté des enquêtes de diagnostic à Stalevo peut être nécessaire. Dans certains cas, la diarrhée peut être associée à la colite [voir Avertissements et précautions ].
Rhabdomyolyse
Informer les patients qu'ils peuvent développer une rhabdomyolyse et une myalgie s'ils éprouvent une activité motrice prolongée, y compris la dyskinésie. Cet événement peut également être associé à la fièvre et à la confusion [voir Avertissements et précautions ].
Nausée And Vomissement
Informer les patients que Stalevo peut provoquer des nausées et des vomissements peuvent survenir plus fréquemment pendant le traitement initial et peuvent nécessiter un ajustement de la dose.
Instructions pour une utilisation
Demandez aux patients de prendre Stalevo uniquement comme prescrit. Demandez aux patients de ne prendre qu'un seul comprimé de Stalevo à chaque intervalle de dosage. Demandez aux patients de ne pas prendre plusieurs comprimés ou des portions supplémentaires de comprimés pour obtenir une dose plus élevée de lévodopa. Conseiller aux patients de ne pas séparer l'écrasement ou de mâcher Stalevo.
Informez le patient que Stalevo est une formulation de carbidopa / lévodopa combinée à l'entacapone conçu pour commencer la libération d'ingrédients dans les 30 minutes suivant l'ingestion. Il est important que Stalevo soit pris à intervalles réguliers selon le calendrier décrit par le médecin. ATTENTION Le patient de ne pas modifier le schéma posologique prescrit et de ne pas ajouter de médicaments antiparkinsoniens supplémentaires, y compris d'autres préparations carbidopa / lévodopa sans consulter d'abord le médecin.
Conseillez les patients que les épisodes interdits (le port de l'effet du médicament) se produisent à la fin de l'intervalle de dosage, mais des épisodes hors de terre imprévisibles peuvent se produire à tout moment. Conseillez au patient d'informer un fournisseur de soins de santé pour d'éventuels ajustements de traitement si une telle réponse pose un problème à la vie quotidienne du patient.
Conseillez les patients que la coloration foncée (brun rouge ou noir) peut apparaître dans l'urine ou la sueur de la salive après avoir pris Stalevo. Bien que la couleur semble être cliniquement insignifiante que les vêtements peuvent être décolorés.
Conseiller les patients qu'un changement de régime alimentaire en aliments riches en protéines peut retarder l'absorption de la lévodopa. Une acidité excessive retarde également la vidange de l'estomac, retardant ainsi l'absorption de la lévodopa. Les sels de fer (comme dans les comprimés multi-vitamines) peuvent également réduire l'efficacité de Stalevo.
Grossesse
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant la thérapie [voir Utiliser dans des populations spécifiques ].
Lactation
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils ont l'intention d'allaiter ou d'allaiter un nourrisson [voir Utiliser dans des populations spécifiques ].
Toxicologie non clinique Carcinogenèse Mutagenèse A trouble de la fertilité Cancérogenèse
Cancérogenèse
Chez le rat, l'administration orale de carbidopa-levodopa pendant 2 ans n'a entraîné aucune preuve de cancérogénicité à des doses d'environ 2 fois (carbidopa) -4 fois (levodopa), la dose humaine maximale recommandée (MRHD).
Des études de cancérogénicité de deux ans de l'entacapone ont été menées chez des souris et des rats. Chez la souris, aucune augmentation des tumeurs n'a été observée à des doses orales de 100 200 et 400 mg / kg / jour. À la dose la plus élevée, les expositions au plasma (ASC) étaient 4 fois plus élevées que celles chez l'homme à la dose quotidienne maximale recommandée (MRDD) de 1600 mg. Chez le rat, des doses orales administrées de 20 90 ou 400 mg / kg / jour, une incidence accrue d'adénomes et de carcinomes tubulaires rénaux a été observée chez les hommes à la dose la plus élevée testée. Les AUC plasmatiques à la dose plus élevée non associée à une augmentation des tumeurs rénales (90 mg / kg / jour) étaient environ 5 fois chez l'homme au MRDD d'Entacapone.
Le potentiel cancérigène de l'entacapone administré en combinaison avec la carbidopa-levodopa n'a pas été évalué.
Mutagenèse
La carbidopa était mutagène dans le test de mutation inverse bactérienne in vitro (AME) en présence et en absence d'activation métabolique et dans le test de lymphome de souris in vitro (TK) en l'absence d'activation métabolique. La carbidopa était négative dans le test de micronucléus de souris in vivo.
Entacapone was mutagenic et clastogenic in the in vitro mouse lymphoma tk assay in the presence et absence of metabolic activation et was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapone either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus et in the Ames assays.
Altération de la fertilité
Dans les études de reproduction, aucun effet sur la fertilité n'a été trouvé chez le rat recevant la carbidopa-levodopa à des doses d'environ 2 fois (carbidopa) -4 fois (lévodopa) le MRHD.
Chez le rat traité par voie orale avec de l'entacapone (jusqu'à 700 mg / kg / jour), aucun effet sur la fertilité ou les performances de reproduction générale n'a été observée. Les expositions au plasma (ASC) à la dose la plus élevée testée étaient environ 30 fois chez l'homme au MRHD d'Entacapone. L'accouplement retardé était évident chez les femmes à la dose la plus élevée testée.
Utiliser dans des populations spécifiques Grossesse Résumé des risques
Résumé des risques
Il n'y a pas de données adéquates sur le risque de développement associé à l'utilisation de Stalevo chez les femmes enceintes. Chez les animaux, l'administration de carbidopa-levodopa ou d'entacapone pendant la grossesse était associée à une toxicité du développement, notamment des incidents accrus de malformations fœtales (voir Données ). Le risque de fond estimé de malformations congénitales et de fausse couche dans la population indiquée est inconnue. Dans la population générale américaine, les risques de fond estimés des principaux malformations congénitales et une fausse couche dans les grossesses cliniquement reconnues sont respectivement de 2 à 4% et 15 à 20%.
Données
Données sur les animaux
Dans les études non cliniques dans lesquelles une carbidopa-levodopa a été administrée à des animaux enceintes, des incidents accrus de malformations viscéraux et squelettiques ont été observés chez les lapins à toutes les doses et les rapports de carbidopa-levodopa testés qui variaient de 10 fois (carbidopa) -5 fois (levodopa) à 20 fois (carbidopa) - 10 fois de 1600 mg / jour. Chez le rat, il y a eu une diminution du nombre de chiots vivants délivrés par les barrages recevant environ deux fois (carbidopa) -five Times (Levodopa) le MRHD tout au long de l'organogenèse. Aucun effet sur les fréquences de malformation n'a été observé chez les souris recevant jusqu'à 20 fois le MRHD de Carbidopa-Levodopa.
Dans le développement des embryons-foetal, des études sur les animaux enceintes de l'entacapone ont reçu des doses allant jusqu'à 1000 mg / kg / jour (rats) ou 300 mg / kg / jour (lapins) tout au long de l'organogenèse. Une incidence accrue de variations fœtales était évidente dans les portées des rats traités avec la dose la plus élevée en l'absence de signes manifestes de toxicité maternelle. L'exposition à l'entacapone plasmatique maternelle (ASC) associée à cette dose était d'environ 34 fois celle chez l'homme au MRHD. Des fréquences accrues d'avortements et de résorption tardive / totale et une diminution des poids fœtaux ont été observés dans les portées de lapins traités avec des doses toxiques maternellement toxiques de 100 mg / kg / jour (AUC plasma inférieur à celle chez l'homme au MRHD) ou plus. Il n'y a eu aucune augmentation des taux de malformation dans ces études.
Lorsque l'entacapone a été administré à des rats femelles avant l'accouplement et pendant la gestation précoce, une incidence accrue d'anomalies oculaires fœtales (Macrophthalmia Microphthalmia anophtalmia) a été observée dans les portées des barrages traités avec des doses de 160 mg / kg / jour (plasma Aucs sept fois dans l'humain à la MRHD) ou plus dans l'absence de l'absence maternelle. Administration jusqu'à 700 mg / kg / jour (AUC plasma 28 fois chez l'homme au MRHD) aux rats pendant la dernière partie de la gestation et tout au long de la lactation n'a produit aucune preuve de déficience du développement chez la progéniture.
Lactation Résumé des risques
La lévodopa a été détectée dans le lait maternel après l'administration de Carbidopa-Levodopa. Il n'y a pas de données sur la présence d'entacapone ou de carbidopa dans le lait maternel les effets de la lévodopa carbidopa ou de l'entacapone sur le nourrisson allaité ou des effets sur la production de lait. Cependant, l'inhibition de la lactation peut se produire car la lévodopa diminue la sécrétion de prolactine [voir Pharmacologie clinique ]. Carbidopa et entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone et/or metabolites in milk up to 2 to 3 times that in plasma. The developmental et health benefits of breastfeeding should be considered along with the mother's clinical need for Stalevo et any potential adverse effects on the breastfed infant from Stalevo or from the underlying maternal condition.
Usage pédiatrique
La sécurité et l'efficacité des patients pédiatriques n'ont pas été établies.
Utilisation gériatrique
Sur le nombre total de sujets dans les études cliniques de Stalevo, 43,8% étaient âgés de 65 ans et plus, tandis que 7,2% avaient 75 ans et plus. Aucune différence globale de sécurité ou d'efficacité n'a été observée entre ces sujets et les sujets plus jeunes et d'autres expériences cliniques signalées n'ont pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes; Cependant, une plus grande sensibilité de certaines personnes âgées ne peut pas être exclue.
Stalevo tablets have not been studied in Maladie de Parkinson patients or in healthy volunteers older than 75 years [see Pharmacologie clinique ].
Trouble rénal
La déficience rénale n'affecte pas la pharmacocinétique de l'entacapone. Il n'y a pas d'études sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles rénaux [voir Pharmacologie clinique ].
Trouble hépatique Or Biliary Obstruction
Il n'y a pas d'études sur la pharmacocinétique de la carbidopa et de la lévodopa chez les patients souffrant de troubles hépatiques. Stalevo devrait être administré avec prudence aux patients présentant une obstruction biliaire ou une maladie hépatique, car l'excrétion biliaire semble être la principale voie d'excrétion de l'entacapone et de la déficience hépatique a eu un effet significatif sur la pharmacocinétique de l'entacapone lorsque 200 mg d'entacapone ont été administrés seuls [voir Pharmacologie clinique ].
Informations sur la surdose pour Stalevo
Signes et symptômes de surdosage
Il y a très peu de cas de surdose avec la lévodopa signalés dans la littérature publiée. Sur la base des informations disponibles, les symptômes aigus de la surdose de l'inhibiteur de la lévodopa et de la dopa décarboxylase devraient résulter d'une surstimulation dopaminergique. Les doses de quelques grammes peuvent entraîner des perturbations du SNC avec une probabilité croissante de perturbation cardiovasculaire (par exemple, une tachycardie d'hypotension) et des problèmes psychiatriques plus graves à des doses plus élevées. Un rapport isolé de la rhabdomyolyse et une autre d'insuffisance rénale transitoire suggèrent que la surdose de la lévodopa peut donner lieu à des complications systémiques secondaires à une surstimulation dopaminergique.
L'inhibition du COMT par le traitement à l'entacapone dépend de la dose. Une surdose massive d'entacapone peut théoriquement produire une inhibition à 100% de l'enzyme COMT chez les personnes empêchant ainsi l'O-méthylation de catéchols endogènes et exogènes.
Dans les essais cliniques, la dose unique d'entacapone la plus élevée administrée à l'homme était de 800 mg, ce qui a entraîné une concentration plasmatique de 14,1 mcg par ml. La dose quotidienne la plus élevée donnée aux humains était de 2400 mg administrée dans une étude à 400 mg six fois par jour avec une carbidopa / lévodopa pendant 14 jours chez 15 patients atteints de la maladie de Parkinson et dans une autre étude comme 800 mg trois fois par jour pendant 7 jours chez 8 volontaires sains. À cette dose quotidienne, les concentrations plasmatiques maximales d'Entacapone ont été en moyenne de 2,0 mcg par ml (à 45 min contre 1,0 mcg par ml et 1,2 mcg par ml avec 200 mg d'entacapone à 45 min.). Les douleurs abdominales et les selles lâches ont été les événements indésirables les plus couramment observés au cours de cette étude. Des doses quotidiennes pouvant atteindre 2000 mg d'entacapone ont été administrées comme 200 mg 10 fois par jour avec des carbidopa / lévodopa ou du bensérazide / lévodopa pendant au moins 1 an chez 10 patients pendant au moins 2 ans chez 8 patients et pendant au moins 3 ans chez 7 patients. Dans l'ensemble, cependant, l'expérience clinique avec des doses quotidiennes supérieures à 1600 mg est limitée.
Gestion de la surdosage
L'hospitalisation est conseillée et des mesures générales de soutien doivent être utilisées ainsi qu'un lavage gastrique immédiat et des doses répétées de charbon de bois au fil du temps. Cela peut accélérer l'élimination de l'entacapone en particulier en diminuant son absorption et sa réabsorption du tractus gastro-intestinal. Les liquides intraveineux doivent être administrés judicieusement et une voie aérienne adéquate.
La fonction circulatoire et rénale respiratoire doit être surveillée et les mesures de soutien appropriées utilisées. La surveillance électrocardiographique doit être instituée et le patient a soigneusement observé pour le développement d'arythmies; Si nécessaire, un traitement antiarythmique approprié doit être donné. La possibilité que le patient ait pris d'autres médicaments augmentant le risque d'interactions médicamenteuses (en particulier les médicaments structurés au catéchol) devrait être pris en considération. À ce jour, aucune expérience n'a été signalée avec dialyse; Par conséquent, sa valeur de surdosage n'est pas connue. Il est peu probable que l'hémodialyse ou l'héperfusion réduise les niveaux d'entacapone en raison de sa liaison élevée aux protéines plasmatiques. La pyridoxine n'est pas efficace pour inverser les actions de Stalevo.
Contre-indications pour Stalevo
Stalevo is contraindicated in patients:
- Prendre des inhibiteurs non sélectifs de la monoamine oxydase (MAO) (par exemple la phénelzine et la tranylcypromine). Ces inhibiteurs non sélectifs du MAO doivent être interrompus au moins deux semaines avant le début du traitement avec Stalevo.
- Avec un angle étroit glaucome .
Pharmacologie clinique for Stalevo
Mécanisme d'action Levodopa
Les preuves actuelles indiquent que les symptômes de la maladie de Parkinson sont liés à l'épuisement de la dopamine dans le corpus striatum. L'administration de dopamine est inefficace dans le traitement de la maladie de Parkinson car elle ne traverse pas la barrière hémato-encéphalique. Cependant, la lévodopa Le précurseur métabolique de la dopamine traverse la barrière hémato-encéphalique et est vraisemblablement converti en dopamine dans le cerveau. On pense que c'est le mécanisme par lequel Levodopa soulage les symptômes de la maladie de Parkinson.
Carbidopa
Lorsque la lévodopa est administrée par voie orale, elle est rapidement décarboxylée à la dopamine dans les tissus extracerébraux afin que seule une petite partie d'une dose donnée soit transportée inchangée vers le système nerveux central. La carbidopa inhibe la décarboxylation de la lévodopa périphérique rendant plus de lévodopa disponible pour l'accouchement au cerveau.
Entacapone
Entacapone is a selective et reversible inhibitor of catechol-O-methyltransferase (COMT).
COMT catalyse le transfert du groupe méthyle de S-adénosyl-l-méthionine vers le groupe phénolique de substrats qui contiennent une structure de catéchol. Les substrats physiologiques du COMT comprennent les dopa catécholamines (dopamine norcéréphrine et épinéphrine) et leurs métabolites hydroxylés. Lorsque la décarboxylation de la lévodopa est empêchée par la carbidopa comt devient l'enzyme métabolisante principale pour la lévodopa catalysant son métabolisme en 3-méthoxy-4-hydroxy-l-phénylalanine (3-OMD).
Pharmacocinétique
La pharmacocinétique des comprimés Stalevo a été étudiée chez des sujets sains (45 ans à 75 ans). Dans l'ensemble, la suite de l'administration de doses correspondantes de Levodopa carbidopa et de l'entacapone comme Stalevo ou en tant que produit carbidopa et lévodopa plus comprimés comtan (entacapone) Les concentrations plasmatiques moyennes de Levodopa carbidopa et de l'entacapone sont comparables.
Absorption et distribution
Levodopa et l'entacapone sont rapidement absorbés et éliminés et leur volume de distribution est modérément petit. La carbidopa est absorbée et éliminée légèrement plus lentement par rapport à la lévodopa et à l'entacapone. Il existe des variations inter et intra-individuelles substantielles dans l'absorption de Levodopa carbidopa et de l'entacapone en particulier concernant son CMAX.
L'effet alimentaire sur le comprimé Stalevo n'a pas été évalué. Parce que la lévodopa rivalise avec certains acides aminés pour le transport à travers la paroi intestinale, l'absorption de la lévodopa peut être altérée chez certains patients après avoir mangé un repas riche en protéines. Les repas riches en grands acides aminés neutres peuvent retarder et réduire l'absorption de la lévodopa [voir Informations de conseil des patients ].
Levodopa
Les propriétés pharmacocinétiques de la lévodopa après l'administration de comprimés de stalevo à dose unique (Carbidopa levodopa et entacapone) sont résumées dans le tableau 3.
Tableau 3: Caractéristiques pharmacocinétiques de la lévodopa avec différentes forces de comprimés de Stalevo (moyenne ± ET)
| Résistance à la tablette | AUC0 -∞ (nanogramme • H via ML) | CMAX (nanogramme par ml) | Tmax (h) |
| 12,5 mg par 50 mg par 200 mg | 1040 ± 314 | 470 ± 154 | 1,1 ± 0,5 |
| 25 mg par 100 mg par 200 mg | 2910 ± 715 | 975 ± 247 | 1,4 ± 0,6 |
| 37,5 mg par 150 mg par 200 mg | 3770 ± 1120 | 1270 ± 329 | 1,5 ± 0,9 |
| 50 mg par 200 mg par 200 mg | 6115 ± 1536 | 1859 ± 455 | 1,76 ± 0,7 |
Levodopa is bound to plasma protein only to a minor extent (about 10% to 30%).
Carbidopa
Après l'administration de Stalevo en tant que dose unique pour des sujets mâles et féminins en bonne santé, la concentration maximale de carbidopa a été atteinte dans les 2,5 heures à 3,4 heures en moyenne. Le CMAX moyen variait d'environ 40 nanogrammes par ml à 225 nanogrammes par ml et l'ASC moyen de 170 nanogrammes • H par ml à 1200 nanogrammes • H par ml avec différentes résistances stalevo fournissant 12,5 mg 25 mg 37,5 mg ou 50 mg de carbidopa.
Carbidopa is approximately 36% bound to plasma protein.
Entacapone
Après l'administration de Stalevo en tant que dose unique pour des sujets mâles et féminins en bonne santé, la concentration maximale d'entacapone dans le plasma a été atteinte dans une heure à 1,2 heure en moyenne. Le CMAX moyen de l'entacapone était d'environ 1200 nanogrammes par ml à 1500 nanogrammes par ml et le nanogramme AUC 1250 • H par ml à 1750 nanagram • H par ml après l'administration de différentes résistances Stalevo fournissant tous 200 mg d'Entacapone.
La liaison à la protéine plasmatique de l'entacapone est de 98% sur la plage de concentration de 0,4 mcg par ml à 50 mcg par ml. Entacapone se lie principalement à l'albumine sérique.
Métabolisme et élimination
Levodopa
La demi-vie d'élimination de la lévodopa La fraction active de l'activité antiparkinsonienne était de 1,7 heures (intervalle de 1,1 heures à 3,2 heures).
Levodopa is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) et O-methylation by COMT.
Carbidopa
La demi-vie d'élimination de la carbidopa était en moyenne de 1,6 heures à 2 heures (intervalle de 0,7 à 4,0 heures).
Carbidopa is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid et α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapone
La demi-vie d'élimination de l'entacapone était en moyenne de 0,8 heure à 1 heure (NULL,3 heure à 4,5 heures).
Entacapone is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapone et the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent et 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 La dose marquée en C d'Entacapone 10% des parents et métabolites marqués est excrété dans l'urine et 90% dans les excréments.
En raison de la courte élimination, aucune véritable accumulation de lévodopa ou d'entacapone ne se produit lorsqu'elles sont administrées à plusieurs reprises.
Trouble rénal
Entacapone
La pharmacocinétique de l'entacapone a été étudiée après une seule dose d'entacapone de 200 mg chez des sujets avec des fonctions rénales normales modérées et gravement altérées sans la lévodopa et la coadmination de l'inhibiteur de la DOPA décarboxylase. Aucun effet significatif de la fonction rénale sur la pharmacocinétique de l'entacapone n'a été trouvé.
Levodopa And carbidopa
Aucune étude sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles rénaux.
Trouble hépatique
Entacapone
Les troubles hépatiques ont eu un effet significatif sur la pharmacocinétique de l'entacapone lorsque 200 mg d'entacapone ont été administrés seuls. Une seule dose de 200 mg d'entacapone sans levodopa et la co-administration de l'inhibiteur de la DOPA décarboxylase a montré des valeurs AUC et CMAX d'environ 2 fois plus élevées chez les patients ayant des antécédents d'alcoolisme et de déficience hépatique (n = 10) par rapport aux sujets normaux (n = 10). Tous les patients avaient une cirrhose hépatique prouvée par la biopsie causée par l'alcool. Selon Child-Pugh, 7 patients atteints d'une maladie du foie ont eu une déficience hépatique légère et 3 patients avaient une déficience hépatique modérée. Comme seulement environ 10% de la dose d'entacapone est excrété dans l'urine en tant que composé parent et excrétion biliaire du glucuronide conjugué semble être la principale voie d'excrétion de ce médicament. Stalevo doit être administré avec soin aux patients présentant une obstruction biliaire ou une maladie hépatique.
Levodopa And Carbidopa
Il n'y a pas d'études sur la pharmacocinétique de la lévodopa et de la carbidopa chez les patients souffrant de troubles hépatiques.
Utilisation gériatrique
Dans les études de pharmacocinétique menées chez des volontaires sains après une seule dose de carbidopa- lévodopa- et entacapone (comme stalevo ou en tant que comprimés de carbidopa / lévodopa et de comtan):
Levodopa
L'AUC de Levodopa est significativement (en moyenne 10% à 20%) plus élevée chez les personnes âgées (60 ans à 75 ans) que les sujets plus jeunes (45 ans à 60 ans). Il n'y a pas de différence significative dans le CMAX de la lévodopa entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 à 75 ans).
Carbidopa
Il n'y a pas de différence significative dans le CMAX et l'ASUC de la carbidopa entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 ans à 75 ans).
Entacapone
L'AUC de l'entacapone est significativement (en moyenne 15%) plus élevée chez les personnes âgées (60 ans à 75 ans) que les sujets plus jeunes (45 à 60 ans). Il n'y a pas de différence significative dans le CMAX de l'entacapone entre les jeunes (45 ans à 60 ans) et les sujets âgés (60 à 75 ans).
Genre
Pharmacocinétique following a single dose of carbidopa levodopa et entacapone together either as Stalevo or as separate carbidopa/levodopa et Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Levodopa
L'exposition au plasma (AUC et CMAX) de la lévodopa est significativement plus élevée chez les femmes que les hommes (en moyenne 40% pour l'ASC et 30% pour CMAX). Ces différences s'expliquent principalement par le poids corporel. Une autre littérature publiée a montré un effet de genre significatif (concentrations plus élevées chez les femmes) même après correction du poids corporel.
Carbidopa
Il n'y a pas de différence entre les sexes dans la pharmacocinétique de la carbidopa.
Entacapone
Il n'y a pas de différence entre les sexes dans la pharmacocinétique de l'entacapone.
Études d'interaction médicamenteuse Médicament métabolisé par comt
Lorsqu'une seule dose d'entacapone de 400 mg a été donnée avec une isoprénaline intraveineuse (isoprotérénol) et une épinéphrine sans inhibiteur de la lévodopa et de la dopa décarboxylase coadmins, les changements maximaux moyens de la fréquence cardiaque pendant la perfusion étaient respectivement environ 50% et 80% plus élevés que le placebo pour l'isoprénaline et l'épinéphrine respectivement.
Les médicaments connus pour être métabolisés par COMT doivent être administrés avec prudence chez les patients recevant de l'entacapone quelle que soit la voie d'administration [voir Interactions médicamenteuses ].
Médicaments métabolisés via CYP2C9
En raison de son affinité avec le CYP2C9 in vitro, l'entacapone peut potentiellement interférer avec les médicaments avec le métabolisme dépendant de cette isoenzyme. Dans une étude d'interaction chez des volontaires sains, Entacapone a augmenté l'ASC de R-warfarine en moyenne de 18% et les valeurs INR ont augmenté en moyenne de 13% [voir Interactions médicamenteuses ].
Niveaux hormonaux
Des ingrédients de Stalevo Levodopa est connu pour déprimer la sécrétion de prolactine et augmenter hormone de croissance niveaux.
Études cliniques
L'efficacité de l'entacapone en complément de la lévodopa dans le traitement de la maladie de Parkinson a été établie dans trois études multicentriques multicentriques de 24 semaines en double aveugle à double aveugle chez les patients atteints de la maladie de Parkinson. Dans 2 de ces études (études 1 et 2), la maladie des patients fluctuait, c'est-à-dire, a été caractérisée par des périodes documentées de (périodes de fonctionnement relativement bon) et désactivées (périodes de fonctionnement relativement médiocre) malgré une thérapie par levodopa optimale. Il y a également eu une période de retrait après 6 mois de traitement. Dans le troisième essai, les patients n'étaient pas tenus de subir des fluctuations. Avant la partie contrôlée de ces études, les patients ont été stabilisés sur la lévodopa pendant 2 semaines à 4 semaines.
Il existe une expérience limitée en utilisant l'entacapone chez les patients qui ne souffrent pas de fluctuations.
Dans les études 1 et 2, les patients ont été randomisés pour recevoir un placebo ou un entacapone 200 mg administré en concomitance avec chaque dose de carbidopa / lévodopa (jusqu'à 10 fois par jour, mais les patients ont en moyenne 4 doses à 6 doses par jour). La partie en double aveugle des deux études a duré 6 mois. Les patients ont périodiquement enregistré le temps passé dans les états de marche et de désactivation dans les journaux intimes pendant toute la durée de l'essai. Dans une étude menée dans les pays nordiques, la principale mesure des résultats a été le temps moyen passé à l'état à l'état pendant un jour enregistré de 18 heures (6 h à minuit). Dans l'autre étude, la principale mesure des résultats était la proportion de temps éveillé passé plus de 24 heures à l'état.
En plus de la mesure principale des résultats, le temps passé à l'état hors de l'état a été évalué et les patients ont également été évalués par les sous-parties de l'échelle de notation de la maladie de Parkinson unifiée (UPDR) Une échelle d'évaluation multi-éléments fréquemment utilisée destiné à évaluer les activités de la thérapie (partie I) de la vie quotidienne (partie II) (partie V et VI); L'évaluation globale d'un enquêteur et du patient de l'état clinique, une échelle subjective de 7 points conçue pour évaluer le fonctionnement global de la maladie de Parkinson; et le changement de dose quotidienne de carbidopa / lévodopa.
rispéridone d'autres médicaments dans la même classe
Dans l'étude 1 171, les patients ont été randomisés dans 16 centres en Finlande, Norvège, la Suède et le Danemark (étude 1) qui ont tous reçu un inhibiteur concomitant de la lévodopa plus dopa décarboxylase (soit carbidopa / lévodopa ou bensérazide / lévodopa). Dans l'étude 2, 205 patients ont été randomisés dans 17 centres en Amérique du Nord (États-Unis et Canada); Tous les patients ont reçu une carbidopa / lévodopa concomitante.
Les tableaux suivants (tableau 4 et tableau 5) affichent les résultats de ces deux études:
Tableau 4: Résultats de l'efficacité de l'étude 1
| Mesure primaire du journal intime (à partir d'une journée du journal de 18 heures) | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 * | valeur p contre placebo | |
| Heures de temps éveillé | |||
| Placebo | 9.2 | 0.1 | - |
| Entacapone | 9.3 | 1.5 | Moins de 0,001 |
| Durée de l'heure après la dose de première am (HRS) | |||
| Placebo | 2.2 | 0.0 | - |
| Entacapone | 2.1 | 0,2 | Moins de 0,05 |
| Mesures secondaires du journal intime (à partir d'une journée du journal de 18 heures) † | |||
| Heures de congé | |||
| Placebo | 5.3 | 0.0 | - |
| Entacapone | 5.5 | -1.3 | Moins de 0,001 |
| Proportion de temps éveillé sur ‡ (%) | |||
| Placebo | 63.8 | 0.6 | - |
| Entacapone | 62.7 | 9.3 | Moins de 0,001 |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 705 | 14 | - |
| Entacapone | 701 | -87 | Moins de 0,001 |
| Fréquence des apports quotidiens de la lévodopa | |||
| Placebo | 6.1 | 0.1 | - |
| Entacapone | 6.2 | - 0,4 | Moins de 0,001 |
| Autres mesures secondaires | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 | valeur p contre placebo | |
| Global (global) de l'enquêteur a amélioré§ § | |||
| Placebo | - | 28 | - |
| Entacapone | - | 56 | Moins de 0,01 |
| Global (global) du patient a amélioré§ | |||
| Placebo | - | 22 | - |
| Entacapone | - | 39 | N.s.¶ |
| UPDRS TOTAL | |||
| Placebo | 37.4 | -1.1 | - |
| Entacapone | 38.5 | -4.8 | Moins de 0,01 |
| Moteur de monte | |||
| Placebo | 24.6 | -0.7 | - |
| Entacapone | 25.5 | -3.3 | Moins de 0,05 |
| UPDRS ADL | |||
| Placebo | 11.0 | -0.4 | - |
| Entacapone | 11.2 | -1.8 | Moins de 0,05 |
| *Signifier; Les valeurs du mois 6 représentent la moyenne des semaines 8 16 et 24 par mesure des résultats définis par le protocole. † Les valeurs P pour les mesures secondaires sont des valeurs P nominales sans aucun ajustement pour la multiplicité. ‡ Pas un critère de terminaison pour cette étude mais un critère d'évaluation principal dans l'étude nord-américaine. § Au moins d'une catégorie change au point de terminaison. ¶S pas significatif. |
Tableau 5: Résultats de l'efficacité de l'étude 2
| Mesure primaire du journal intime (pour une journée de journal 24h / 24) | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 * | valeur p contre placebo | |
| Pour cent de temps éveillé | |||
| Placebo | 60.8 | 2.0 | - |
| Entacapone | 60.0 | 6.7 | Moins de 0,05 |
| Mesures secondaires du journal intime (pour une journée du journal 24h / 24) † | |||
| Heures de congé | |||
| Placebo | 6.6 | -0.3 | - |
| Entacapone | 6.8 | -1.2 | Moins de 0,01 |
| Heures de temps éveillé | |||
| Placebo | 10.3 | 0.4 | - |
| Entacapone | 10.2 | 1.0 | N.S. ‡ |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 758 | 19 | - |
| Entacapone | 804 | -93 | Moins de 0,001 |
| Fréquence des apports quotidiens de la lévodopa | |||
| Placebo | 6.0 | 0,2 | - |
| Entacapone | 6.2 | 0.0 | N.S. ‡ |
| Autres mesures secondaires† | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 | valeur p contre placebo | |
| Global (global) de l'enquêteur a amélioré§ § | |||
| Placebo | - | 21 | - |
| Entacapone | - | 34 | Moins de 0,05 |
| Global (global) du patient a amélioré§ | |||
| Placebo | - | 20 | - |
| Entacapone | - | 31 | Moins de 0,05 |
| UPDRS TOTAL¶ | |||
| Placebo | 35.6 | 2.8 | - |
| Entacapone | 35.1 | -0.6 | Moins de 0,05 |
| Moteur de monte ¶ | |||
| Placebo | 22.6 | 1.2 | - |
| Entacapone | 22.0 | -0.9 | Moins de 0,05 |
| UPDRS ADL¶ | |||
| Placebo | 11.7 | 1.1 | - |
| Entacapone | 11.9 | 0.0 | Moins de 0,05 |
| *Signifier; Les valeurs du mois 6 représentent la moyenne des semaines 8 16 et 24 par mesure des résultats définis par le protocole. † Les valeurs P pour les mesures secondaires sont des valeurs P nominales sans aucun ajustement pour la multiplicité. ‡ Pas significatif. § Au moins d'une catégorie change au point de terminaison. ¶Score Change à un point final similaire à l'étude nordique. |
Les effets sur le temps ne différaient pas par l'âge de poids sexuel La gravité de la maladie à la dose de lévodopa de base et un traitement simultané avec des agonistes de dopamine ou de la sélégiline.
Retrait de l'entacapone
Dans l'étude 2, un retrait brusque de l'entacapone sans altération de la dose de carbidopa / lévodopa a entraîné une aggravation significative des fluctuations par rapport au placebo. Dans certains cas, les symptômes étaient légèrement pires qu'au départ, mais sont revenus à une gravité approximativement de base dans les 2 semaines suivant l'augmentation de la dose de levodopa en moyenne de 80 mg. Dans l'étude 1, une aggravation significative des symptômes parkinsoniens a été observée après le retrait de l'entacapone, comme évalué 2 semaines après le retrait du médicament. À cette phase, les symptômes étaient approximativement à la gravité de base après l'augmentation de la dose de levodopa d'environ 50 mg.
Dans le troisième essai contrôlé par placebo (étude 3), un total de 301 patients ont été randomisés dans 32 centres en Allemagne et en Autriche. Dans cet essai, comme dans les 2 autres études, Entacapone 200 mg a été administré avec chaque dose d'inhibiteur de la lévodopa et de la dopa décarboxylase (jusqu'à 10 fois par jour) et les parties II et III totales et iii et le total au temps étaient les principales mesures de l'efficacité. Les résultats des mesures primaires ainsi que pour certaines mesures secondaires sont présentés dans le tableau 6.
Tableau 6: Résultats de l'efficacité de l'étude 3
| Mesures primaires | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 | valeur p contre placebo (LOCF) | |
| UPDRSADL * | |||
| Placebo | 12.0 | 0,5 | - |
| Entacapone | 12.4 | -0.4 | Moins de 0,05 |
| Moteur de monte* | |||
| Placebo | 24.1 | 0.1 | - |
| Entacapone | 24.9 | -2.5 | Moins de 0,05 |
| Heures de temps éveillé (Home Diary)† | |||
| Placebo | 10.1 | 0,5 | - |
| Entacapone | 10.2 | 1.1 | N.S. ‡ |
| Mesures secondaires§ | |||
| Base de base | Changement par rapport à la ligne de base au mois 6 | valeur p contre placebo | |
| UPDRS TOTAL * | |||
| Placebo | 37.7 | 0.6 | - |
| Entacapone | 39.0 | -3.4 | Moins de 0,05 |
| Pour cent de temps éveillé (Home Diary) ** | |||
| Placebo | 59.8 | 3.5 | - |
| Entacapone | 62.0 | 6.5 | N.S. ‡ |
| Heures de congé (Home Diary) | |||
| Placebo | 6.8 | -0.6 | - |
| Entacapone | 6.3 | -1.2 | 0.07 |
| Levodopa Total Daily Dose (mg)* | |||
| Placebo | 572 | 4 | - |
| Entacapone | 566 | -35 | N.S. |
| Fréquence de l'apport quotidien de la lévodopa * | |||
| Placebo | 5.6 | 0,2 | - |
| Entacapone | 5.4 | 0.0 | Moins de 0,01 |
| Global (global)% amélioréoit | |||
| Placebo | - | 34 | - |
| Entacapone | - | 38 | N.S. ‡ |
| * Population totale; changement de score au point de terminaison. † fluctuant de la population avec 5 doses à 10 doses; changement de score au point de terminaison. ‡ Pas significatif. Les valeurs §p pour les mesures secondaires sont des valeurs p nominales sans aucun ajustement pour la multiplicité. ¶Population totale; Au moins une catégorie change au point final. |
Informations sur les patients pour Stalevo
S'endormir pendant les activités de la vie quotidienne et de la somnolence
Conseillez les patients sur le potentiel d'effets sédatifs associés à Stalevo, y compris la somnolence et sur la possibilité de s'endormir tout en se livrant à des activités de vie quotidienne. Parce que la somnolence peut être une réaction indésirable fréquente avec des conséquences potentiellement graves, les patients ne devraient pas conduire un véhicule à moteur à faire fonctionner des machines lourdes ou s'engager dans d'autres activités potentiellement dangereuses jusqu'à ce qu'elles aient acquis une expérience suffisante avec STALEVO pour déterminer si cela affecte ou non leurs performances mentales et / ou motrices [voir adversation [voir Avertissements et précautions ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Conseiller aux patients de parler avec leur prescripteur de soins de santé avant de prendre des médicaments en séduisant ou d'autres dépresseurs du SNC (par exemple les antidépresseurs antipsychotiques benzodiazépines, etc.) en raison des effets additifs possibles en combinaison avec Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Informer les patients qu'ils peuvent développer une hypotension symptomatique (ou asymptomatique) posturale (orthostatique) ou une hypotension non orthostatique lors de la prise de Stalevo. L'hypotension / hypotension orthostatique peut se produire plus fréquemment pendant le traitement initial. Les patients ne devraient pas augmenter rapidement après s'asseoir ou se coucher, surtout s'ils l'ont fait pendant des périodes prolongées et surtout lors de l'initiation du traitement avec Stalevo.
Conseillez les patients sur le potentiel de syncope chez les patients utilisant des agonistes de dopamine. Pour cette raison, informer les patients de la possibilité de syncope tout en prenant Stalevo [voir Avertissements et précautions ].
Dyskinésies
Informer les patients que Stalevo peut provoquer et / ou exacerber les dyskinésies préexistantes [voir Avertissements et précautions ].
Hallucinations et / ou comportement psychotique
Informer les patients que les hallucinations et autres comportements de type psychotique peuvent se produire lors de la prise de Stalevo [voir Avertissements et précautions ].
Contrôle des impulsions et / ou comportements compulsifs
Informer les patients qu'ils peuvent ressentir des comportements de contrôle des impulsions et / ou compulsifs tout en prenant un ou plusieurs médicaments utilisés pour le traitement de la maladie de Parkinson, y compris Stalevo. Demandez aux patients sur le développement des envies de jeu nouvelles ou accrues les envies sexuelles les envies de dépenses incontrôlées ou d'autres envies intenses tout en étant traitées avec Stalevo. Conseiller aux patients d'informer leur médecin ou leur fournisseur de soins de santé s'ils connaissent des envies de jeu nouvelles ou accrues accrues les envies sexuelles ou d'autres envies intenses tout en prenant Stalevo. Les médecins devraient envisager la réduction de la dose ou l'arrêt du médicament si un patient développe de telles envies tout en prenant Stalevo [voir Avertissements et précautions ].
Hyperpyrexie et confusion du retrait émergent
Informer les patients qu'ils peuvent développer de la fièvre et de la confusion dans le cadre d'un syndrome ressemblant à la NMS et éventuellement avec d'autres caractéristiques cliniques (par exemple, la rigidité musculaire dysfonctionnement hyper ou hypotension, etc.). Ce syndrome de fièvre et de confusion peut se produire particulièrement avec des réductions de dose ou un retrait de Stalevo mais peut également se développer après le début du traitement. Conseiller aux patients de contacter leur fournisseur de soins de santé s'ils souhaitent interrompre ou diminuer la dose de Stalevo et contacter un fournisseur de soins de santé s'ils développent de la fièvre et de la confusion [voir Avertissements et précautions ].
Diarrhée And Colitis
Informez les patients que la diarrhée peut se produire avec Stalevo et qu'il peut avoir un début retardé. Parfois, la diarrhée prolongée peut être causée par la colite (inflammation du gros intestin). Les patients atteints de diarrhée doivent boire des liquides pour maintenir une hydratation adéquate et surveiller la perte de poids. Si la diarrhée associée à STALEVO est prolongée, ce qui devrait entraîner la résolution. Si la diarrhée se poursuit après avoir arrêté des enquêtes de diagnostic à Stalevo peut être nécessaire. Dans certains cas, la diarrhée peut être associée à la colite [voir Avertissements et précautions ].
Rhabdomyolyse
Informer les patients qu'ils peuvent développer une rhabdomyolyse et une myalgie s'ils éprouvent une activité motrice prolongée, y compris la dyskinésie. Cet événement peut également être associé à la fièvre et à la confusion [voir Avertissements et précautions ].
Nausée And Vomissement
Informer les patients que Stalevo peut provoquer des nausées et des vomissements peuvent survenir plus fréquemment pendant le traitement initial et peuvent nécessiter un ajustement de la dose.
Instructions pour une utilisation
Demandez aux patients de prendre Stalevo uniquement comme prescrit. Demandez aux patients de ne prendre qu'un seul comprimé de Stalevo à chaque intervalle de dosage. Demandez aux patients de ne pas prendre plusieurs comprimés ou des portions supplémentaires de comprimés pour obtenir une dose plus élevée de lévodopa. Conseiller aux patients de ne pas séparer l'écrasement ou de mâcher Stalevo.
Informez le patient que Stalevo est une formulation de carbidopa / lévodopa combinée à l'entacapone conçu pour commencer la libération d'ingrédients dans les 30 minutes suivant l'ingestion. Il est important que Stalevo soit pris à intervalles réguliers selon le calendrier décrit par le médecin. ATTENTION Le patient de ne pas modifier le schéma posologique prescrit et de ne pas ajouter de médicaments antiparkinsoniens supplémentaires, y compris d'autres préparations carbidopa / lévodopa sans consulter d'abord le médecin.
Conseillez les patients que les épisodes interdits (le port de l'effet du médicament) se produisent à la fin de l'intervalle de dosage, mais des épisodes hors de terre imprévisibles peuvent se produire à tout moment. Conseillez au patient d'informer un fournisseur de soins de santé pour d'éventuels ajustements de traitement si une telle réponse pose un problème à la vie quotidienne du patient.
Conseillez les patients que la coloration foncée (brun rouge ou noir) peut apparaître dans l'urine ou la sueur de la salive après avoir pris Stalevo. Bien que la couleur semble être cliniquement insignifiante que les vêtements peuvent être décolorés.
Conseiller les patients qu'un changement de régime alimentaire en aliments riches en protéines peut retarder l'absorption de la lévodopa. Une acidité excessive retarde également la vidange de l'estomac, retardant ainsi l'absorption de la lévodopa. Les sels de fer (comme dans les comprimés multi-vitamines) peuvent également réduire l'efficacité de Stalevo.
Grossesse
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant la thérapie [voir Utiliser dans des populations spécifiques ].
Lactation
Demandez aux patients de notifier leur fournisseur de soins de santé s'ils ont l'intention d'allaiter ou d'allaiter un nourrisson [voir Utiliser dans des populations spécifiques ].
